解答题-原理综合题 较难0.4 引用1 组卷162
氮氧化物(NOx)是常见的大气污染物,能引起雾霾、光化学烟雾、酸雨等环境问题。因此,研究氮氧化物(NOx)的无害化处理对治理大气污染、建设生态文明具有重要意义。请按要求回答下列问题:
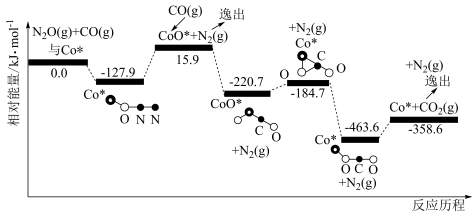
(1)一氧化二氮是一种强大的温室气体,可用CO(g)在Co*的催化作用下还原N2O(g)以除去污染,反应的化学方程式为CO(g)+N2O(g) CO2(g)+N2(g),其反应历程和能量变化如图所示(逸出后物质认为状态未发生变化,在图中略去)。
CO2(g)+N2(g),其反应历程和能量变化如图所示(逸出后物质认为状态未发生变化,在图中略去)。
第一步:Co*(s)+N2O(g) CoO*(s)+N2(g) ΔH=+15.9kJ/mol;
CoO*(s)+N2(g) ΔH=+15.9kJ/mol;
第二步:___________ (填写第二步反应的热化学方程式)。
(2)汽车尾气中的NO可以和CO在催化转换器中发生反应,以减少尾气污染。某温度时,向2L恒容密闭体系中通入2molCO和1molNO气体,发生反应2CO(g)+2NO(g) N2(g)+2CO2(g),下列能说明反应达到平衡状态的是
N2(g)+2CO2(g),下列能说明反应达到平衡状态的是___________ (填序号)。
a.2v正(NO)=v逆(N2)
b.体系中混合气体密度不再改变
c.CO与NO转化率的比值不再改变
d.该温度下, 的值不再改变
的值不再改变
(3)某研究小组探究温度和催化剂对CO、NO转化率的影响。将CO和NO按物质的量之比1∶1以一定的流速分别通过两种催化剂(Cat-1和Cat-2)进行反应,相同时间内测量逸出气体中NO的含量,从而确定尾气脱氮率(即NO的转化率),结果如图所示:___________ (填“Cat-1”或“Cat-2”)。
②催化剂在Cat-2条件下,450℃后,脱氮率随温度升高而下降的原因是___________ 。
(4)用H2也可还原NO气体,其反应为2H2(g)+2NO(g) N2(g)+2H2O(g) ΔH=-752kJ/mol。
N2(g)+2H2O(g) ΔH=-752kJ/mol。
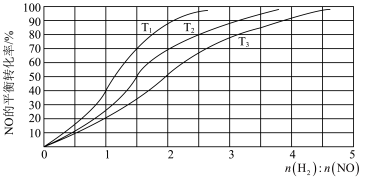
为研究H2和NO的起始投料比对NO平衡转化率的影响,分别在不同温度下,向三个体积均为aL的刚性密闭容器中加入一定量H2和NO发生反应,实验结果如图:___________ ﹔判断理由是___________ 。
②T1温度下,充入H2、NO分别为3mol、3mol,容器内的压强为wPa,反应进行到6min时达平衡,0~6min内N2的平均反应速率为___________ mol·L-1·min-1,该反应的平衡常数Kp=___________ (写出计算表达式)。
(1)一氧化二氮是一种强大的温室气体,可用CO(g)在Co*的催化作用下还原N2O(g)以除去污染,反应的化学方程式为CO(g)+N2O(g)
第一步:Co*(s)+N2O(g)
第二步:
(2)汽车尾气中的NO可以和CO在催化转换器中发生反应,以减少尾气污染。某温度时,向2L恒容密闭体系中通入2molCO和1molNO气体,发生反应2CO(g)+2NO(g)
a.2v正(NO)=v逆(N2)
b.体系中混合气体密度不再改变
c.CO与NO转化率的比值不再改变
d.该温度下,
(3)某研究小组探究温度和催化剂对CO、NO转化率的影响。将CO和NO按物质的量之比1∶1以一定的流速分别通过两种催化剂(Cat-1和Cat-2)进行反应,相同时间内测量逸出气体中NO的含量,从而确定尾气脱氮率(即NO的转化率),结果如图所示:
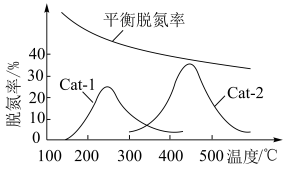
②催化剂在Cat-2条件下,450℃后,脱氮率随温度升高而下降的原因是
(4)用H2也可还原NO气体,其反应为2H2(g)+2NO(g)
为研究H2和NO的起始投料比对NO平衡转化率的影响,分别在不同温度下,向三个体积均为aL的刚性密闭容器中加入一定量H2和NO发生反应,实验结果如图:
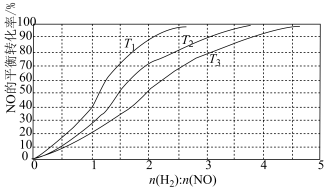
②T1温度下,充入H2、NO分别为3mol、3mol,容器内的压强为wPa,反应进行到6min时达平衡,0~6min内N2的平均反应速率为
2024·贵州黔东南·三模
类题推荐
以NOx为主要成分的雾霾综合治理是当前重要的研究课题,其中汽车尾气的处理尤为重要。请回答下列问题:
(1)NO和CO均为汽车尾气的成分,在催化转换器中二者可发生反应2CO(g)+2NO(g)=N2(g)+2CO2(g)减少尾气污染。
①已知:N2(g)+O2(g)= 2NO(g) △H= a kJ/mol
C(s)+O2(g)= CO2(g) △H = b kJ/mol
2C(s)+O2(g) = 2CO(g) △H = c kJ/mol
则2CO(g)+2NO(g)=N2(g)+2CO2(g) △H =_______ (用含a、b、c的表达式表示)。
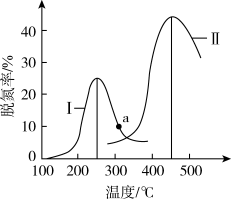
②某研究小组探究催化剂对CO、NO转化的影响。将CO和 NO以一定的流速通过两种不同的催化剂Ⅰ和Ⅱ进行反应,相同时间内测量逸出气体中N2的含量,从而确定尾气脱氮率(即NO的转化率)结果如图(对应曲线Ⅰ和Ⅱ)所示。由图可知:要达到最大脱氮率,应采取的最佳实验条件为_______ ;若低于200℃,图中曲线Ⅰ脱氮率随温度升高变化不大的主要原因为_______ 。
(2)①在500℃时,向恒容密闭体系中通入1 mol NO和 1 mol CO进行反应2CO(g)+ 2NO(g) N2(g)+ 2CO2(g)时,下列描述能说明反应达到平衡状态的是
N2(g)+ 2CO2(g)时,下列描述能说明反应达到平衡状态的是_______ 。(填字母)
A.单位时间内,断裂2 mol C=O键同时生成1 mol N≡N键
B.体系中混合气体的密度不变
C.混合气体的平均相对分子质量不变
D.CO与NO的转化率比值不再改变
②一定温度下,向恒容容器中通入等物质的量的NO和CO气体,测得容器中压强随时间的变化关系如表所示:
该条件下反应的平衡常数Kp=_______ (kPa)-1(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
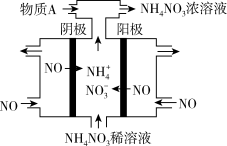
(3)间接电化学法可对NO进行无害化处理,其工作原理如图所示,为使电解产物全部转化为NH4NO3,需要补充物质A,A是_______ ,理由是_______ 。
(1)NO和CO均为汽车尾气的成分,在催化转换器中二者可发生反应2CO(g)+2NO(g)=N2(g)+2CO2(g)减少尾气污染。
①已知:N2(g)+O2(g)= 2NO(g) △H= a kJ/mol
C(s)+O2(g)= CO2(g) △H = b kJ/mol
2C(s)+O2(g) = 2CO(g) △H = c kJ/mol
则2CO(g)+2NO(g)=N2(g)+2CO2(g) △H =
②某研究小组探究催化剂对CO、NO转化的影响。将CO和 NO以一定的流速通过两种不同的催化剂Ⅰ和Ⅱ进行反应,相同时间内测量逸出气体中N2的含量,从而确定尾气脱氮率(即NO的转化率)结果如图(对应曲线Ⅰ和Ⅱ)所示。由图可知:要达到最大脱氮率,应采取的最佳实验条件为

(2)①在500℃时,向恒容密闭体系中通入1 mol NO和 1 mol CO进行反应2CO(g)+ 2NO(g)
A.单位时间内,断裂2 mol C=O键同时生成1 mol N≡N键
B.体系中混合气体的密度不变
C.混合气体的平均相对分子质量不变
D.CO与NO的转化率比值不再改变
②一定温度下,向恒容容器中通入等物质的量的NO和CO气体,测得容器中压强随时间的变化关系如表所示:
| t/min | 0 | 1 | 2 | 3 | 4 | 5 |
| p/kPa | 200 | 185 | 173 | 165 | 160 | 160 |
(3)间接电化学法可对NO进行无害化处理,其工作原理如图所示,为使电解产物全部转化为NH4NO3,需要补充物质A,A是

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网