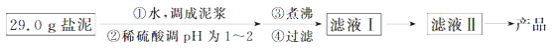解答题-工业流程题 较难0.4 引用1 组卷105
盐泥是氯碱工业的废渣,主要含镁、钙、铁、铝、锰的硅酸盐和碳酸盐,可用于提取 ,工艺流程如图所示:
,工艺流程如图所示: .常见氢氧化物的溶度积Ksp如下表:
.常见氢氧化物的溶度积Ksp如下表:
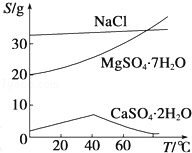
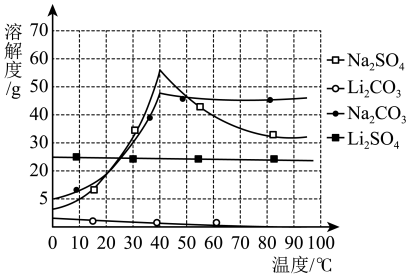
 .物质的溶解度S(g/100g水)
.物质的溶解度S(g/100g水)
(1)基态Fe原子价层电子轨道排布图为___________
(2)滤渣 的主要成分为
的主要成分为___________ (填化学式)。
(3)流程中加NaClO溶液煮沸10min后,立即趁热过滤的原因是___________ 。
(4)滤渣 含有
含有 、写出生成
、写出生成 的离子反应方程式
的离子反应方程式___________ 。
(5)滤液 中
中
___________ 。
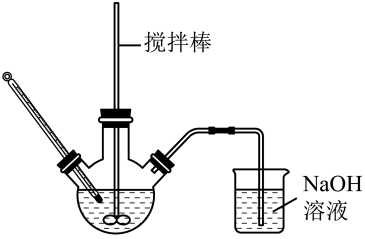
(6)从滤液 中获得晶体的实验操作步骤为:①向滤液中加入NaOH,②过滤,得沉淀,③向沉淀中加入稀硫酸,④
中获得晶体的实验操作步骤为:①向滤液中加入NaOH,②过滤,得沉淀,③向沉淀中加入稀硫酸,④___________ ,⑤过滤、洗涤得产品。
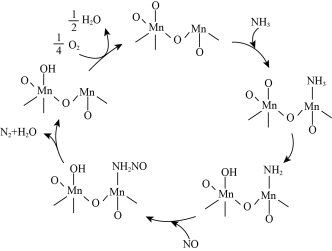
(7) 作催化剂、氨催化还原脱除NO的一种催化机理示意图如图。从化学键的角度解释
作催化剂、氨催化还原脱除NO的一种催化机理示意图如图。从化学键的角度解释 能结合
能结合 的原因:
的原因:___________ 。

| 温度/℃ | 0 | 10 | 20 | 40 | 60 | 80 | 100 |
| 20.3 | 23.3 | 25.2 | 30.8 | 35.3 | 35.8 | 33.4 | |
| 0.223 | 0.224 | 0.255 | 0.265 | 0.244 | 0.234 | 0.205 |
(1)基态Fe原子价层电子轨道排布图为
(2)滤渣
(3)流程中加NaClO溶液煮沸10min后,立即趁热过滤的原因是
(4)滤渣
(5)滤液
(6)从滤液
(7)
2024·广西贵港·模拟预测
类题推荐
以某工业废锰渣(含MnO2及少量KOH、MgO、Fe2O3)为原料制备MnSO4晶体,其工艺流程如下:

该工艺条件下金属离子开始沉淀和完全沉淀 的pH如表所示:
的pH如表所示:
(1)“反应Ⅰ”中加入硫铁矿(主要成分FeS2)将MnO2还原为 。滤渣1的主要成分除FeS2外,还有一种相对分子质量为256的单质,其化学式为
。滤渣1的主要成分除FeS2外,还有一种相对分子质量为256的单质,其化学式为___________ 。
(2)“反应Ⅱ”中主要反应的离子方程式为___________ 。
(3)“反应Ⅲ”中,“某碳酸盐”的化学式为___________ ,加热的目的是___________ 应调节溶液pH的范围是___________ 。
(4)测定产品纯度。取制得的MnSO4晶体0.3020g,溶于适量水中,加硫酸酸化;用过量NaBiO3(难溶于水)将 完全氧化为
完全氧化为 ,过滤、洗涤;将几次洗涤的滤液与过滤所得的滤液合并,向其中加入Na2C2O4固体1.072g;充分反应后,用
,过滤、洗涤;将几次洗涤的滤液与过滤所得的滤液合并,向其中加入Na2C2O4固体1.072g;充分反应后,用 溶液滴定,用去40.00mL。
溶液滴定,用去40.00mL。
已知: (未配平)。
(未配平)。
①用KMnO4溶液滴定时,滴定终点的现象为___________ 。
②计算产品中MnSO4的质量分数___________ (写出计算过程)。

该工艺条件下金属离子开始沉淀和完全沉淀
| 金属离子 | ||||
| 开始沉淀pH | 2.10 | 7.45 | 9.27 | 9.60 |
| 完全沉淀pH | 3.20 | 8.95 | 10.87 | 11.13 |
(1)“反应Ⅰ”中加入硫铁矿(主要成分FeS2)将MnO2还原为
(2)“反应Ⅱ”中主要反应的离子方程式为
(3)“反应Ⅲ”中,“某碳酸盐”的化学式为
(4)测定产品纯度。取制得的MnSO4晶体0.3020g,溶于适量水中,加硫酸酸化;用过量NaBiO3(难溶于水)将
已知:
①用KMnO4溶液滴定时,滴定终点的现象为
②计算产品中MnSO4的质量分数
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网