多选题 适中0.65 引用2 组卷136
利用钒电池电解制备ClO2的装置如图所示。下列说法中错误的是
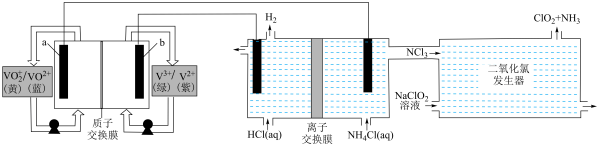
| A.工作时,b极区溶液由绿色变成紫色 |
| B.离子交换膜为阳离子交换膜 |
| C.生成的H2和NH3的物质的量之比为3∶1 |
| D.当钒电池有2 mol |
2024·山东日照·模拟预测
类题推荐
全钒液流电池是一种新型的绿色环保储能系统,工作原理如图1。该电池放电时总反应为V2++VO +2H+=V3+ +VO2+ +H2O。图2是太阳能电池工作示意图,与图1装置联合可实现能量的转化和储存。下列有关说法错误的是
+2H+=V3+ +VO2+ +H2O。图2是太阳能电池工作示意图,与图1装置联合可实现能量的转化和储存。下列有关说法错误的是
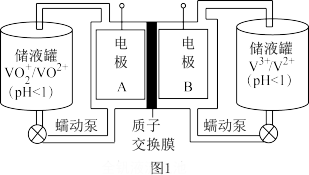



| A.储能时,电极A接太阳能电池的N电极,电极B接P电极 |
| B.放电时,电极B的电极反应式为V2+-e-=V3+ |
| C.储能时,电极A的电极反应式为VO2+-e- +H2O= |
| D.放电时,每转移1 mole-就有1 mol H+通过质子交换膜进入电极A区 |
全钒液流储能电池是一种新型的绿色环保储能系统(工作原理如图,电解液含硫酸)。该电池负载工作时,左罐颜色由黄色变为蓝色。
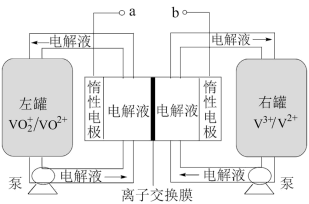
下列说法错误的是

| 离子种类 | VO2+ | V3+ | V2+ | |
| 颜色 | 黄色 | 蓝色 | 绿色 | 紫色 |
| A.该电池工作原理为VO2++VO2++2H+ |
| B.a和b接用电器时,左罐电动势小于右罐,电解液中的H+通过离子交换膜向左罐移动 |
| C.电池储能时,电池负极溶液颜色变为紫色 |
| D.电池无论是负载还是储能,每转移1 mol电子,均消耗1 mol氧化剂 |
全钒电池以惰性材料作电极,在电解质溶液中发生的电池总反应为VO2+(蓝色)+H2O+V3+(绿色)  VO2+(黄色)+V2+(紫色)+2H+。下列说法错误的是
VO2+(黄色)+V2+(紫色)+2H+。下列说法错误的是
 VO2+(黄色)+V2+(紫色)+2H+。下列说法错误的是
VO2+(黄色)+V2+(紫色)+2H+。下列说法错误的是| A.充电时,反应每生成2 mol H+时转移的电子的物质的量为1 mol |
| B.充电时,阳极附近溶液由绿色逐渐变为紫色 |
| C.放电时,负极反应为V2+-e-=V3+ |
| D.放电过程中,正极附近溶液的酸性减弱 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


