解答题-工业流程题 适中0.65 引用2 组卷174
以低品位铜钴矿(主要成分为 、
、 、
、 ,还有少量的FeO、
,还有少量的FeO、 、CaO、MgO等杂质)为原料制备硫酸铜晶体和
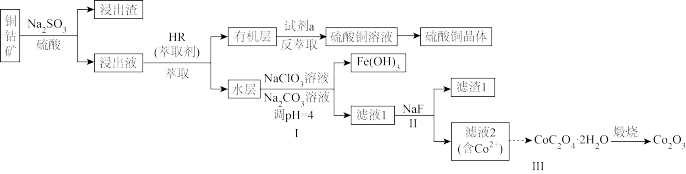
、CaO、MgO等杂质)为原料制备硫酸铜晶体和 的一种工艺流程如下:
的一种工艺流程如下:
②萃取时发生反应
(1)铜钴矿浸出前要预先粉碎,其目的是______ 。
(2)浸出步骤铜钴矿中的 转化为
转化为 ,该反应的离子方程式为
,该反应的离子方程式为______ 。
(3)加入试剂a______ 可使萃取剂再生。
(4)对于过程I:
①加 溶液作用是
溶液作用是______ 。
②通过计算判断 是否沉淀完全并简述理由
是否沉淀完全并简述理由______ 。(一般认为溶液中离子浓度小于 时沉淀完全)
时沉淀完全)
(5)滤渣1成分______ 。
(6) 在足量空气中煅烧生成
在足量空气中煅烧生成 ,写出煅烧过程中的化学反应方程式
,写出煅烧过程中的化学反应方程式______ 。
(7) 产品纯度测定方法如下:
产品纯度测定方法如下: 与EDTA-2Na按物质的量1:1反应,若滴定至终点时消耗EDTA-2Na标准液体积为20.00mL,则
与EDTA-2Na按物质的量1:1反应,若滴定至终点时消耗EDTA-2Na标准液体积为20.00mL,则 产品纯度为
产品纯度为______ 。( 的摩尔质量是
的摩尔质量是 )
)
物质 | ||||||
(1)铜钴矿浸出前要预先粉碎,其目的是
(2)浸出步骤铜钴矿中的
(3)加入试剂a
(4)对于过程I:
①加
②通过计算判断
(5)滤渣1成分
(6)
(7)
2024·北京通州·一模
类题推荐
以低品位铜钴矿(主要成分为 ,还有少量的
,还有少量的 等杂质)为原料制备硫酸铜晶体和
等杂质)为原料制备硫酸铜晶体和 的一种工艺流程如下:
的一种工艺流程如下:
②萃取时发生反应 。
。
(1)漫出步骤铜钴矿中的 转化为
转化为 ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
(2)加入试剂
___________ 可使萃取剂再生。
(3)对于过程
①加 溶液作用是
溶液作用是___________ 。
②判断 是否沉淀完全并简述理由
是否沉淀完全并简述理由___________ 。(离子浓度小于 时可视为沉淀完全)。
时可视为沉淀完全)。
(4)滤渣1成分为___________ 。
(5) 在足量空气中煅烧生成
在足量空气中煅烧生成 ,写出煅烧过程的化学反应方程式
,写出煅烧过程的化学反应方程式___________ 。
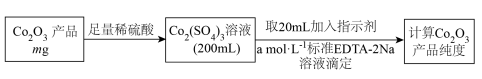
(6) 产品纯度测定方法如下:
产品纯度测定方法如下:
i.取 产品试样于
产品试样于 锥形瓶中,加入过量浓盐酸低温加热使试样完全溶解,得到含
锥形瓶中,加入过量浓盐酸低温加热使试样完全溶解,得到含 的溶液;
的溶液;
ii.加入 缓冲溶液,调节
缓冲溶液,调节 后再加入过量的
后再加入过量的 溶液,稀释至
溶液,稀释至 ;
;
iii.加入1~2滴二甲酚橙指示剂,用 标准溶液滴定至终点。
标准溶液滴定至终点。
已知 与
与 或
或 都能按物质的量
都能按物质的量 发生反应,产物均为无色配合物;二甲酚橙
发生反应,产物均为无色配合物;二甲酚橙 时显黄色)能与
时显黄色)能与 形成红色配合物。
形成红色配合物。
①到达滴定终点时的现象为___________ 。
②计算 产品试样中
产品试样中 的纯度还需要的实验数据有
的纯度还需要的实验数据有___________ 。

| 物质 | ||||||
(1)漫出步骤铜钴矿中的
(2)加入试剂
(3)对于过程
①加
②判断
(4)滤渣1成分为
(5)
(6)
i.取
ii.加入
iii.加入1~2滴二甲酚橙指示剂,用
已知
①到达滴定终点时的现象为
②计算
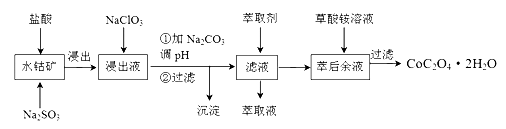
钴及其化合物广泛应用于磁性材料、电池材料及超硬材料等领域。一种制备草酸钴晶体(CoC2O4·2H2O)的工艺流程如下:
已知:①水钴矿主要成分为Co2O3、Co(OH)3,还含有少量Fe2O3、Al2O3、MnO等杂质。
②浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等。
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
(金属离子浓度以0.01mol·L-1计)
(1) 写出浸出过程中Co(OH)3发生反应的离子方程式:____________________ 。
(2) NaClO3的作用是_______________________ 。
(3) 加Na2CO3调pH的范围应该在_____ 之间。加入萃取剂的目的是____________ 。
(4) 在空气中加热5.49g草酸钴晶体(CoC2O4·2H2O)样品,受热过程中不同温度范围内分别得到一种固体物质,其质量如下表:
经测定,210~290℃过程中产生的气体只有CO2,此过程发生反应的化学方程式是____________________ 。[M(CoC2O4·2H2O=183g/mol]

已知:①水钴矿主要成分为Co2O3、Co(OH)3,还含有少量Fe2O3、Al2O3、MnO等杂质。
②浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等。
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
(金属离子浓度以0.01mol·L-1计)
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀pH | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1) 写出浸出过程中Co(OH)3发生反应的离子方程式:
(2) NaClO3的作用是
(3) 加Na2CO3调pH的范围应该在
(4) 在空气中加热5.49g草酸钴晶体(CoC2O4·2H2O)样品,受热过程中不同温度范围内分别得到一种固体物质,其质量如下表:
| 温度范围/℃ | 固体质量/g |
| 150~210 | 4.41 |
| 290~320 | 2.41 |
| 890~920 | 2.25 |
经测定,210~290℃过程中产生的气体只有CO2,此过程发生反应的化学方程式是
钴及其化合物广泛应用于磁性材料、电池材料及超硬材料等领域。一种制备草酸钴晶体(CoC2O4·2H2O)的工艺流程如下

已知:①水钴矿主要成分为Co2O3、Co(OH)3;还含有少量Fe2O3、Al2O3、MnO等杂质。
②浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、A13+等
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
(金属离子浓度以0.01mol·L-1计)
(1)写出浸出过程中Co(OH)3发生反应的离子方程式:______________________________ 。
(2)NaClO3的作用是_____________________________________________ 。
(3)加Na2CO3调pH的范围应该在_______________ 间,a加入萃取剂的目的是______________________________ 。
(4)在空气中加热5.49g草酸钻晶体(CoC2O4·2H2O)样品,受热过程中不同温度范围内分别得到一种固体物质,其质量如下表:
经测定,210~290℃过程中产生的气体只有CO2,此过程发生反应的化学方程式是_____________________________________________ 。[M( CoC2O4·2H2O)=183g/mol]

已知:①水钴矿主要成分为Co2O3、Co(OH)3;还含有少量Fe2O3、Al2O3、MnO等杂质。
②浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、A13+等
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
(金属离子浓度以0.01mol·L-1计)
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀pH | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(2)NaClO3的作用是
(3)加Na2CO3调pH的范围应该在
(4)在空气中加热5.49g草酸钻晶体(CoC2O4·2H2O)样品,受热过程中不同温度范围内分别得到一种固体物质,其质量如下表:
| 温度范围/℃ | 固体质量/g |
| 150~210 | 4.41 |
| 290~320 | 2.41 |
| 890~920 | 2.25 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


