解答题-实验探究题 适中0.65 引用1 组卷89
二氧化氯 是目前国际上公认的第四代高效、无毒的广谱消毒剂,是一种黄绿色气体,易溶于水,浓度过大时易发生分解爆炸。近来有学者发现使用复合法
是目前国际上公认的第四代高效、无毒的广谱消毒剂,是一种黄绿色气体,易溶于水,浓度过大时易发生分解爆炸。近来有学者发现使用复合法 发生器进行消毒的水中含有中等毒性的
发生器进行消毒的水中含有中等毒性的 ,进一步研究表明
,进一步研究表明 是由于
是由于 制备过程中未完全反应的
制备过程中未完全反应的 原料液进入水体引起的。实验室模拟复合法二氧化氯发生器反应工艺,探索反应温度对氯酸盐残留量的影响。实验原理:
原料液进入水体引起的。实验室模拟复合法二氧化氯发生器反应工艺,探索反应温度对氯酸盐残留量的影响。实验原理: 溶液(质量分数33.3%)与盐酸溶液(HCl质量分数
溶液(质量分数33.3%)与盐酸溶液(HCl质量分数 )经计量泵按1∶1比例进入反应残液一同混合形成二氧化氯复合消毒液模拟实验装置:
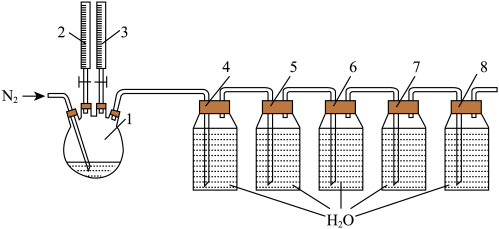
)经计量泵按1∶1比例进入反应残液一同混合形成二氧化氯复合消毒液模拟实验装置:
ⅰ.将 溶液与盐酸溶液按1∶1比例加入烧瓶1中,产生黄绿色气体后通入高纯
溶液与盐酸溶液按1∶1比例加入烧瓶1中,产生黄绿色气体后通入高纯 ;
;
ⅱ.反应90分钟,将5个口瓶内的液体和烧瓶内的反应残液一同倒入一个棕色广口瓶内,形成浓度均匀的复合二氧化氯消毒液;
ⅲ.分别在反应温度20℃、30℃、40℃、50℃、60℃、70℃、80℃、90℃重复上述过程;
ⅳ.测试复合二氧化氯消毒液中各组分浓度,收集整理数据。
(1)用来滴加反应液的仪器名称:______ ;为确保实验准确性,控制反应温度,发生装置选择的加热方式:______ 。
(2)烧瓶1中反应的化学方程式:____________ 。
(3)若已知所用盐酸的密度是 ,则盐酸的浓度是:
,则盐酸的浓度是:____________ 。
(4)通入高纯 的作用:
的作用:____________ 。
(5) 转化率及
转化率及 产率随温度的变化如图,据图可知,随反应温度的提高,氯酸盐残留量
产率随温度的变化如图,据图可知,随反应温度的提高,氯酸盐残留量______ (填“升高”或“降低”);改变反应时间,重复实验, 产率随温度变化趋势均如图所示,不考虑有副反应发生,试分析90℃时
产率随温度变化趋势均如图所示,不考虑有副反应发生,试分析90℃时 产率降低的可能原因
产率降低的可能原因____________ 。 等金属离子,还可杀菌消毒,下列与二氧化氯杀菌消毒原理一致的是
等金属离子,还可杀菌消毒,下列与二氧化氯杀菌消毒原理一致的是______ 。
a.臭氧浴足盆 b.酒精消毒 c.明矾净水
ⅰ.将
ⅱ.反应90分钟,将5个口瓶内的液体和烧瓶内的反应残液一同倒入一个棕色广口瓶内,形成浓度均匀的复合二氧化氯消毒液;
ⅲ.分别在反应温度20℃、30℃、40℃、50℃、60℃、70℃、80℃、90℃重复上述过程;
ⅳ.测试复合二氧化氯消毒液中各组分浓度,收集整理数据。
(1)用来滴加反应液的仪器名称:
(2)烧瓶1中反应的化学方程式:
(3)若已知所用盐酸的密度是
(4)通入高纯
(5)

a.臭氧浴足盆 b.酒精消毒 c.明矾净水
2024·四川成都·三模
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网