解答题-工业流程题 较难0.4 引用1 组卷133
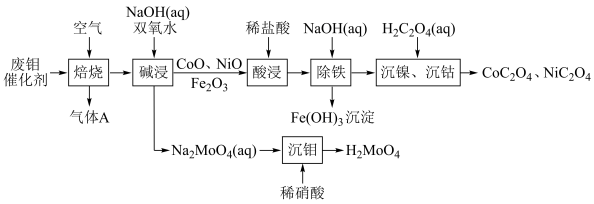
废钼催化剂中钼、钴、镍等有色金属作为二次资源可加以回收利用,一种从废钼催化剂(主要成分为 、
、 ,含少量CoO、CoS、NiO、
,含少量CoO、CoS、NiO、 等)中回收有色金属的一种工艺流程如图所示:
等)中回收有色金属的一种工艺流程如图所示: ;
;
②部分金属阳离子生成氢氧化物沉淀时溶液的pH如表所示:
回答下列问题:
(1)基态Mo原子的价电子排布式为 ,则Mo在元素周期表中的位置为
,则Mo在元素周期表中的位置为___________ 。
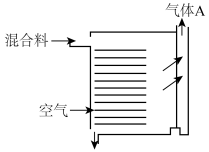
(2)“焙烧”时,采用“多层逆流焙烧”方法,即混合料与空气逆向而行,该方法的优点是___________ 。
(3)“焙烧”时 转化为
转化为 ,写出“碱浸”时
,写出“碱浸”时 参与反应的离子方程式:
参与反应的离子方程式:___________ 。
(4)“除铁”时,控制pH的范围为___________ 。
(5)“除铁”后所得滤液中 ,“沉镍”后所得滤液中
,“沉镍”后所得滤液中 ,则沉镍率=
,则沉镍率=___________ [沉镍率= ,计算过程中不考虑溶液体积变化,保留三位有效数字]。
,计算过程中不考虑溶液体积变化,保留三位有效数字]。
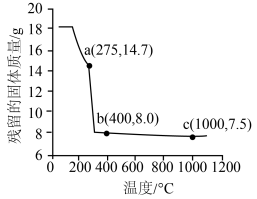
(6)在空气中加热18.3g ,其残留固体质量与温度的关系如图所示。图中,a、c两点对应固体的成分分别是
,其残留固体质量与温度的关系如图所示。图中,a、c两点对应固体的成分分别是___________ 、___________ (填化学式,其中c为Co的氧化物)。 表示,则晶体的密度为
表示,则晶体的密度为___________  。
。

②部分金属阳离子生成氢氧化物沉淀时溶液的pH如表所示:
| 金属阳离子 | |||
| 开始沉淀 | 7.0 | 2.3 | 7.1 |
| 沉淀完全 | 9.0 | 3.2 | 9.2 |
(1)基态Mo原子的价电子排布式为
(2)“焙烧”时,采用“多层逆流焙烧”方法,即混合料与空气逆向而行,该方法的优点是
(3)“焙烧”时
(4)“除铁”时,控制pH的范围为
(5)“除铁”后所得滤液中
(6)在空气中加热18.3g
2024·河北秦皇岛·二模
类题推荐
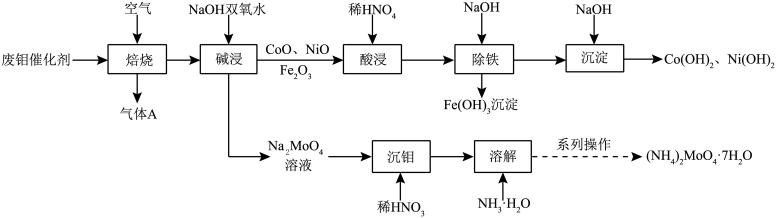
废钼催化剂中钼、钴、镍等有价金属作为二次资源可加以回收利用,一种从废钼催化剂(主要成分为MoO3、MoS2,含少量CoO、CoS、NiO、Fe2O3等)中回收有价金属的一种工艺流程如图。
已知:溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
(1)Ni在元素周期表中的位置为___________ , “焙烧”时产生的气体 A的主要成分为___________ 。
(2)“焙烧”时MoS2转化为MoO3,写出“碱浸”时MoO3参与反应的离子方程式___________ 。
(3)“碱浸”时 NaOH 加入量、浸出温度、浸出时间对钼浸出率的影响如图所示。
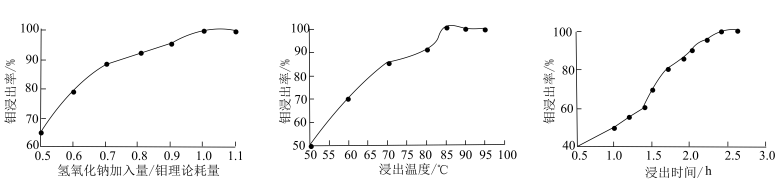
则应选择的适宜的生产工艺条件为___________ 、___________ 、___________ 。
(4)“除铁”时应调节溶液pH的范围为___________ ,“沉淀”时调节溶液 pH=9.0, 则此时溶液中 
_______ (pX=-lgX)。
(5)“系列操作”为___________ 、___________ 、过滤洗涤、干燥得到(NH4)2MoO4·7H2O晶体。
(6)50.00kg该废钼催化剂(含 Mo 元素质量分数为10.56%)通过该工艺最终得到15.05kg七水钼酸铵(相对分子质量为322)产品,则该工艺中七水钼酸铵的收率为___________ %(保留小数点后一位数字。收率= )。
)。

已知:溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 | Fe3+ | Co2+ | Ni2+ |
| 开始沉淀时 (c=0.01 mol·L-1) 的pH 沉淀完全时(c=1.0×10-5mol·L-1)的 pH | 2.2 3.2 | 6.4 9.0 | 7.2 8.7 |
回答下列问题:
(1)Ni在元素周期表中的位置为
(2)“焙烧”时MoS2转化为MoO3,写出“碱浸”时MoO3参与反应的离子方程式
(3)“碱浸”时 NaOH 加入量、浸出温度、浸出时间对钼浸出率的影响如图所示。

则应选择的适宜的生产工艺条件为
(4)“除铁”时应调节溶液pH的范围为
(5)“系列操作”为
(6)50.00kg该废钼催化剂(含 Mo 元素质量分数为10.56%)通过该工艺最终得到15.05kg七水钼酸铵(相对分子质量为322)产品,则该工艺中七水钼酸铵的收率为
废钼催化剂中钼、钴、镍等金属作为二次资源可加以回收利用,一种从废钼催化剂(主要成分为MoO3、MoS2,含少量CoO、CoS、NiO、Fe2O3等)中回收金属的一种工艺流程如图:
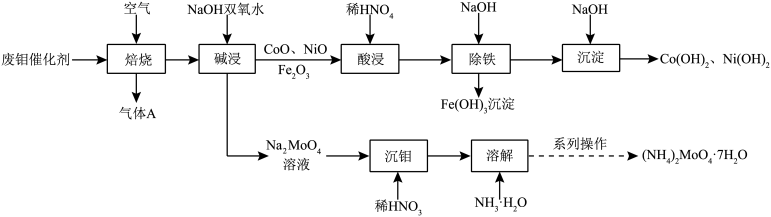
已知:溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)Ni2+价层电子轨道表示式为________ ,“焙烧”时产生的气体A的主要成分为________ 。
(2)“焙烧”时MoS2转化为MoO3,写出“碱浸”时MoO3参与反应的离子方程式_________ 。
(3)“除铁”时应调节溶液pH的范围为___________ ,“沉淀”时调节溶液pH=9.0,则此时溶液中[ =
=___________ (pX=-lgX)。
(4)“系列操作”为________ 、________ 、过滤、洗涤、干燥得到(NH4)2MoO4·7H2O晶体。
(5)50.00kg该废钼催化剂(含Mo元素质量分数为10.56%)通过该工艺最终得到15.05kg七水钼酸铵(相对分子质量为322)产品,则该工艺中七水钼酸铵的收率为___________ %(保留小数点后一位数字,收率= )。
)。

已知:溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 | Fe3+ | Co2+ | Ni2+ |
| 开始沉淀时(c=0.01mol·L-1)的pH 沉淀完全时(c=1.0×10-5mol·L-1)的pH | 2.2 3.2 | 6.4 9.0 | 7.2 8.7 |
(1)Ni2+价层电子轨道表示式为
(2)“焙烧”时MoS2转化为MoO3,写出“碱浸”时MoO3参与反应的离子方程式
(3)“除铁”时应调节溶液pH的范围为
(4)“系列操作”为
(5)50.00kg该废钼催化剂(含Mo元素质量分数为10.56%)通过该工艺最终得到15.05kg七水钼酸铵(相对分子质量为322)产品,则该工艺中七水钼酸铵的收率为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网