解答题-原理综合题 较易0.85 引用1 组卷134
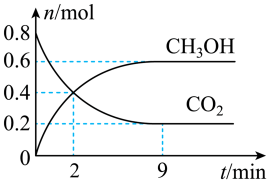
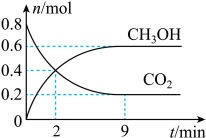
某温度下CO2加氢制甲醇的总反应为CO2(g)+3H2(g) CH3OH(g)+H2O(g)(该反应为放热反应),在固定容积为2.0 L的密闭容器中充入0.8 mol的CO2和2.4 mol的H2,测得CO2和CH3OH的物质的量随时间变化如图。请回答:
CH3OH(g)+H2O(g)(该反应为放热反应),在固定容积为2.0 L的密闭容器中充入0.8 mol的CO2和2.4 mol的H2,测得CO2和CH3OH的物质的量随时间变化如图。请回答:_______ (填“大于”“小于”或“等于”)生成物的化学键形成要放出的能量。
(2)2 min末时v正_______ (填“<”“>”或“=”)v逆。
(3)恒温恒容条件下,能说明反应已达平衡状态的是_______ 。
A.混合气体的密度保持不变
B.消耗1molCO2的同时消耗1molCH3OH
C.容器中CH3OH浓度与H2O浓度之比为1∶1
D.CO2(g)体积分数保持不变
E.v(H2) = 3v(CH3OH)
(4)该反应平衡时H2的转化率为_______ 。
(5)二氧化碳加氢制甲醇一般认为可通过两步反应来实现,物质变化与体系能量变化如题图所示。 CO(g)+H2O(g)。
CO(g)+H2O(g)。
②_______ (用化学方程式表示)。
总反应可表示为CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH
CH3OH(g)+H2O(g) ΔH_______ (填“>”或“<”)0。
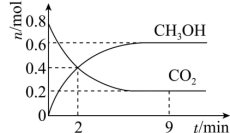
(2)2 min末时v正
(3)恒温恒容条件下,能说明反应已达平衡状态的是
A.混合气体的密度保持不变
B.消耗1molCO2的同时消耗1molCH3OH
C.容器中CH3OH浓度与H2O浓度之比为1∶1
D.CO2(g)体积分数保持不变
E.v(H2) = 3v(CH3OH)
(4)该反应平衡时H2的转化率为
(5)二氧化碳加氢制甲醇一般认为可通过两步反应来实现,物质变化与体系能量变化如题图所示。
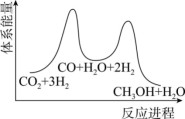
②
总反应可表示为CO2(g)+3H2(g)
23-24高一下·福建莆田·期中
类题推荐
蕴藏在海底的大量“可燃冰”,煤液化和气化形成的甲醇都是重要的能源。
(1) 。若1molCH4气体
。若1molCH4气体完全 反应时,吸收akJ热量,部分化学键的键能如下表。
①写出甲烷的结构式_______ 。
②C=O的键能为_______ kJ/mol(用含a、b、c、d的式子表示)。
(2)某温度下CO2加氢制甲醇的总反应为: ,该反应为放热反应,在固定容积为2.0L的密闭容器中充入0.8mol的CO2和2.4mol的H2,CO2和CH3OH的物质的量随时间变化如下图。
,该反应为放热反应,在固定容积为2.0L的密闭容器中充入0.8mol的CO2和2.4mol的H2,CO2和CH3OH的物质的量随时间变化如下图。
①下列说法正确的是_______ 。
A.反应物的化学键断裂要吸收的能量大于生成物的化学键形成要放出的能量
B.往容器中充入一定量的N2,反应速率不变
C.分离出CH3OH后,正反应速率不变,逆反应速率一直在减小
D.减小容器体积,反应速率加快
E.2min时混合气体的密度大于9min时混合气体的密度
②2min内CH3OH的反应速率为_______ ,2min末时V正_______ V逆(填“<”“>”或“=”)。
③恒温恒容条件下,能说明反应已达平衡状态的是_______ 。
A.CO2(g)体积分数保持不变
B.容器中气体压强保持不变
C.容器中CH3OH浓度与H2O浓度之比为1∶1
D.混合气体的密度保持不变
E.H2的生成速率是H2O生成速率的3倍
④该反应平衡时CO2的转化率为_______ 。(请写出计算过程)
(1)
| 化学键 | C—H | H—H | H—O |
| 键能kJ/mol | b | c | d |
②C=O的键能为
(2)某温度下CO2加氢制甲醇的总反应为:
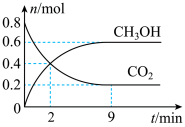
①下列说法正确的是
A.反应物的化学键断裂要吸收的能量大于生成物的化学键形成要放出的能量
B.往容器中充入一定量的N2,反应速率不变
C.分离出CH3OH后,正反应速率不变,逆反应速率一直在减小
D.减小容器体积,反应速率加快
E.2min时混合气体的密度大于9min时混合气体的密度
②2min内CH3OH的反应速率为
③恒温恒容条件下,能说明反应已达平衡状态的是
A.CO2(g)体积分数保持不变
B.容器中气体压强保持不变
C.容器中CH3OH浓度与H2O浓度之比为1∶1
D.混合气体的密度保持不变
E.H2的生成速率是H2O生成速率的3倍
④该反应平衡时CO2的转化率为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网