解答题-实验探究题 适中0.65 引用3 组卷396
苯氧乙酸是制备除草剂(2,4-D)的原料。某小组设计方案制备苯氧乙酸,制备原理:
步骤1:如图1装置(部分夹持及加热装置省略),在三颈瓶中加入3.8g氯乙酸和5mL水,开动搅拌,慢慢滴加饱和 溶液(约需8mL),至溶液pH为7~8.然后加入2.5g苯酚,再慢慢滴加35%的NaOH溶液至反应混合液pH为12。
溶液(约需8mL),至溶液pH为7~8.然后加入2.5g苯酚,再慢慢滴加35%的NaOH溶液至反应混合液pH为12。
步骤3:反应完毕后,将三口瓶移出水浴,趁热转入锥形瓶中,在搅拌下用浓盐酸酸化至pH为2~3。
步骤4:在冰浴中冷却,析出固体,待结晶完全后,抽滤(如图2所示),粗产物用冷水洗涤2~3次,在60~65℃干燥,产量约3.0g。
(1)图1仪器A名称是___________ ,进水口为___________ (填“a”或“b”)。
(2)步骤1中滴加试剂要“缓慢”,其原因是___________ ;能否用NaOH溶液替代 溶液?答:
溶液?答:___________ (填“能”或“不能”),理由是___________ 。
(3)本实验多次调节pH,其目的是___________ 。
(4)相对酒精灯直接加热,步骤2用沸水浴加热的优点是___________ 。步骤3“趁热”转移的目的是___________ 。
(5)步骤4抽滤的优点是___________ ;抽滤操作部分步骤如下:
①过滤完成后,先关闭抽气泵,然后再断开抽气泵和吸滤瓶之间的橡皮管。
②将准备好的液体缓慢地倒入布氏漏斗中。
③开启抽气泵,抽气以帮助滤纸紧贴在漏斗的内壁,防止液体泄漏。
④从漏斗中取出固体时,应小心地将漏斗从抽滤瓶上移除,并将漏斗管倒置,利用手的力量将固体和滤纸一同脱落到干净的表面上。
正确的先后操作顺序是___________ (填序号)。
(6)本实验产率最接近___________(填字母)。
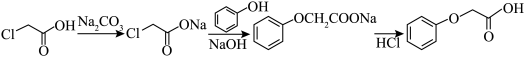
步骤1:如图1装置(部分夹持及加热装置省略),在三颈瓶中加入3.8g氯乙酸和5mL水,开动搅拌,慢慢滴加饱和
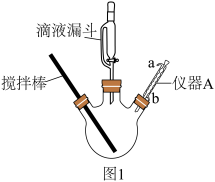
步骤3:反应完毕后,将三口瓶移出水浴,趁热转入锥形瓶中,在搅拌下用浓盐酸酸化至pH为2~3。
步骤4:在冰浴中冷却,析出固体,待结晶完全后,抽滤(如图2所示),粗产物用冷水洗涤2~3次,在60~65℃干燥,产量约3.0g。
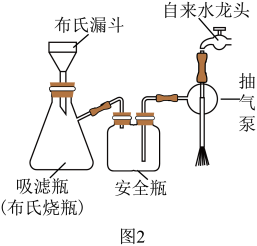
(1)图1仪器A名称是
(2)步骤1中滴加试剂要“缓慢”,其原因是
(3)本实验多次调节pH,其目的是
(4)相对酒精灯直接加热,步骤2用沸水浴加热的优点是
(5)步骤4抽滤的优点是
①过滤完成后,先关闭抽气泵,然后再断开抽气泵和吸滤瓶之间的橡皮管。
②将准备好的液体缓慢地倒入布氏漏斗中。
③开启抽气泵,抽气以帮助滤纸紧贴在漏斗的内壁,防止液体泄漏。
④从漏斗中取出固体时,应小心地将漏斗从抽滤瓶上移除,并将漏斗管倒置,利用手的力量将固体和滤纸一同脱落到干净的表面上。
正确的先后操作顺序是
(6)本实验产率最接近___________(填字母)。
| A.46% | B.58% | C.75% | D.81% |
2024·湖北·二模
类题推荐
苯氧乙酸为除草剂的中间体。制备苯氧乙酸的反应原理和装置(夹持仪器已省略)如图所示。相关物理数据如下表。 HOCH2COONa+NaCl+H2O
HOCH2COONa+NaCl+H2O
Ⅰ、将 3.8g氯乙酸和5mL水加入100mL的仪器X中,开启搅拌器,缓慢加入7mL饱和碳酸钠溶液至溶液 pH 为 7~8。
Ⅱ、加入2.35g 苯酚, 再滴加 35%氢氧化钠溶液至反应溶液pH为12,将反应物在沸水浴中加热 30min。
Ⅲ、反应过程中溶液pH下降,补充氢氧化钠使pH保持为12,在沸水浴中继续加热15min。
Ⅳ、反应结束,将溶液转入锥形瓶中,在搅拌下用浓盐酸酸化至pH为3~4。
Ⅴ、冰水浴中冷却析出晶体,抽滤,冷水洗涤产物3次,在60~65℃下干燥得到黄色产品,再加入活性炭,得到2.47g白色晶体。
请回答下列问题:
(1)仪器X的名称是___________ 。
(2)球形冷凝管中冷水由______ (填“a”或“b”) 口流进, 与直形冷凝管相比,其优点是________ 。
(3)步骤Ⅰ中用饱和碳酸钠溶液将pH调至7~8的原因:___________ 。
(4)写出反应③的化学方程式:___________ 。
(5)步骤Ⅳ用浓盐酸酸化至pH为3~4,其目的是___________ 。
(6)步骤Ⅴ中,抽滤装置如图所示,采用“抽滤”的优点是___________ 。
(7)步骤Ⅴ中加活性炭的目的是___________ 。
(8)该过程中苯氧乙酸的产率为___________ 。

| 相对分子质量 | 熔点/℃ | 沸点/℃ | 溶解性 | |
| 苯酚 | 94 | 43 | 181.75 | 易溶于热水,易溶于乙醇 |
| 苯氧乙酸 | 152 | 89~100 | 285 | 易溶于热水,不溶于冷水,溶于乙醇 |
| 氯乙酸 | 94.5 | 63 | 189 | 易溶于水, 溶于乙醇 |
| 羟基乙酸 | 76 | 79~80 | 分解 | 易溶于水, 易溶于乙醇 |

Ⅰ、将 3.8g氯乙酸和5mL水加入100mL的仪器X中,开启搅拌器,缓慢加入7mL饱和碳酸钠溶液至溶液 pH 为 7~8。
Ⅱ、加入2.35g 苯酚, 再滴加 35%氢氧化钠溶液至反应溶液pH为12,将反应物在沸水浴中加热 30min。
Ⅲ、反应过程中溶液pH下降,补充氢氧化钠使pH保持为12,在沸水浴中继续加热15min。
Ⅳ、反应结束,将溶液转入锥形瓶中,在搅拌下用浓盐酸酸化至pH为3~4。
Ⅴ、冰水浴中冷却析出晶体,抽滤,冷水洗涤产物3次,在60~65℃下干燥得到黄色产品,再加入活性炭,得到2.47g白色晶体。
请回答下列问题:
(1)仪器X的名称是
(2)球形冷凝管中冷水由
(3)步骤Ⅰ中用饱和碳酸钠溶液将pH调至7~8的原因:
(4)写出反应③的化学方程式:
(5)步骤Ⅳ用浓盐酸酸化至pH为3~4,其目的是
(6)步骤Ⅴ中,抽滤装置如图所示,采用“抽滤”的优点是
(7)步骤Ⅴ中加活性炭的目的是
(8)该过程中苯氧乙酸的产率为
对氯苯氧乙酸是一个常用的植物生长调节剂,俗称“防落素”,可以减少农作物或瓜果蔬菜的落花落果,有明显的增产作用。其实验原理为
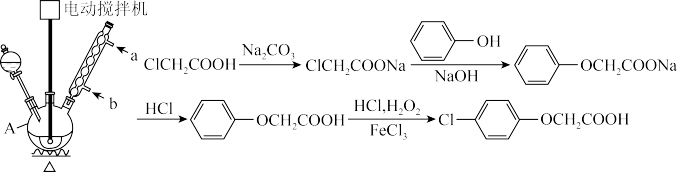
实验步骤:①在反应器中,加入3.8g氯乙酸和5mL水,开始搅拌,慢慢滴加饱和碳酸钠溶液,至溶液的pH为7〜8,然后加入2.5g苯酚,再慢慢滴加35%氢氧化钠溶液至 ;
;
②将反应器置于油浴中缓慢加热,维持此温度20min;
③移去油浴,用浓盐酸调 ,析出固体,抽滤,水洗2〜3次,再用乙醇溶液洗涤,得到粗产品;
,析出固体,抽滤,水洗2〜3次,再用乙醇溶液洗涤,得到粗产品;
④加入少量三氯化铁和10mL浓盐酸,升温至60〜70℃,滴加双氧水,反应20〜30min,升温使固体溶解,慢慢冷却,析出固体,抽滤,洗涤,重结晶。
完成下列问题:
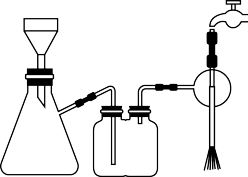
(1)装置中A的名称是___________ ,球形冷凝管的进水口是___________ (填“a”或“b”)。
(2)步骤②中采用油浴加热,用油浴加热的优点是___________ 。
(3)步骤③用乙醇溶液洗涤的目的是___________ 。
(4)步骤③和④均涉及抽滤,下列关于抽滤的说法中正确的是___________。
(5)步骤④中加入浓盐酸的目的是___________ ,有时需要将“粗产品用沸水溶解,冷却结晶,抽滤”的操作进行多次,其目的是___________ 。
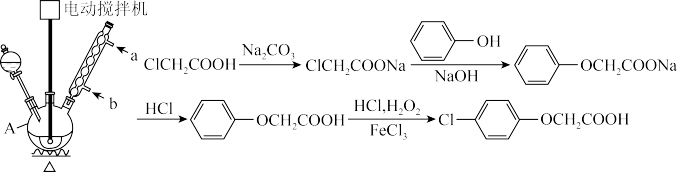
实验步骤:①在反应器中,加入3.8g氯乙酸和5mL水,开始搅拌,慢慢滴加饱和碳酸钠溶液,至溶液的pH为7〜8,然后加入2.5g苯酚,再慢慢滴加35%氢氧化钠溶液至
②将反应器置于油浴中缓慢加热,维持此温度20min;
③移去油浴,用浓盐酸调
④加入少量三氯化铁和10mL浓盐酸,升温至60〜70℃,滴加双氧水,反应20〜30min,升温使固体溶解,慢慢冷却,析出固体,抽滤,洗涤,重结晶。
完成下列问题:
(1)装置中A的名称是
(2)步骤②中采用油浴加热,用油浴加热的优点是
(3)步骤③用乙醇溶液洗涤的目的是
(4)步骤③和④均涉及抽滤,下列关于抽滤的说法中正确的是___________。

| A.抽滤的主要目的是得到较为干净的沉淀 |
| B.滤纸的直径应略小于漏斗内径,又能盖住全部小孔 |
| C.图中有一处出错 |
| D.抽滤结束,从吸滤瓶的支管口倒出滤液 |
1,6-己二酸是常用的化工原料,实验室利用图中的装置(夹持装置已省略),以环己醇和硝酸为原料制备1,6-己二酸。反应原理为:
 +2HNO3
+2HNO3
 +2NO2↑+2H2O
+2NO2↑+2H2O
 +6HNO3
+6HNO3 HOOC(CH2)4COOH+6O2↑+3H2O
HOOC(CH2)4COOH+6O2↑+3H2O

相关物质的物理性质见表:
实验步骤如下:
I.向三颈烧瓶中加入0.03gNH4VO3固体和18mL浓HNO3(略过量),向恒压滴液漏斗中加入6mL环己醇。
II.将三颈烧瓶放入水浴中,磁力搅拌并加热至50℃;移去水浴,打开恒压滴液漏斗活塞滴加5~6滴环己醇,观察到三颈烧瓶中产生红棕色气体时,开始慢慢加入余下的环己醇,调节滴加环己醇的速度,使三颈烧瓶内温度维持在50~60℃之间,直至环己醇全部滴加完毕。
III.将三颈烧瓶放入80~90℃水浴中加热10min,至几乎无红棕色气体导出为止。然后迅速将三颈烧瓶中混合液倒入100L烧杯中,冷却至室温后,有白色晶体析出,减压过滤,____,干燥,得到粗产品。
IV.1,6-己二酸粗产品的提纯。
(1)根据上述实验药品的用量,三颈烧瓶的最适宜规格为____ (填字母)。
(2)仪器A的名称为____ ,其作用是____ 。
(3)若步骤II中控制水浴温度不当,未滴加环己醇前就会观察到有红棕色气体生成,原因为____ 。滴加环己醇的过程中,若温度过高,可用冷水浴冷却维持50~60℃,说明该反应的△H____ (填“>”或“<”)0。
(4)实验中用到的减压过滤装置如图所示,下列操作不正确的是____ 。

(5)将步骤III补充完整:____ 。步骤IV提纯方法的名称为____ 。
(6)下列说法不正确的是____ 。
 +2HNO3
+2HNO3 +2NO2↑+2H2O
+2NO2↑+2H2O +6HNO3
+6HNO3
相关物质的物理性质见表:
| 物质 | 相对分子质量 | 密度/(g•mL-1) | 溶解性 |
| 环己醇 | 100 | 0.962 | 可溶于水、乙醇、乙醚 |
| 1,6-己二酸 | 146 | 1.360 | 微溶于冷水,易溶于乙醇 |
| NH4VO3 | 117 | 2.326 | 微溶于冷水,溶于热水 |
I.向三颈烧瓶中加入0.03gNH4VO3固体和18mL浓HNO3(略过量),向恒压滴液漏斗中加入6mL环己醇。
II.将三颈烧瓶放入水浴中,磁力搅拌并加热至50℃;移去水浴,打开恒压滴液漏斗活塞滴加5~6滴环己醇,观察到三颈烧瓶中产生红棕色气体时,开始慢慢加入余下的环己醇,调节滴加环己醇的速度,使三颈烧瓶内温度维持在50~60℃之间,直至环己醇全部滴加完毕。
III.将三颈烧瓶放入80~90℃水浴中加热10min,至几乎无红棕色气体导出为止。然后迅速将三颈烧瓶中混合液倒入100L烧杯中,冷却至室温后,有白色晶体析出,减压过滤,____,干燥,得到粗产品。
IV.1,6-己二酸粗产品的提纯。
(1)根据上述实验药品的用量,三颈烧瓶的最适宜规格为
| A.50mL | B.100mL | C.500mL | D.1000mL |
(3)若步骤II中控制水浴温度不当,未滴加环己醇前就会观察到有红棕色气体生成,原因为
(4)实验中用到的减压过滤装置如图所示,下列操作不正确的是

| A.选择比布氏漏斗内径略小又能将全部小孔盖住的滤纸 |
| B.放入滤纸后,直接用倾析法转移溶液和沉淀,再打开水龙头抽滤 |
| C.洗涤晶体时,先关闭水龙头,用蒸馏水缓慢淋洗,再打开水龙头抽滤 |
| D.抽滤完毕时,应先断开抽气泵和吸滤瓶之间的橡皮管,以防倒吸 |
(6)下列说法不正确的是
| A.反应完成后,倒反应液时要在通风橱中进行 |
| B.反应时,温度计水银球应置于三颈烧瓶中液面以下 |
| C.装置B中发生非氧化还原反应 |
| D.常用质谱法进行1,6-己二酸相对分子质量的测定 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


