解答题-结构与性质 适中0.65 引用1 组卷33
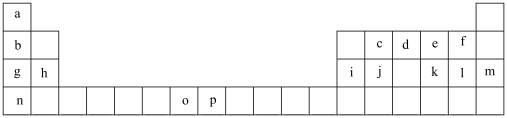
下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题。_______ (用元素符号表示),1和n的离子半径较大的是_______ (填离子符号)。
(2)h的单质在空气中燃烧发出耀眼的白光,从原子结构角度解释是涉及电子从能量较高的轨道跃迁到能量较低的轨道时,以光(子)的形式释放能量,以下现象与该原理一样的是_______ (填字母)。
A.燃放焰火 B.棱镜分出的光 C.霓虹灯射出五颜六色的光
(3)o、p两元素的部分电离能数据如下表所示。
比较两元素的 、
、 可知,气态
可知,气态 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难。对此,你认为原因可能是
再失去一个电子难。对此,你认为原因可能是_______ 。
(4)第三周期8种元素其中电负性最大的是_______ (填图中的序号)。
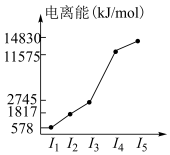
(5)表中所列的某主族元素的电离能情况如图所示,写出该元素的最高价氧化物对应的水化物与g的最高价氧化物对应的水化物反应的离子方程式:_______ 。
(2)h的单质在空气中燃烧发出耀眼的白光,从原子结构角度解释是涉及电子从能量较高的轨道跃迁到能量较低的轨道时,以光(子)的形式释放能量,以下现象与该原理一样的是
A.燃放焰火 B.棱镜分出的光 C.霓虹灯射出五颜六色的光
(3)o、p两元素的部分电离能数据如下表所示。
| 电离能/ | |||
| o | 717 | 1509 | 3248 |
| p | 759 | 1561 | 2957 |
(4)第三周期8种元素其中电负性最大的是
(5)表中所列的某主族元素的电离能情况如图所示,写出该元素的最高价氧化物对应的水化物与g的最高价氧化物对应的水化物反应的离子方程式:
23-24高二下·新疆阿克苏·阶段练习
类题推荐
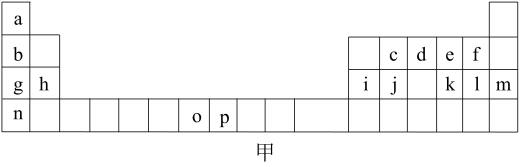
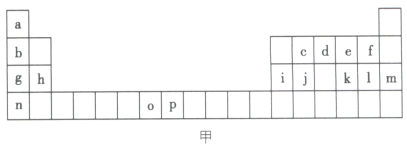
如图甲是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
试回答下列问题。
(1)元素p为26号元素,请写出其基态原子的电子排布式:_______ 。
(2)c、d、e、f四种元素的第一电高能由大到小的顺序为_______ (填元素符号)。
(3)h的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:_______ 。
(4)o、p两元素的部分电离能数据如表:
比较两元素的 、
、 可知,气态基态
可知,气态基态 再失去一个电子比基态气态
再失去一个电子比基态气态 再失去一个电子难。对此,你的解释是
再失去一个电子难。对此,你的解释是_______ 。
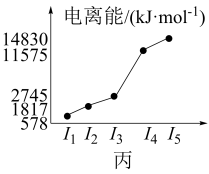
(5)图甲中的某主族元素的电离能情况如图丙所示,则该元素的单质与氢氧化钠溶液反应的化学方程式为_______ 。

试回答下列问题。
(1)元素p为26号元素,请写出其基态原子的电子排布式:
(2)c、d、e、f四种元素的第一电高能由大到小的顺序为
(3)h的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:
(4)o、p两元素的部分电离能数据如表:
| 元素 | o | p | |
| 电高能 | 717 | 759 | |
| 1509 | 1561 | ||
| 3248 | 2957 |
(5)图甲中的某主族元素的电离能情况如图丙所示,则该元素的单质与氢氧化钠溶液反应的化学方程式为

如图甲是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
试回答下列问题。
(1)元素p为26号元素,请写出其基态原子的电子排布式:___________ 。
(2)c、d、e、f四种元素的第一电离能由大到小的顺序为___________ (填元素符号)。
(3)h的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:___________ 。
(4)o、p两元素的部分电离能数据如表:
比较两元素的 、
、 可知,气态基态
可知,气态基态 再失去一个电子比基态气态
再失去一个电子比基态气态 再失去一个电子难。对此,你的解释是
再失去一个电子难。对此,你的解释是___________ 。
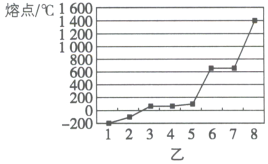
(5)第三周期8种元素按单质熔点高低的顺序排列如图乙所示,其中电负性最大的是___________ (填图中的序号)。
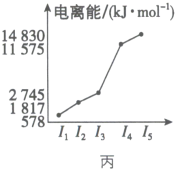
(6)图甲中的某主族元素的电离能情况如图丙所示,则该元素是___________ (填元素符号)。

试回答下列问题。
(1)元素p为26号元素,请写出其基态原子的电子排布式:
(2)c、d、e、f四种元素的第一电离能由大到小的顺序为
(3)h的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:
(4)o、p两元素的部分电离能数据如表:
| 元素 | o | p | |
| 717 | 759 | ||
| 1509 | 1561 | ||
| 3248 | 2957 | ||
比较两元素的
(5)第三周期8种元素按单质熔点高低的顺序排列如图乙所示,其中电负性最大的是

(6)图甲中的某主族元素的电离能情况如图丙所示,则该元素是

如图甲是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
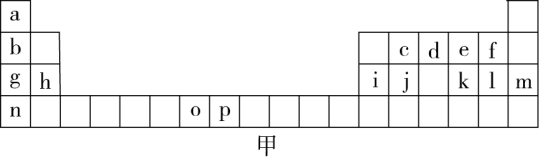
试回答下列问题。
(1)元素p为26号元素,请写出其基态原子的电子排布式:___________ 。
(2)c、d、e、f四种元素的第一电离能由大到小的顺序为___________ (填元素符号)。
(3)h的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:____________ 。
(4)o、p两元素的部分电离能数据如表:
比较两元素的I2、I3可知,气态基态o2+再失去一个电子比基态气态p2+再失去一个电子难。对此,你的解释是___________ 。
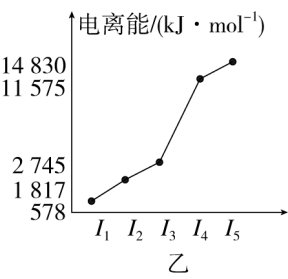
(5)图甲中的某主族元素的电离能情况如图乙所示,则该元素是___________ (填元素符号)。

试回答下列问题。
(1)元素p为26号元素,请写出其基态原子的电子排布式:
(2)c、d、e、f四种元素的第一电离能由大到小的顺序为
(3)h的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:
(4)o、p两元素的部分电离能数据如表:
| 元素 | o | p | |
| I1 | 717 | 759 | |
| I2 | 1 509 | 1 561 | |
| I3 | 3 248 | 2 957 | |
(5)图甲中的某主族元素的电离能情况如图乙所示,则该元素是

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


