解答题-原理综合题 较难0.4 引用3 组卷526
深入研究碳、氮元素的物质转化有着重要的实际意义,汽车尾气净化装置中CO和NO发生如下反应:
ⅰ.
 ,
,
ⅱ.
 ,
,
ⅲ.
 ,
,
回答下列问题:
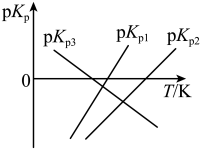
(1)上述反应的 的线性关系如图所示。
的线性关系如图所示。
______ (填“>”或“<”)0,反应 的
的
______ (用 、
、 表示)。
表示)。 ,初始总压强为
,初始总压强为 。反应
。反应 的
的 ,
, ,
, 、
、 分别为正、逆反应速率常数。充分反应达平衡时压强为
分别为正、逆反应速率常数。充分反应达平衡时压强为 (该温度下忽略反应ⅲ),
(该温度下忽略反应ⅲ), 的物质的量为1.25mol,则
的物质的量为1.25mol,则
______ 。
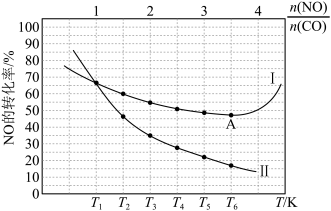
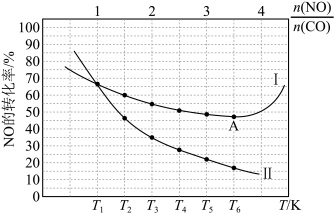
(3)CO和NO发生上述反应,在不同条件下达到平衡时,在 时NO的转化率与
时NO的转化率与 的变化曲线及
的变化曲线及 时NO的转化率与T的变化曲线如图所示。将2mol
时NO的转化率与T的变化曲线如图所示。将2mol  和2mol
和2mol  充入1L恒容密闭容器,初始总压强为100kPa,发生上述反应。
充入1L恒容密闭容器,初始总压强为100kPa,发生上述反应。 时NO的转化率与T的变化曲线为
时NO的转化率与T的变化曲线为______ 曲线(填“Ⅰ”或“Ⅱ”),A点后NO的平衡转化率增大的原因是______ 。
②已知:反应iii的平衡常数 。
。 条件下反应达平衡时,
条件下反应达平衡时, ,则平衡时
,则平衡时 的物质的量
的物质的量
______ mol,反应ii的压强平衡常数
______ (保留两位有效数字)。
ⅰ.
ⅱ.
ⅲ.
回答下列问题:
(1)上述反应的
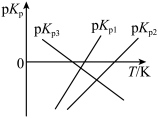
(3)CO和NO发生上述反应,在不同条件下达到平衡时,在
②已知:反应iii的平衡常数
2024·山东潍坊·二模
类题推荐
研究CO2资源的综合利用,对实现“碳达峰”和“碳中和”有重要意义。
(1)已知:
Ⅰ.

Ⅱ.

Ⅲ.

①
_______ 
②一定条件下,向体积为2L的恒容密闭容器中通入1molCO2和3molH2,发生上述反应,达到平衡时,容器中CH3OH(g)的物质的量为0.5mol;CO的物质的量为0.3mol;此时H2O(g)的浓度为_______ mol·L-1。
(2)CO2在Cu—ZnO催化下,同时发生反应Ⅰ、Ⅲ;此方法是解决温室效应和能源短缺问题的重要手段。保持温度T时,在容积不变的密闭容器中,充入一定量的CO2及H2;起始及达到平衡时(t min时恰好达到平衡);容器内各气体物质的量及总压强如下表:
若反应Ⅰ、Ⅲ均达到平衡时,p0=1.4p;则表中n=_______ ;0~t min内,CO2的分压变化率为_______ kPa·min⁻¹;反应Ⅰ的平衡常数Kp=_______ (kPa)-2(用含p的式子表示)。
(3)CO2催化加氢制甲烷涉及的反应主要有:
主反应:

副反应:

若将CO2和H2按体积比为1∶4混合(n总=5mol);匀速通入装有催化剂的反应容器中,发生反应(包括主反应和副反应)。反应相同时间,CO2转化率、CH4和CO选择性随温度变化的曲线分别如图所示。
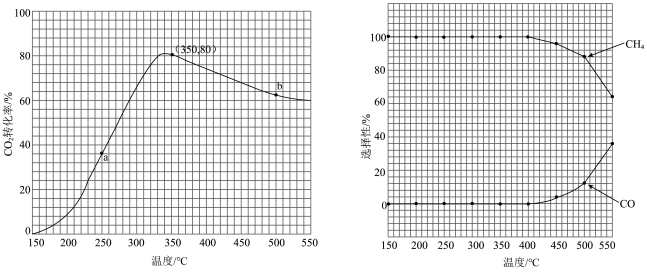
①a点的正反应速率和逆反应速率的大小关系为v正(a)_______ (填“>”、“=”或“<”)v逆(a)。
②催化剂在较低温度时主要选择_______ (填“主反应”或“副反应”)。
③350~400℃;CO2转化率呈现减小的变化趋势,其原因是_______ 。
(1)已知:
Ⅰ.
Ⅱ.
Ⅲ.
①
②一定条件下,向体积为2L的恒容密闭容器中通入1molCO2和3molH2,发生上述反应,达到平衡时,容器中CH3OH(g)的物质的量为0.5mol;CO的物质的量为0.3mol;此时H2O(g)的浓度为
(2)CO2在Cu—ZnO催化下,同时发生反应Ⅰ、Ⅲ;此方法是解决温室效应和能源短缺问题的重要手段。保持温度T时,在容积不变的密闭容器中,充入一定量的CO2及H2;起始及达到平衡时(t min时恰好达到平衡);容器内各气体物质的量及总压强如下表:
| 物质的量/mol | 总压强/kPa | |||||
| CO2 | H2 | CH3OH(g) | CO | H2O(g) | ||
| 起始 | 0.5 | 0.9 | 0 | 0 | 0 | p0 |
| 平衡 | n | 0.3 | p | |||
(3)CO2催化加氢制甲烷涉及的反应主要有:
主反应:
副反应:
若将CO2和H2按体积比为1∶4混合(n总=5mol);匀速通入装有催化剂的反应容器中,发生反应(包括主反应和副反应)。反应相同时间,CO2转化率、CH4和CO选择性随温度变化的曲线分别如图所示。

①a点的正反应速率和逆反应速率的大小关系为v正(a)
②催化剂在较低温度时主要选择
③350~400℃;CO2转化率呈现减小的变化趋势,其原因是
研究 资源的综合利用,对实现“碳达峰”和“碳中和”有重要意义。已知:
资源的综合利用,对实现“碳达峰”和“碳中和”有重要意义。已知:
I.
II.
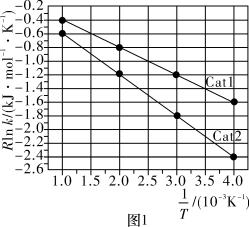
(1)一定条件下,速率常数与活化能、温度的关系式为 (R、C为常数,k为速率常数,
(R、C为常数,k为速率常数, 为活化能,T为温度)。一定温度下,反应Ⅰ的速率常数在不同催化剂(Cat1、Cat2)作用下,与温度的关系如图1所示。
为活化能,T为温度)。一定温度下,反应Ⅰ的速率常数在不同催化剂(Cat1、Cat2)作用下,与温度的关系如图1所示。
在Cat2作用下,该反应的活化能 为
为___________  ;催化效果更好的是
;催化效果更好的是___________ (填“Cat1”或“Cat2”)。
(2) 在
在 催化下,同时发生反应I、II;此方法是解决温室效应和能源短缺问题的重要手段。保持温度T时,在容积不变的密闭容器中,充入一定量的
催化下,同时发生反应I、II;此方法是解决温室效应和能源短缺问题的重要手段。保持温度T时,在容积不变的密闭容器中,充入一定量的 及
及 ;起始及达到平衡时(tmin时恰好达到平衡),容器内各气体物质的量及总压强如下表:
;起始及达到平衡时(tmin时恰好达到平衡),容器内各气体物质的量及总压强如下表:
若反应I、II均达到平衡时, ;则表中
;则表中
___________ ; 内,
内, 的分压变化率为
的分压变化率为___________  ;反应I的平衡常数
;反应I的平衡常数
___________  。
。
(3) 催化加氢制甲烷涉及的反应主要有:
催化加氢制甲烷涉及的反应主要有:
主反应:

副反应:

若将 和
和 按体积比为
按体积比为 混合(
混合( ),匀速通入装有催化剂的反应容器中,发生上述反应(包括主反应和副反应)。反应相同时间,
),匀速通入装有催化剂的反应容器中,发生上述反应(包括主反应和副反应)。反应相同时间, 转化率、
转化率、 和CO选择性随温度变化的曲线分别如图所示。
和CO选择性随温度变化的曲线分别如图所示。
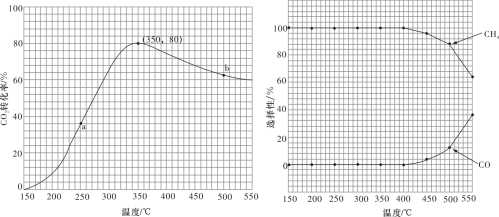
①a点的正反应速率和逆反应速率的大小关系为
___________ (填“>”“=”或“<”) 。
。
②催化剂在较低温度时主要选择___________ (填“主反应”或“副反应”)。
③350~400℃时; 转化率呈现减小的变化趋势,其原因是
转化率呈现减小的变化趋势,其原因是___________ 。
I.
II.
(1)一定条件下,速率常数与活化能、温度的关系式为
在Cat2作用下,该反应的活化能

(2)
| 物质的量/mol | 总压强/kPa | |||||
| CO | ||||||
| 起始 | 0.5 | 0.9 | 0 | 0 | 0 | |
| 平衡 | n | 0.3 | p | |||
(3)
主反应:
副反应:
若将

①a点的正反应速率和逆反应速率的大小关系为
②催化剂在较低温度时主要选择
③350~400℃时;
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网