解答题-原理综合题 较难0.4 引用1 组卷142
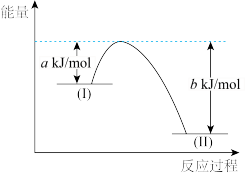
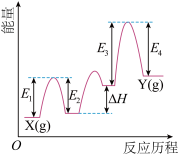
(Ⅰ)铬及其化合物在催化、金属防腐等方面具有重要应用。 催化丙烷脱氢过程中,部分反应历程如图,
催化丙烷脱氢过程中,部分反应历程如图, 过程的焓变为
过程的焓变为___ (列式表示)。
(2)该反应
_______ 0(填“>”或“=”或“<”)。
(Ⅱ)2022年11月29日23时08分,我国在酒泉卫星发射中心使用长征二号F遥十五火箭,成功将神舟十五号载人飞船发射升空,是空间站建造阶段最后一次载人飞行任务。
(3)火箭发射时可以用肼( ,液态)作燃料,
,液态)作燃料, 作氧化剂,二者反应生成
作氧化剂,二者反应生成 和水蒸气。已知:①
和水蒸气。已知:①
 kJ/mol②
kJ/mol②
 kJ/mol请写出
kJ/mol请写出 与
与 反应的热化学方程式
反应的热化学方程式_______ 。③
 ,
, 与
与 进行大小比较:
进行大小比较:
_______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(4)二甲醚( )是一种新型能源,被誉为“21世纪的清洁燃料”。用CO和
)是一种新型能源,被誉为“21世纪的清洁燃料”。用CO和 合成二甲醚的反应为:
合成二甲醚的反应为:
 kJ/mol。
kJ/mol。
①改变下列“量”,一定会引起 发生变化的是
发生变化的是_______ (填代号)。
a.化学计量数 b.反应物浓度 c.催化剂
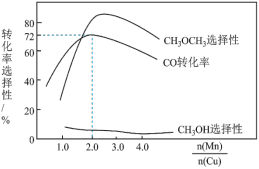
②采用新型催化剂(主要成分是Cu-Mn的合金)制备二甲醚。催化剂中 对合成二甲醚的影响情况如下图所示。当
对合成二甲醚的影响情况如下图所示。当 时,二甲醚的选择性(选择性
时,二甲醚的选择性(选择性 )为85.8%,此时二甲醚的产率为
)为85.8%,此时二甲醚的产率为_______ 。(保留3位有效数字)
 kJ·mol
kJ·mol
反应III:
 kJ·mol
kJ·mol
在反应Ⅱ中,若标准状况下有33.6 L 气体与水蒸气完全反应生成液态硫酸和固态硫单质,则放出的热量为
气体与水蒸气完全反应生成液态硫酸和固态硫单质,则放出的热量为______ kJ。
(2)该反应
(Ⅱ)2022年11月29日23时08分,我国在酒泉卫星发射中心使用长征二号F遥十五火箭,成功将神舟十五号载人飞船发射升空,是空间站建造阶段最后一次载人飞行任务。
(3)火箭发射时可以用肼(
(4)二甲醚(
①改变下列“量”,一定会引起
a.化学计量数 b.反应物浓度 c.催化剂
②采用新型催化剂(主要成分是Cu-Mn的合金)制备二甲醚。催化剂中
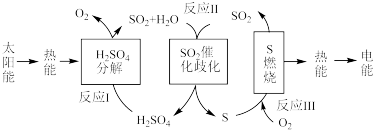
反应III:
在反应Ⅱ中,若标准状况下有33.6 L
23-24高一下·湖北武汉·阶段练习
类题推荐
二甲醚(CH3OCH3)是一种新型能源,被誉为“21世纪的清洁燃料”。
(1)用CO和H2合成二甲醚的反应为:3H2(g)+3CO(g) CH3OCH3(g)+CO2(g)△H。
CH3OCH3(g)+CO2(g)△H。
几种物质的相对能量如下:
△H=______ kJ·mol。改变下列“量”,一定会引起△H发生变化的是_____ (填代号)。
A.温度B.反应物浓度C.催化剂D.化学计量数
(2)有利于提高反应中CH3OCH3产率的条件为_______ (填标号)。
A.高温低压B.低温高压C.高温高压D.低温低压
(3)采用新型催化剂(主要成分是Cu—Mn的合金)制备二甲醚。催化剂中n(Mn)/n(Cu)对合成二甲醚的影响情况如下图所示。
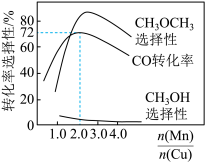
当n(Mn)/n(Cu)=2时,二甲醚的选择性( )为85.8%,此时二甲醚的产率为
)为85.8%,此时二甲醚的产率为_________ 。
(4)用二甲醚燃料电池电解法可将酸性含铬废水(主要含有Cr2O72-)转化为Cr3+。原理如下图:
①燃料电池中的负极是______ (填“M”或“N”)电极。电解池阴极的电极反应式为______________________________ 。
②消耗6.9g二甲醚时可处理Cr的含量为26.0g·L-1的废水1L,该套装置的能量利用率为___________ 。(保留3位有效数字)
(1)用CO和H2合成二甲醚的反应为:3H2(g)+3CO(g)
几种物质的相对能量如下:
物质 | H2(g) | CO(g) | CO2 (g) | CH3OCH3(g) |
相对能量/(kJ·mol-1) | 285.8 | 283 | 0 | 1453.0 |
A.温度B.反应物浓度C.催化剂D.化学计量数
(2)有利于提高反应中CH3OCH3产率的条件为
A.高温低压B.低温高压C.高温高压D.低温低压
(3)采用新型催化剂(主要成分是Cu—Mn的合金)制备二甲醚。催化剂中n(Mn)/n(Cu)对合成二甲醚的影响情况如下图所示。

当n(Mn)/n(Cu)=2时,二甲醚的选择性(
(4)用二甲醚燃料电池电解法可将酸性含铬废水(主要含有Cr2O72-)转化为Cr3+。原理如下图:
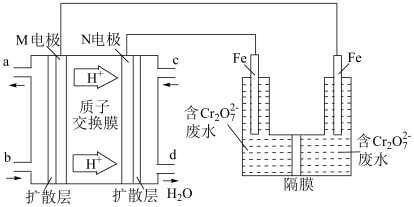
①燃料电池中的负极是
②消耗6.9g二甲醚时可处理Cr的含量为26.0g·L-1的废水1L,该套装置的能量利用率为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网