解答题-实验探究题 适中0.65 引用2 组卷310
苯胺是一种重要的精细化工原料,在染料、医药等行业中具有广泛的应用。
(1)实验室以苯为原料制取苯胺,其反应原理如下:
第一步:_________________ ;
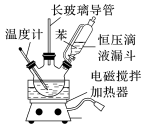
实验步骤:实验室采用如图所示装置制取硝基苯,恒压滴液漏斗中装有一定量的苯,三颈烧瓶中装有一定比例的浓硫酸和浓硝酸混合物。____________ (填字母)。
A. 配制混酸时,将浓硝酸沿杯壁缓缓加入浓硫酸中,并不断搅拌、冷却
B. 浓硫酸可以降低该反应的活化能
C. 温度控制在50~60 ℃原因之一是减少副反应的发生
D. 制得的粗硝基苯可以先用乙醇萃取,分液后再洗涤
②制备硝基苯时使用了恒压滴液漏斗,其作用是________________ ;
③粗硝基苯中有少量浓硫酸、浓硝酸,可选用的除杂试剂是_______________ ;
(3)制取苯胺
步骤2:先向三颈烧瓶中加入沸石及硝基苯,再取下恒压滴液漏斗,换上温度计;
步骤3:打开活塞K,通入H2一段时间;
步骤4:利用油浴加热;
步骤5:反应结束后,关闭活塞K,向三颈烧瓶中加入生石灰;
步骤6:调整好温度计的位置,继续加热,收集182~186 ℃馏分,得到较纯苯胺。
回答下列问题:
①步骤4中油浴加热的优点是___________ ;
②步骤5中加入生石灰的作用是____________ ;
③步骤6中,仪器A的名称是______________ ,冷凝水的流向为____ →____ (填字母);
④若实验中硝基苯用量为10 mL,最后得到苯胺5.6 g,苯胺的产率为_________ (精确到0.1%)。
物质 | 相对分子质量 | 沸点/℃ | 密度/(g·mL-1) | 溶解性 |
硝基苯 | 123 | 210.9 | 1.23 | 不溶于水,易溶于乙醇、乙醚 |
苯胺 | 93 | 184.4 | 1.02 | 微溶于水,易溶于乙醇、乙醚;还原性强、易被氧化 |
第一步:
第二步: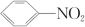 + 3H2
+ 3H2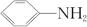 + 2H2O
+ 2H2O
实验步骤:实验室采用如图所示装置制取硝基苯,恒压滴液漏斗中装有一定量的苯,三颈烧瓶中装有一定比例的浓硫酸和浓硝酸混合物。
A. 配制混酸时,将浓硝酸沿杯壁缓缓加入浓硫酸中,并不断搅拌、冷却
B. 浓硫酸可以降低该反应的活化能
C. 温度控制在50~60 ℃原因之一是减少副反应的发生
D. 制得的粗硝基苯可以先用乙醇萃取,分液后再洗涤
②制备硝基苯时使用了恒压滴液漏斗,其作用是
③粗硝基苯中有少量浓硫酸、浓硝酸,可选用的除杂试剂是
(3)制取苯胺
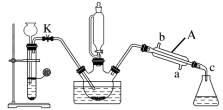
步骤2:先向三颈烧瓶中加入沸石及硝基苯,再取下恒压滴液漏斗,换上温度计;
步骤3:打开活塞K,通入H2一段时间;
步骤4:利用油浴加热;
步骤5:反应结束后,关闭活塞K,向三颈烧瓶中加入生石灰;
步骤6:调整好温度计的位置,继续加热,收集182~186 ℃馏分,得到较纯苯胺。
回答下列问题:
①步骤4中油浴加热的优点是
②步骤5中加入生石灰的作用是
③步骤6中,仪器A的名称是
④若实验中硝基苯用量为10 mL,最后得到苯胺5.6 g,苯胺的产率为
23-24高二下·四川绵阳·期中
类题推荐
苯胺是一种重要精细化工原料,在染料、医药等行业中具有广泛的应用。实验室以苯为原料制取苯胺,其原理简示如下:
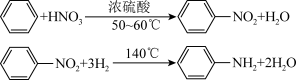
实验步骤:
I.制取硝基苯
实验室采用如图所示装置制取硝基苯,A中装有一定量的苯,三颈烧瓶装有一定比例的浓硫酸和浓硝酸混合物。请回答下列问题:

(1)仪器A的名称是___________ 。
(2)配制浓硫酸和浓硝酸的混合物时,应将___________ 逐滴加入到___________ 中,并及时搅拌和冷却。
(3)实验装置中长玻璃导管的作用是___________ 。
(4)粗硝基苯用5% NaOH溶液洗涤的目的是___________ 。
II.制取苯胺
①组装好实验装置(如图,夹持仪器已略去),并检查气密性。②先向三颈烧瓶中加入沸石及硝基苯,再取下恒压分液漏斗,换上温度计。③打开活塞K,通入H2一段时间。④利用油浴加热,使反应液温度维持在140℃进行反应。⑤反应结束后,关闭活塞K,向三颈烧瓶中加入生石灰。⑥调整好温度计的位置,继续加热,收集182~186℃馏分,得到较纯苯胺。

回答下列问题:
(5)操作①中加入沸石的作用___________ ,冷凝装置中的冷凝水应该从___________ (填“a”或者“b”)口进入。
(6)若实验中步骤③和④的顺序颠倒,则实验中可能产生的不良后果是___________ 。
(7)蒸馏前,步骤⑤中加入生石灰的作用是___________ 。
(8)若实验中硝基苯用量为5 mL,最后得到苯胺2.79 g,苯胺的产率为___________ 。

| 物质 | 沸点/°C | 密度/(g*cm3) | 部分性质 |
| 苯 | 80 | 0.88 | 无色油状液体,难溶于水 |
| 硝基苯 | 210.9 | 1.23 | 无色或淡黄色油状液体,不溶于水,易溶于乙醇、乙醚 |
| 苯胺 | 184.4. | 1.02 | 无色油状液体,微溶于水,易溶于乙醇、乙醚:还原性强,易被氧化 |
I.制取硝基苯
实验室采用如图所示装置制取硝基苯,A中装有一定量的苯,三颈烧瓶装有一定比例的浓硫酸和浓硝酸混合物。请回答下列问题:

(1)仪器A的名称是
(2)配制浓硫酸和浓硝酸的混合物时,应将
(3)实验装置中长玻璃导管的作用是
(4)粗硝基苯用5% NaOH溶液洗涤的目的是
II.制取苯胺
①组装好实验装置(如图,夹持仪器已略去),并检查气密性。②先向三颈烧瓶中加入沸石及硝基苯,再取下恒压分液漏斗,换上温度计。③打开活塞K,通入H2一段时间。④利用油浴加热,使反应液温度维持在140℃进行反应。⑤反应结束后,关闭活塞K,向三颈烧瓶中加入生石灰。⑥调整好温度计的位置,继续加热,收集182~186℃馏分,得到较纯苯胺。

回答下列问题:
(5)操作①中加入沸石的作用
(6)若实验中步骤③和④的顺序颠倒,则实验中可能产生的不良后果是
(7)蒸馏前,步骤⑤中加入生石灰的作用是
(8)若实验中硝基苯用量为5 mL,最后得到苯胺2.79 g,苯胺的产率为
苯胺是最重要的胺类物质之一,其应用广泛。某实验小组以苯为原料制取苯胺,方法如下:
I.制取硝基苯
实验步骤:实验室采用下图装置X制取硝基苯,仪器B中装有定量的苯,仪器A中装有一定比例的浓硫酸和浓硝酸混合物(略去加热装置)。
实验步骤:
①按上图组装实验仪器,检查装置气密性;
②先向三颈烧瓶中加入少量碎瓷片及10.0mL硝基苯,再取下恒压滴液漏斗,换上温度计;
③打开活塞K;
④用油浴加热,使反应液温度维持在140℃;
⑤反应结束后,关闭活塞K,向三颈烧瓶中加入生石灰;
⑥调整好温度计的位置,继续加热,收集185℃馏分,得到较纯苯胺。
已知部分有机物的一些数据如下表:
请回答下列问题:
(1)装置X中仪器C的名称是___________ ,其作用是___________ 。
(2)请写出该实验制取硝基苯的化学方程式:___________ 。
(3)制得的粗硝基苯不纯,用 溶液洗涤可除去
溶液洗涤可除去___________ 。
(4)装置Y有一个明显的缺点是___________ 。
(5)步骤②中温度计水银球的位置位于___________ (填序号,下同),步骤⑥中位于___________ 。
A.烧瓶内溶液液面以下 B.贴近烧瓶内液面处 C.三颈烧瓶出气口附近
(6)若实验中步骤③和④的顺序颠倒,则实验中可能产生的不良后果是___________ 。
(7)实验结束得到7.44g产物,则苯胺的产率为___________ 。
I.制取硝基苯
实验步骤:实验室采用下图装置X制取硝基苯,仪器B中装有定量的苯,仪器A中装有一定比例的浓硫酸和浓硝酸混合物(略去加热装置)。
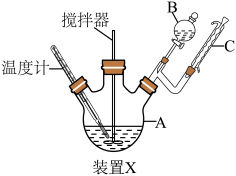
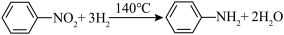

实验步骤:
①按上图组装实验仪器,检查装置气密性;
②先向三颈烧瓶中加入少量碎瓷片及10.0mL硝基苯,再取下恒压滴液漏斗,换上温度计;
③打开活塞K;
④用油浴加热,使反应液温度维持在140℃;
⑤反应结束后,关闭活塞K,向三颈烧瓶中加入生石灰;
⑥调整好温度计的位置,继续加热,收集185℃馏分,得到较纯苯胺。
已知部分有机物的一些数据如下表:
| 名称 | 相对分子质量 | 密度( | 沸点(℃) |
| 硝基苯 | 123 | 1.23 | 210.8 |
| 苯胺 | 93 | 1.02 | 184.4 |
(1)装置X中仪器C的名称是
(2)请写出该实验制取硝基苯的化学方程式:
(3)制得的粗硝基苯不纯,用
(4)装置Y有一个明显的缺点是
(5)步骤②中温度计水银球的位置位于
A.烧瓶内溶液液面以下 B.贴近烧瓶内液面处 C.三颈烧瓶出气口附近
(6)若实验中步骤③和④的顺序颠倒,则实验中可能产生的不良后果是
(7)实验结束得到7.44g产物,则苯胺的产率为
苯胺(有机碱,常温下为无色油状液体,易被氧化)在染料、医药、农药、香料等领域有广泛的应用。实验室以硝基苯为原料制备苯胺,反应原理如下:
实验步骤为:
①组装好实验装置(如图,部分夹持仪器已略去),并检查装置气密性。
②向三颈烧瓶中依次加入沸石及10mL硝基苯。
③打开活塞K,先通入H2一段时间。
④使三颈烧瓶内溶液保持140℃恒温,充分反应。
⑤反应结束后,关闭活塞K,向三颈烧瓶中加入干燥剂。
⑥继续加热,收集182~186℃馏分,将所得馏分进行二次纯化,最终得到较纯苯胺5.6g。
回答下列问题:___________ 。
(2)长颈漏斗内的试剂最好选用___________ 。
a.稀盐酸 b.稀硝酸 c.稀硫酸
(3)A装置是一个简易启普发生器,其优点是___________ ,若实验中未先通入H2一段时间,则可能产生的不良后果是___________ 。
(4)步骤⑤中干燥剂可选用___________ 。
a.浓硫酸 b.碱石灰 c.无水硫酸镁 d.五氧化二磷
(5)二次纯化并测定产率:
蒸馏所得苯胺中混有少量硝基苯杂质,可以采用如下方案除杂提纯:___________ ,“液相”是___________ (填“水层”或“有机层”)。
(6)苯胺与甲苯相对分子质量相近,但沸点相差较大,试从物质结构的角度说明原因___________ 。
(7)本实验的产率为___________ (保留一位小数)。
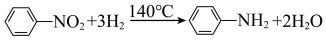
| 物质 | 相对分子质量 | 沸点/℃ | 密度g/mL | 溶解性 |
| 硝基苯 | 123 | 210.9 | 1.23 | 不溶于水,易溶于乙醇、乙醚 |
| 苯胺 | 93 | 184.4 | 1.02 | 微溶于水,易溶于乙醇、乙醚 |
| 甲苯 | 92 | 110.6 | 0.872 | 略 |
①组装好实验装置(如图,部分夹持仪器已略去),并检查装置气密性。
②向三颈烧瓶中依次加入沸石及10mL硝基苯。
③打开活塞K,先通入H2一段时间。
④使三颈烧瓶内溶液保持140℃恒温,充分反应。
⑤反应结束后,关闭活塞K,向三颈烧瓶中加入干燥剂。
⑥继续加热,收集182~186℃馏分,将所得馏分进行二次纯化,最终得到较纯苯胺5.6g。
回答下列问题:

(2)长颈漏斗内的试剂最好选用
a.稀盐酸 b.稀硝酸 c.稀硫酸
(3)A装置是一个简易启普发生器,其优点是
(4)步骤⑤中干燥剂可选用
a.浓硫酸 b.碱石灰 c.无水硫酸镁 d.五氧化二磷
(5)二次纯化并测定产率:
蒸馏所得苯胺中混有少量硝基苯杂质,可以采用如下方案除杂提纯:

(6)苯胺与甲苯相对分子质量相近,但沸点相差较大,试从物质结构的角度说明原因
(7)本实验的产率为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


