解答题-原理综合题 较难0.4 引用1 组卷164
2023年全国政府工作报告指出,推动重点领域节能降碳减污。一种太空生命保障系统利用电解水供氧,生成的氢气与宇航员呼出的二氧化碳在催化剂作用下生成水和甲烷,水可循环使用。
(1)已知 与
与 的燃烧热分别为
的燃烧热分别为 ,
, ,
,
 ,写出
,写出 与
与 反应生成
反应生成 和
和 的热化学方程式
的热化学方程式_____ 。
(2)一定温度下,在恒容密闭容器中 与
与 反应生成
反应生成 和
和 。
。
①能说明该反应达到平衡状态的是_______ (填字母)。
A. B.容器内压强一定 C.气体平均相对分子,质量一定
B.容器内压强一定 C.气体平均相对分子,质量一定
D.气体密度一定 E. 的体积分数一定
的体积分数一定
②已知容器的容积为5L初始加入0.2mol 和0.6mol
和0.6mol ,反应平衡后测得
,反应平衡后测得 的转化率为50%,则该反应的平衡常数为
的转化率为50%,则该反应的平衡常数为_______ 。
③温度不变,再加入 、
、 、
、 、
、 各0.2mol,则
各0.2mol,则
_______  。(填“>”“<”或“=”)
。(填“>”“<”或“=”)
(3)工业上在一定条件下利用 与
与 可直接合成有机中间体二甲醚:
可直接合成有机中间体二甲醚: 。当
。当 时,实验测得
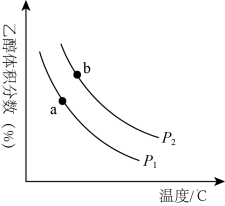
时,实验测得 的平衡转化率檤温度及压强变化如图所示。
的平衡转化率檤温度及压强变化如图所示。
_______ (填“>”或“<”)0。
②图中压强(p)由大到小的顺序是_______ 。
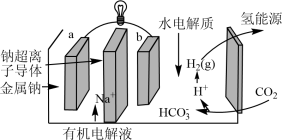
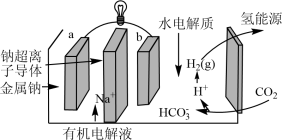
(4)科学家研发出一种新系统,通过“溶解”水中的二氧化碳,以触发电化学反应,有效减少碳的排放,其工作原理如图所示。_______ 。
(1)已知
(2)一定温度下,在恒容密闭容器中
①能说明该反应达到平衡状态的是
A.
D.气体密度一定 E.
②已知容器的容积为5L初始加入0.2mol
③温度不变,再加入
(3)工业上在一定条件下利用
②图中压强(p)由大到小的顺序是
(4)科学家研发出一种新系统,通过“溶解”水中的二氧化碳,以触发电化学反应,有效减少碳的排放,其工作原理如图所示。
2024·陕西西安·模拟预测
类题推荐
当今世界多国相继规划了碳达峰、碳中和的时间节点,中国承诺2030年前,二氧化碳的排放不再增长,达到峰值之后逐步降低。2060年前实现“碳中和”,体现了中国对解决气候问题的大国担当。因此,降低空气中二氧化碳含量成为研究热点,其中研发二氧化碳的利用技术,将二氧化碳转化为能源是缓解环境和解决能源问题的方案之一、
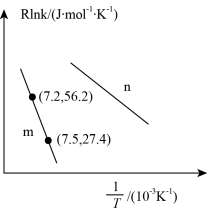
Ⅰ.二氧化碳在一定条件下转化为甲烷,其反应过程如下图所示。
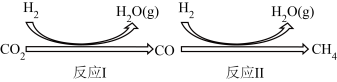
已知:CO2(g)+4H2(g)⇌CH4(g)+2H2O(g) ΔHl=-205kJ∙mol-1
反应Ⅱ:CO(g)+3H2(g)⇌CH4(g)+H2O(g) ΔH2=-246kJ∙mol-1
(1)则反应Ⅰ的热化学方程式为___________ 。
(2)一定条件下,向2L恒容密闭容器中加入1molCO2和5molH2,只发生上述反应Ⅰ和反应Ⅱ;10min后容器内总压强(P)不再变化,容器中CH4为0.6mol,CO2为0.2mol,H2O为1.4mol,10min内H2的平均反应速率
___________ ,CH4的体积分数=___________ 。
Ⅱ.在催化剂作用下CO2加氢还可制得甲醇。
(3)能说明反应CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH=+50kJ∙mol-1已达平衡状态的是___________(填字母)。
Ⅲ.催化重整制备CH3OCH3的过程中存在反应:
①2CO2(g)+6H2(g)⇌CH3OCH3(g)+3H2O(g) ΔH<0;
②CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH>0。
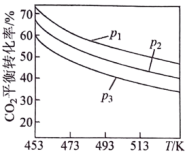
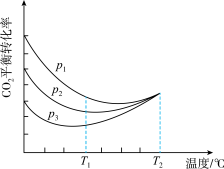
(4)向密闭容器中以物质的量之比为1∶3充入CO2与H2,实验测得CO2的平衡转化率随温度和压强的变化关系如图所示。P1、P2、P3由大到小的顺序为___________ ;T2℃时主要发生反应________ (填“①”或“②”)。
(5)科学家研发出一种新系统,通过“溶解”水中的二氧化碳,以触发电化学反应,有效减少碳的排放,其工作原理如图所示。系统工作时,a极为________ 极,b极区的电极反应式为___________ 。
Ⅰ.二氧化碳在一定条件下转化为甲烷,其反应过程如下图所示。

已知:CO2(g)+4H2(g)⇌CH4(g)+2H2O(g) ΔHl=-205kJ∙mol-1
反应Ⅱ:CO(g)+3H2(g)⇌CH4(g)+H2O(g) ΔH2=-246kJ∙mol-1
(1)则反应Ⅰ的热化学方程式为
(2)一定条件下,向2L恒容密闭容器中加入1molCO2和5molH2,只发生上述反应Ⅰ和反应Ⅱ;10min后容器内总压强(P)不再变化,容器中CH4为0.6mol,CO2为0.2mol,H2O为1.4mol,10min内H2的平均反应速率
Ⅱ.在催化剂作用下CO2加氢还可制得甲醇。
(3)能说明反应CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH=+50kJ∙mol-1已达平衡状态的是___________(填字母)。
| A.单位时间内生成1molCH3OH(g)的同时消耗了3molH2(g) |
| B.在恒温恒容的容器中,混合气体的密度保持不变 |
| C.在绝热恒容的容器中,反应的平衡常数不再变化 |
| D.在恒温恒压的容器中,气体的平均摩尔质量不再变化 |
Ⅲ.催化重整制备CH3OCH3的过程中存在反应:
①2CO2(g)+6H2(g)⇌CH3OCH3(g)+3H2O(g) ΔH<0;
②CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH>0。
(4)向密闭容器中以物质的量之比为1∶3充入CO2与H2,实验测得CO2的平衡转化率随温度和压强的变化关系如图所示。P1、P2、P3由大到小的顺序为

(5)科学家研发出一种新系统,通过“溶解”水中的二氧化碳,以触发电化学反应,有效减少碳的排放,其工作原理如图所示。系统工作时,a极为

Ⅰ.中国积极推进低碳发展,力争在2030年前实现碳达峰,2060年前实现碳中和。
(1)近年来,科学家致力于将一氧化碳和二氧化碳转化为有机物的技术研究。
已知:①CO(g)+H2O(g) HCOOH(g) △H1=-72.6kJ•mol-1
HCOOH(g) △H1=-72.6kJ•mol-1
②2CO(g)+O2(g) 2CO2(g) △H2=-566.0kJ•mol-1
2CO2(g) △H2=-566.0kJ•mol-1
则反应2CO2(g)+2H2O(g) 2HCOOH(g)+O2(g)的△H=
2HCOOH(g)+O2(g)的△H=________ kJ•mol-1。
(2)一种太空生命保障系统利用电解水供氧,生成的氢气与宇航员呼出的二氧化碳在催化剂作用下生成水和甲烷,水可循环使用。已知1gH2与CO2完全反应生成甲烷和气态水释放20.5kJ的热量,该反应的热化学方程式为_______ 。
Ⅱ.CO2可转化成有机物实现碳循环。在恒温条件下,向体积为2L的密闭容器中充入1molCO2和3molH2,发生CO2(g)+3H2(g) CH3OH(g)+H2O(g),测得CO2(g)和CH3OH(g)的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g),测得CO2(g)和CH3OH(g)的物质的量随时间变化如图所示。
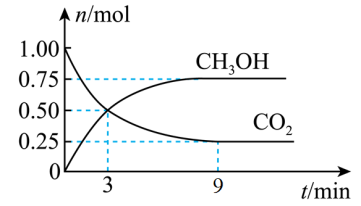
(3)从0~3min,v(H2)=________ mol•L-1•min-1。
(4)能说明上述反应达到平衡状态的是________ (填字母)。
(5)一定温度下,第9分钟时v逆(CH3OH)______ (填“>”、“<”或“=”)第3分钟时v正(CH3OH)。
(6)平衡时混合气体中CH3OH(g)的体积分数是________ 。
Ⅲ.近几年开发的甲醇燃料电池是采用铂作电极催化剂,电池中的质子交换膜只允许质子(H+)和水分子通过,其工作原理的示意图如图。
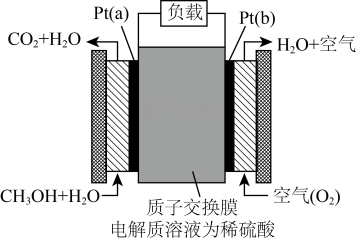
(7)通入甲醇(CH3OH)一极的电极反应式为________ 。
(8)每消耗3.2gCH3OH,理论上有________ molH+通过质子交换膜。
(1)近年来,科学家致力于将一氧化碳和二氧化碳转化为有机物的技术研究。
已知:①CO(g)+H2O(g)
②2CO(g)+O2(g)
则反应2CO2(g)+2H2O(g)
(2)一种太空生命保障系统利用电解水供氧,生成的氢气与宇航员呼出的二氧化碳在催化剂作用下生成水和甲烷,水可循环使用。已知1gH2与CO2完全反应生成甲烷和气态水释放20.5kJ的热量,该反应的热化学方程式为
Ⅱ.CO2可转化成有机物实现碳循环。在恒温条件下,向体积为2L的密闭容器中充入1molCO2和3molH2,发生CO2(g)+3H2(g)

(3)从0~3min,v(H2)=
(4)能说明上述反应达到平衡状态的是
| A.H2的生成速率是H2O生成速率的3倍 |
| B.混合气体的密度不随时间的变化而变化 |
| C.反应中CO2与CH3OH的物质的量浓度之比为1:1 |
| D.混合气体的平均相对分子质量不随时间的变化而变化 |
(6)平衡时混合气体中CH3OH(g)的体积分数是
Ⅲ.近几年开发的甲醇燃料电池是采用铂作电极催化剂,电池中的质子交换膜只允许质子(H+)和水分子通过,其工作原理的示意图如图。

(7)通入甲醇(CH3OH)一极的电极反应式为
(8)每消耗3.2gCH3OH,理论上有
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网