解答题-原理综合题 较难0.4 引用1 组卷42
甲醇既可用于基本有机原料,又可作为燃料用于替代矿物燃料。
(1)以下是工业上合成甲醇的反应:CO(g)+2H2(g) CH3OH(g) △H,下表所列数据是该反应在不同温度下的化学平衡常数(K)
CH3OH(g) △H,下表所列数据是该反应在不同温度下的化学平衡常数(K)
由表中数据判断反应为___________ 热反应(填“吸”或“放”);某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2mol/L,则CO的转化率为___________ ,此时的温度为___________ (从表中选择)。
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) △H1kJ/mol
②2CO(g)+O2(g)=2CO2(g) △H2kJ/mol
③H2O(g)=H2O(l) △H3kJ/mol
则CH3OH(l)+O2(g)=CO(g)+2H2O(l) △H=___________ kJ/mol(用△H1、△H2、△H3表示)
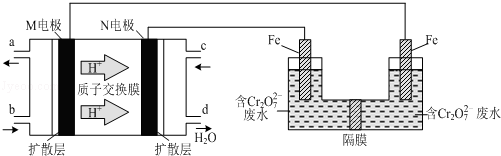
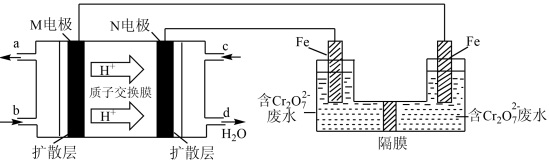
(3)现以甲醇燃料电池,采用电解法来处理酸性含铬废水(主要含有 )时,实验室利用如图装置模拟该法:
)时,实验室利用如图装置模拟该法:___________ 。
(4)处理废水时,最后Cr3+以Cr(OH)3形式除去,当c(Cr3+)=1×10-5mol·L-1时,Cr3+沉淀完全,此时溶液的pH=___________ 。(已知,Ksp=6.4×10-31,lg2=0.3)
(1)以下是工业上合成甲醇的反应:CO(g)+2H2(g)
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) △H1kJ/mol
②2CO(g)+O2(g)=2CO2(g) △H2kJ/mol
③H2O(g)=H2O(l) △H3kJ/mol
则CH3OH(l)+O2(g)=CO(g)+2H2O(l) △H=
(3)现以甲醇燃料电池,采用电解法来处理酸性含铬废水(主要含有
(4)处理废水时,最后Cr3+以Cr(OH)3形式除去,当c(Cr3+)=1×10-5mol·L-1时,Cr3+沉淀完全,此时溶液的pH=
23-24高二上·福建福州·期末
类题推荐
甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)工业上一般采用下列两种反应合成甲醇:
反应Ⅰ: CO(g) + 2H2(g)⇌CH3OH(g) ΔH1
反应Ⅱ: CO2(g) + 3H2(g)⇌CH3OH(g) + H2O(g) ΔH2
①反应Ⅱ的平衡常数表达式是______ 。
②下表所列数据是反应Ⅰ在不同温度下的化学平衡常数(K)。
由表中数据判断ΔH1______ 0 (填“>”、“=”或“<”)。
③某温度下,将2 mol CO和6 mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)= 0.2 mol/L,则CO的转化率为______ 。
(2)已知在常温常压下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH1= -1275.6 kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ΔH2= -566.0 kJ/mol
③ H2O(g) = H2O(l) ΔH3= -44.0 kJ/mol写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:______ 。
(3)某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置。该电池正极的电极反应为______ 。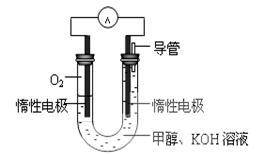
(1)工业上一般采用下列两种反应合成甲醇:
反应Ⅰ: CO(g) + 2H2(g)⇌CH3OH(g) ΔH1
反应Ⅱ: CO2(g) + 3H2(g)⇌CH3OH(g) + H2O(g) ΔH2
①反应Ⅱ的平衡常数表达式是
②下表所列数据是反应Ⅰ在不同温度下的化学平衡常数(K)。
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
由表中数据判断ΔH1
③某温度下,将2 mol CO和6 mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)= 0.2 mol/L,则CO的转化率为
(2)已知在常温常压下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH1= -1275.6 kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ΔH2= -566.0 kJ/mol
③ H2O(g) = H2O(l) ΔH3= -44.0 kJ/mol写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
(3)某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置。该电池正极的电极反应为

能源短缺是人类社会面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)工业上一般采用下列两种反应合成甲醇:
反应Ⅰ:CO(g)+2H2(g)⇌CH3OH(g)△H1
反应Ⅱ:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)△H2
①上述反应符合“原子经济”原则的是________ (填“I”或“Ⅱ”);
②下表所列数据是反应I在不同温度下的化学平衡常数(K)
由表中数据判断△H1________ 0 (填“>”、“=”或“<”);
③某温度下,将2mol CO和6mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2mol/L,则CO的转化率为________ ,此时的温度为________ (从上表中选择);
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) △H=﹣1275.6kJ/mol
②2CO(g)+O2(g)=2CO2(g) △H=﹣566.0kJ/mol
③H2O(g)=H2O(l) △H=﹣44.0kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:___________ ;
(3)某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置。
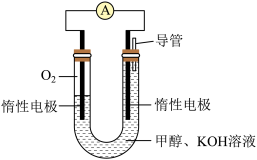
①该电池正极的电极反应为___________ ;
②工作一段时间后,测得溶液的pH减小,该电池总反应的离子方程式为___________ 。
(1)工业上一般采用下列两种反应合成甲醇:
反应Ⅰ:CO(g)+2H2(g)⇌CH3OH(g)△H1
反应Ⅱ:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)△H2
①上述反应符合“原子经济”原则的是
②下表所列数据是反应I在不同温度下的化学平衡常数(K)
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
③某温度下,将2mol CO和6mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2mol/L,则CO的转化率为
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) △H=﹣1275.6kJ/mol
②2CO(g)+O2(g)=2CO2(g) △H=﹣566.0kJ/mol
③H2O(g)=H2O(l) △H=﹣44.0kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
(3)某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置。

①该电池正极的电极反应为
②工作一段时间后,测得溶液的pH减小,该电池总反应的离子方程式为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网