解答题-结构与性质 适中0.65 引用1 组卷43
元素周期表中的四种元素A、B、C、D、E、F,原子序数依次增大。A的基态原子价层电子排布为 ;B的基态原子2p能级有3个单电子;C的原子最外层电子数是其内层的3倍;D的基态原子的3p轨道上有4个电子;
;B的基态原子2p能级有3个单电子;C的原子最外层电子数是其内层的3倍;D的基态原子的3p轨道上有4个电子; 的3d轨道中有10个电子;F单质在金属活动性顺序中排在最末位。
的3d轨道中有10个电子;F单质在金属活动性顺序中排在最末位。
(1)A、B形成的 常作为配位化合物中的配体。在
常作为配位化合物中的配体。在 中,元素A的原子采取sp杂化,则A与B形成的化学键中含有的σ键与π键的数目之比为
中,元素A的原子采取sp杂化,则A与B形成的化学键中含有的σ键与π键的数目之比为___________ 。
(2)B的基态原子的价电子排布图___________ ;E的基态原子的电子排布式___________ ;C与D形成的DC3的空间构型为___________ ;C与D可形成的 的VSEPR模型为
的VSEPR模型为___________ (用文字描述)。
(3)E与D所形成化合物晶体的晶胞如下图所示。在该晶胞中,E离子的数目为___________ ;与E离子周围紧邻且距离相等的D离子共有___________ 个;该化合物的化学式为___________ ;该晶胞边长为a pm,则E离子与D离子之间的最短距离为___________ cm。___________ 。
(5)E、F均能与 形成配离子,已知
形成配离子,已知 与
与 形成配离子时,配位数为4;
形成配离子时,配位数为4; 与
与 形成配离子时,配位数为2。工业上常用
形成配离子时,配位数为2。工业上常用 和
和 形成的配离子与E单质反应,生成
形成的配离子与E单质反应,生成 与
与 形成的配离子和F单质来提取F,写出上述反应的离子方程式
形成的配离子和F单质来提取F,写出上述反应的离子方程式___________ 。
(1)A、B形成的
(2)B的基态原子的价电子排布图
(3)E与D所形成化合物晶体的晶胞如下图所示。在该晶胞中,E离子的数目为

(5)E、F均能与
23-24高二下·内蒙古赤峰·阶段练习
类题推荐
A、B、X、Y、Z是l~36号原元素中,原子序数依次递增的5种元素,其原子结构或元素性质如下:
(1)A元素在周期表中的位置为_______
(2)上述5种元素中:
①原子半径最大的是_______ (填元素符号,下同)。
②电负性最大的是_______ 。
③位于周期表p区的元素有_______ 。
④从原子结构的角度解释元素B的第一电离能高于同周期相邻元素的原因_______ 。
(3) 可与某种冠醚形成具有特定结构和功能的聚集体,如右图所示。
可与某种冠醚形成具有特定结构和功能的聚集体,如右图所示。 与冠醚之间的作用力属于
与冠醚之间的作用力属于_______ (填字母)。
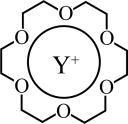
a.离子键 b.配位键 c.氢键 d.范德华力
(4)A、B形成的 常做配位化合物的配体。
常做配位化合物的配体。
①在 中,元素A的原子采取sp杂化,则A与B形成的化学键中含有的σ键与π键的数目之比为
中,元素A的原子采取sp杂化,则A与B形成的化学键中含有的σ键与π键的数目之比为_______ 。
②Z元素与金元素(Au)均能与 形成配离子。已知,
形成配离子。已知, 与
与 形成配离子时,配位数为4;
形成配离子时,配位数为4; 与
与 形成配离子时,配位数为2,工业常用
形成配离子时,配位数为2,工业常用 与
与 形成配离子与Z单质反应,生成
形成配离子与Z单质反应,生成 与
与 形成配离子和Au单质来提取Au,写出上述反应的离子方程式:
形成配离子和Au单质来提取Au,写出上述反应的离子方程式:_______ 。
| 元素 | 元素性质或原子结构 |
| A | 基态原子价层电子排布式为 |
| B | 基态原子2p能级有3个单电子 |
| X | 原子最外层电子数是其内层电子数的3倍 |
| Y | 单质与水剧烈反应,发出紫色火焰 |
| Z |
(2)上述5种元素中:
①原子半径最大的是
②电负性最大的是
③位于周期表p区的元素有
④从原子结构的角度解释元素B的第一电离能高于同周期相邻元素的原因
(3)

a.离子键 b.配位键 c.氢键 d.范德华力
(4)A、B形成的
①在
②Z元素与金元素(Au)均能与
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


