解答题-原理综合题 适中0.65 引用1 组卷117
含硫化合物是实验室和工业上的常用化学品。
回答下列问题:
(1)实验室可用铜与浓硫酸反应制备少量 :
:
 ,判断该反应的自发性,并说明理由
,判断该反应的自发性,并说明理由___________ 。
(2)在一个固定容积为 的密闭容器中,充入
的密闭容器中,充入 和
和 ,半分钟后达到平衡,测得容器中含
,半分钟后达到平衡,测得容器中含 ,则
,则
___________  。若继续通入
。若继续通入 和
和 ,则平衡
,则平衡___________ 移动(填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡时,___________ 
___________  。
。
(3)接触法制硫酸工艺中,其主反应在 并有催化剂存在条件下进行:
并有催化剂存在条件下进行:

①该热化学反应方程式的含义是___________ 。
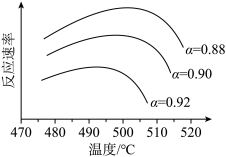
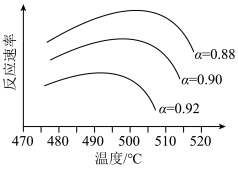
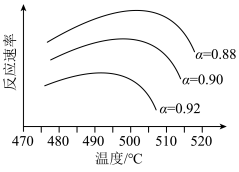
②为寻求固定投料比下不同反应阶段的最佳生产温度,绘制相应转化率(α)下反应速率(数值已略去)与温度的关系如图所示。下列说法正确的是___________ (填标号)。
a.温度越高,反应速率越大
b. 的曲线代表平衡转化率
的曲线代表平衡转化率
c. 越大,反应速率最大值对应温度越低
越大,反应速率最大值对应温度越低
d.可根据不同 对应的最大反应速率,选择最佳生产温度
对应的最大反应速率,选择最佳生产温度
③设 的平衡分压为
的平衡分压为 的平衡转化率为
的平衡转化率为 ,用含
,用含 和
和 的代数式表示上述催化氧化反应的
的代数式表示上述催化氧化反应的
___________ (用平衡分压代替平衡浓度)。
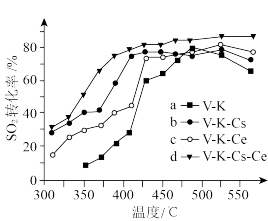
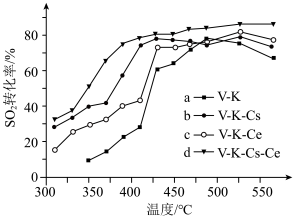
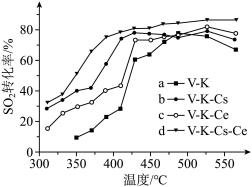
④为提高钒催化剂的综合性能,我国科学家对其进行了改良。不同催化剂下,温度和转化率关系如下图所示,催化性能最佳的是___________ (填标号)。
回答下列问题:
(1)实验室可用铜与浓硫酸反应制备少量
(2)在一个固定容积为
(3)接触法制硫酸工艺中,其主反应在
①该热化学反应方程式的含义是
②为寻求固定投料比下不同反应阶段的最佳生产温度,绘制相应转化率(α)下反应速率(数值已略去)与温度的关系如图所示。下列说法正确的是

a.温度越高,反应速率越大
b.
c.
d.可根据不同
③设
④为提高钒催化剂的综合性能,我国科学家对其进行了改良。不同催化剂下,温度和转化率关系如下图所示,催化性能最佳的是

2024·河南开封·三模
类题推荐
合成氨工业和硫酸工业在国民经济中占有重要地位。
(1)在合成氨工业中,原料气(N2、H2及少量CO、NH3的混合气)在进入合成塔前需经过铜氨液处理,目的是除去其中的CO其反应为:[Cu(NH3)2]++CO+NH3 [Cu(NH3)3CO]+ △H<0。吸收CO后的铜氨液经过适当处理可再生,恢复其吸收CO的能力,可循环使用。铜氨液再生适宜的生产条件是
[Cu(NH3)3CO]+ △H<0。吸收CO后的铜氨液经过适当处理可再生,恢复其吸收CO的能力,可循环使用。铜氨液再生适宜的生产条件是_______ 。
(2)将等物质的量的H2和N2通入绝热恒容密闭容器中发生反应N2(g)+3H2(g) 2NH3(g) △H<0,下列选项表明反应一定已达平衡状态的是_______(填标号,下同)。
2NH3(g) △H<0,下列选项表明反应一定已达平衡状态的是_______(填标号,下同)。
接触法制硫酸的关键反应为SO2的催化氧化,二氧化硫在V2O5作用下的催化氧化是工业上生产硫酸的主要反应。SO2的催化氧化热化学方程式为:2SO2(g)+O2(g) 2SO3(g) △H=akJ·mol-1其催化机理分为三步:
2SO3(g) △H=akJ·mol-1其催化机理分为三步:
第1步:SO2(g)+V2O5(s) SO3(g)+V2O4(s) △H=bkJ·mol-1
SO3(g)+V2O4(s) △H=bkJ·mol-1
第2步:V2O4(s)+O2(g)+2SO2(g) 2VOSO4(s) △H=ckJ·mol-1
2VOSO4(s) △H=ckJ·mol-1
第3步:_______。
(3)第3步热化学方程式_______ (△H的值用a、b、c的代数式表示)。
(4)T℃时,将3molSO2和1molO2通入体积为2L的恒温恒容密闭容器中,发生反应。3min时反应达到平衡,此时测得O2还剩余0.1mol。则达平衡时SO2的转化率为_______ ;从反应开始至达到平衡,用SO3表示反应速率为_______ 。
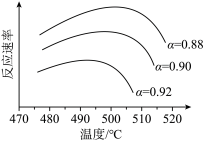
(5)为寻求固定投料比下不同反应阶段的最佳生产温度,绘制相应转化率(α)下反应速率(数值已略去)与温度的关系如下图所示,下列说法正确的是_______。
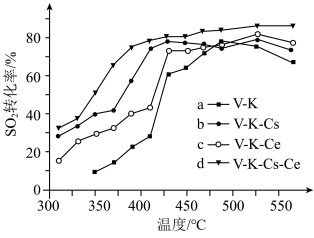
(6)为提高钒催化剂的综合性能,我国科学家对其进行了改良。不同催化剂下,温度和转化率关系如图所示,催化性能最佳的是_______ (填标号)。
(7)设O2的平衡分压为p,SO2的平衡转化率为α,用含p和α的代数式表示上述催化氧化反应的Kp=_______ (用平衡分压代替平衡浓度计算)。
(1)在合成氨工业中,原料气(N2、H2及少量CO、NH3的混合气)在进入合成塔前需经过铜氨液处理,目的是除去其中的CO其反应为:[Cu(NH3)2]++CO+NH3
(2)将等物质的量的H2和N2通入绝热恒容密闭容器中发生反应N2(g)+3H2(g)
| A.容器内的压强不再变化 |
| B.相同时间内,断开H-H键的数目和生成N-H键的数目相等 |
| C.容器内气体的浓度c(N2):c(H2):c(NH3)=1:3:2 |
| D.N2的体积分数不再发生变化 |
接触法制硫酸的关键反应为SO2的催化氧化,二氧化硫在V2O5作用下的催化氧化是工业上生产硫酸的主要反应。SO2的催化氧化热化学方程式为:2SO2(g)+O2(g)
第1步:SO2(g)+V2O5(s)
第2步:V2O4(s)+O2(g)+2SO2(g)
第3步:_______。
(3)第3步热化学方程式
(4)T℃时,将3molSO2和1molO2通入体积为2L的恒温恒容密闭容器中,发生反应。3min时反应达到平衡,此时测得O2还剩余0.1mol。则达平衡时SO2的转化率为
(5)为寻求固定投料比下不同反应阶段的最佳生产温度,绘制相应转化率(α)下反应速率(数值已略去)与温度的关系如下图所示,下列说法正确的是_______。

| A.温度越高,反应速率越大 |
| B.可根据不同α下的最大速率,选择最佳生产温度 |
| C.α=0.88的曲线代表平衡转化率 |
| D.α越大,反应速率最大值对应温度越低 |
(6)为提高钒催化剂的综合性能,我国科学家对其进行了改良。不同催化剂下,温度和转化率关系如图所示,催化性能最佳的是

(7)设O2的平衡分压为p,SO2的平衡转化率为α,用含p和α的代数式表示上述催化氧化反应的Kp=
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网