解答题-实验探究题 较易0.85 引用1 组卷81
焦亚硫酸钠 是一种抗氧化剂,受热易分解。某研究小组用下述方法制备少量
是一种抗氧化剂,受热易分解。某研究小组用下述方法制备少量 :在不断搅拌下,控制反应温度在
:在不断搅拌下,控制反应温度在 左右,向
左右,向 过饱和溶液中通入适量
过饱和溶液中通入适量 ,在
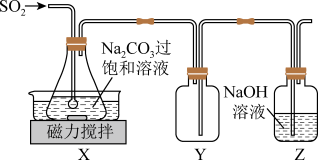
,在 左右静置结晶。实验装置如图所示。
左右静置结晶。实验装置如图所示。 的化学方程式为
的化学方程式为 ,该反应是否为氧化还原反应
,该反应是否为氧化还原反应_______ (填“是”或“否”)。
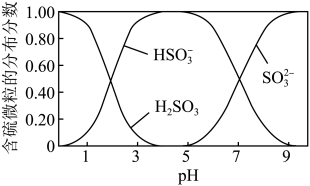
(2)已知平衡时含硫微粒的分布系数(分布系数 )与
)与 的关系如图所示。装置
的关系如图所示。装置 中,
中, 与
与 溶液反应的离子方程式为
溶液反应的离子方程式为_______ ;判定可停止通 的实验操作为
的实验操作为_______ 。
(3)装置 的作用是
的作用是_______ 。
(4)制得的 中混有
中混有 和
和 杂质,其可能的原因是
杂质,其可能的原因是_______ 。
(5)测定某葡萄酒中 残留量,取
残留量,取 样品,用
样品,用 的碘标准液滴定至终点,消耗
的碘标准液滴定至终点,消耗 标准液。滴定反应为
标准液。滴定反应为 。该样品中
。该样品中 的残留量为
的残留量为_______  ;以下操作会造成
;以下操作会造成 残留量测定值偏高的是
残留量测定值偏高的是_______ (填字母)。
A.滴定终点读数时,俯视滴定管的刻度
B.盛装待测液的锥形瓶用蒸馏水洗过,未用待测液润洗
C.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
(2)已知平衡时含硫微粒的分布系数(分布系数
(3)装置
(4)制得的
(5)测定某葡萄酒中
A.滴定终点读数时,俯视滴定管的刻度
B.盛装待测液的锥形瓶用蒸馏水洗过,未用待测液润洗
C.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
2024·海南·一模
类题推荐
生活中常用一定浓度的过氧乙酸 溶液作消毒液。某化学小组对过氧乙酸的制备和性质进行如下探究(夹持、加热及搅拌装置均未画出)。
溶液作消毒液。某化学小组对过氧乙酸的制备和性质进行如下探究(夹持、加热及搅拌装置均未画出)。

Ⅰ.在磁力搅拌作用下,向仪器 中加入一定量的冰醋酸和浓硫酸,打开开关
中加入一定量的冰醋酸和浓硫酸,打开开关 ,缓缓滴入适量30%的
,缓缓滴入适量30%的 溶液,控制温度在20~30℃。已知:过氧乙酸的氧化性强于高锰酸钾的。
溶液,控制温度在20~30℃。已知:过氧乙酸的氧化性强于高锰酸钾的。
(1)仪器 的名称为
的名称为_______ 。
(2)仪器 与分液漏斗相比,其优点是
与分液漏斗相比,其优点是_______ 。
(3)温度不能超过30℃的原因是_______ 。
Ⅱ.过氧乙酸样品中常含有残留的 。样品中过氧乙酸的浓度为
。样品中过氧乙酸的浓度为 时,发生如下反应:①
时,发生如下反应:① ;
;
② ;
;
③ 。
。
i.取 待测液并用硫酸酸化,再用
待测液并用硫酸酸化,再用 的
的 标准溶液滴定待测液至溶液呈粉红色,消耗
标准溶液滴定待测液至溶液呈粉红色,消耗 标准溶液。
标准溶液。
ii.另取 待测液,加入过量的
待测液,加入过量的 溶液和几滴淀粉,并用硫酸酸化,再用
溶液和几滴淀粉,并用硫酸酸化,再用 的
的 标准溶液滴定,达到滴定终点时消耗
标准溶液滴定,达到滴定终点时消耗 标准溶液。
标准溶液。
(4)i中发生反应的离子方程式为_______ 。ii中用 标准溶液进行滴定时,达到滴定终点的标志是
标准溶液进行滴定时,达到滴定终点的标志是_______ ,过氧乙酸的浓度
_______  (用含
(用含 、
、 、
、 、
、 、
、 、
、 的代数式表示)。
的代数式表示)。
(5)当其他操作均正确时,下列实验操作可能使测定结果偏高的是_______(填标号)。

Ⅰ.在磁力搅拌作用下,向仪器
(1)仪器
(2)仪器
(3)温度不能超过30℃的原因是
Ⅱ.过氧乙酸样品中常含有残留的
②
③
i.取
ii.另取
(4)i中发生反应的离子方程式为
(5)当其他操作均正确时,下列实验操作可能使测定结果偏高的是_______(填标号)。
| A.配制 |
| B.盛装 |
| C.用 |
| D.用 |
氯系消毒剂是目前使用最广泛的一类消毒剂,在生产生活中有着重要的应用,主要有氯气、次氯酸、次氯酸盐、亚氯酸钠、二氧化氯等。
(1)同温同压下,研究 分别在不同浓度的盐酸和
分别在不同浓度的盐酸和 溶液中的溶解度(用溶解
溶液中的溶解度(用溶解 的物质的量浓度表示)变化如图所示。已知氯气在溶解时存在以下平衡:
的物质的量浓度表示)变化如图所示。已知氯气在溶解时存在以下平衡:

①

②

③

随着 浓度的增大,
浓度的增大, 溶解度减小,溶液中
溶解度减小,溶液中
___________ (填“变大”“变小”或“不变”);a点时, 、
、 、
、 、
、 四种离子浓度由大到小的顺序为
四种离子浓度由大到小的顺序为___________ 。
(2) 是一种高效漂白剂。经测定,25℃时
是一种高效漂白剂。经测定,25℃时 溶液中各组分分布系数随
溶液中各组分分布系数随 变化情况如图所示(
变化情况如图所示( 未画出)。
未画出)。
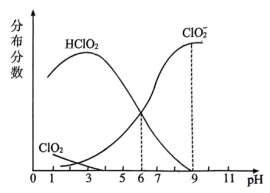
①25℃时,
___________  。
。
②25℃时,浓度均为 的
的 和
和 的混合溶液中,
的混合溶液中,
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(3)为测定某 消毒剂样品中含氯量,用
消毒剂样品中含氯量,用 溶液滴定该样品溶液,操作如下:
溶液滴定该样品溶液,操作如下:
a.取样:取 样品溶液置于锥形瓶,加入稀硫酸酸化,发生反应:
样品溶液置于锥形瓶,加入稀硫酸酸化,发生反应: (
( 极易溶于水);
极易溶于水);
b.氧化:加入足量碘化钾溶液,振荡充分反应;
c.滴定:加入淀粉作指示剂,在锥形瓶下垫一张白纸,用 标准溶液滴定碘单质(
标准溶液滴定碘单质( );
);
d.重复上述操作三次。
滴定时,左手控制滴定管,右手摇动锥形瓶,眼睛注视___________ ,直到加入半滴 溶液后,溶液
溶液后,溶液___________ ,即到终点。
测得的实验数据如下表:
由以上数据计算该样品溶液的含氯量(以 计)
计)___________  (保留三位有效数字)。滴定时,有一组数据出现了明显异常,所测含氯量偏大,原因可能有
(保留三位有效数字)。滴定时,有一组数据出现了明显异常,所测含氯量偏大,原因可能有___________ (填字母序号)。
A.取样时用 的滴定管液面在
的滴定管液面在 处放出所有溶液
处放出所有溶液
B.滴定终点读数时仰视刻度线
C.达终点时滴定管尖嘴有标准液悬挂
D.盛装待测液的锥形瓶未润洗
E.摇动锥形瓶时有液体溅出
(1)同温同压下,研究

①
②
③
随着
(2)

①25℃时,
②25℃时,浓度均为
(3)为测定某
a.取样:取
b.氧化:加入足量碘化钾溶液,振荡充分反应;
c.滴定:加入淀粉作指示剂,在锥形瓶下垫一张白纸,用
d.重复上述操作三次。
滴定时,左手控制滴定管,右手摇动锥形瓶,眼睛注视
测得的实验数据如下表:
| 实验序号 | 待测液体积( | ||
| 滴定前刻度/ | 滴定后刻度/ | ||
| 1 | 20.00 | 0.60 | 20.60 |
| 2 | 20.00 | 6.00 | 25.95 |
| 3 | 20.00 | 1.40 | 23.20 |
| 4 | 20.00 | 1.00 | 21.05 |
A.取样时用
B.滴定终点读数时仰视刻度线
C.达终点时滴定管尖嘴有标准液悬挂
D.盛装待测液的锥形瓶未润洗
E.摇动锥形瓶时有液体溅出
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网



