解答题-结构与性质 适中0.65 引用1 组卷64
当下新能源汽车电池的发展加大了对金属钻(Co)的需求。回答下列问题:
(1)基态Co原子价电子排布式为__________ ,Co2+有___ 个未成对电子。
(2)Co的第四电离能比Fe的第四电离能要小很多,原因是________________ 。
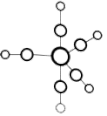
(3)Na3[Co(NO2)6]中的 中N原子为
中N原子为_______ 杂化,空间构型名称为_________ 形。
(4)一种Co(Ⅱ)的配合物结构如图所示,下列说法错误的是______(填序号)。
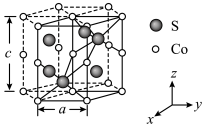
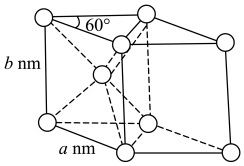
(5)金属钴晶胞结构及参数如图所示,该晶胞中Co的配位数为________ 。已知金属Co晶体密度为ρ g/cm3,则阿伏加德罗常数NA=___________ mol-1。
(1)基态Co原子价电子排布式为
(2)Co的第四电离能比Fe的第四电离能要小很多,原因是
(3)Na3[Co(NO2)6]中的
(4)一种Co(Ⅱ)的配合物结构如图所示,下列说法错误的是______(填序号)。
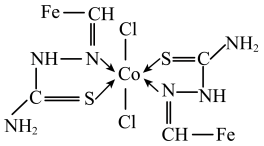
| A.配合物中的氯元素是Cl- |
| B.配合物中Co2+配位数为4 |
| C.结构中所有N原子有sp2、sp3杂化 |
D.结构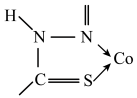 中所有原子共平面 中所有原子共平面 |
(5)金属钴晶胞结构及参数如图所示,该晶胞中Co的配位数为
23-24高三下·陕西西安·期中
类题推荐
Ⅰ.Fe3+可以与SCN-、CN-、F-、有机分子等形成很多的配合物。请回答下列问题:
(1)基态Fe3+的电子排布式可表示为__________________ 。
(2)与CN-互为等电子体的分子有___________ (写出2种)。
(3)金属配合物Fe(CO)n的中心原子价电子数与配体提供电子总数之和为18,则n=_____ 。
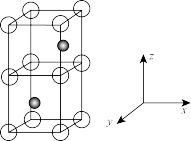
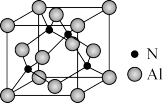
Ⅱ.已知氮化铝的晶胞结构如图所示。请回答下列问题:
(4)下列说法正确的是__________ (填序号)。
(5)NH3空间构型为______ ;已知(CH3)3Al为非极性分子,则其中铝原子的杂化方式为__________ 。
(6)若氮化铝可由(CH3)3Al和NH3在一定条件下反应制得,则反应的方程式为_________ 。
(7)若Al与N 原子最近的距离为a cm,则该晶体的密度为____ g/cm。(阿伏加德罗常数用NA表示)
(1)基态Fe3+的电子排布式可表示为
(2)与CN-互为等电子体的分子有
(3)金属配合物Fe(CO)n的中心原子价电子数与配体提供电子总数之和为18,则n=
Ⅱ.已知氮化铝的晶胞结构如图所示。请回答下列问题:

(4)下列说法正确的是
| A.氮化铝晶胞结构与NaCl相同 | B.第一电离能 N>Al |
| C.电负性N>Al | D.原子半径 N>Al |
(6)若氮化铝可由(CH3)3Al和NH3在一定条件下反应制得,则反应的方程式为
(7)若Al与N 原子最近的距离为a cm,则该晶体的密度为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网