单选题 较难0.4 引用1 组卷62
已知H2A为二元弱酸,Ka1(H2A)=1.0×10 3,常温下向Na2A溶液中逐惭加入一元弱酸HB溶液,溶液离子浓度变化关系如图所示。下列说法正确的是
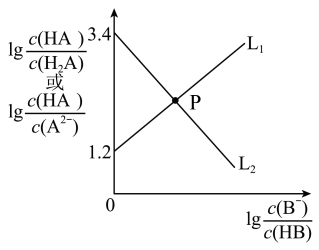
| A.K(HB)=10 2.8 |
| B.NaHA溶液呈碱性 |
| C.交点P对应溶液存在: c(H+)+c(A2-)+c(HA-)=c(B-)+c(OH-) |
| D.Na2A溶液中滴入足量HB溶液的离子方程式为A2-+HB=HA-+B- |
23-24高三下·陕西西安·期中
类题推荐
25℃时,用 NaOH 溶液滴定H2A 溶液,溶液中 和
和 、
、 和
和 关系如图所示,下列说法正确的是
关系如图所示,下列说法正确的是


| A.H2A 为弱酸,其Ka1约为 10−4 |
| B.滴定过程中,当 pH=5 时,c(Na+)+ c(H+)=3c(A2−)+c(OH−) |
| C.已知 H2CO3的 Ka1=4.3×10-7,Ka2=5.6×10-11,则足量Na2CO3溶液中滴入少量H2A溶液,发生的离子反应为:H2A + 2 |
| D.向H2A 溶液中加入等体积等浓度的NaOH 溶液,完全反应后溶液显碱性 |
常温下将NaOH溶液滴加到二元弱酸(H2A) 溶液中,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述正确的是


| A.曲线M表示pH与 |
| B. |
| C.当滴定到pH=7时,c(Na+)=c(A2-)+c(HA-) |
| D.电离常数Ka1(H2A)的数量级为10-3 |
常温下,向0.1mol∙L-1二元弱酸H2A溶液中逐滴加入NaOH溶液,H2A、HA-、A2-的物质的量分数[已知 ]。随pH的变化如图所示。下列叙述正确的是
]。随pH的变化如图所示。下列叙述正确的是
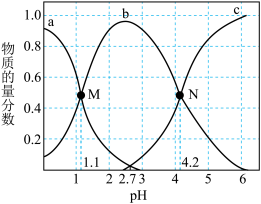

| A.b曲线代表A2-的物质的量分数随pH的变化 |
| B.M点pH=1.1时,溶液中微粒浓度的大小关系为:c(H+)>c(HA-)=c(H2A)>c(OH-) |
| C. pH=2.73时,c(A2-)+c(HA-)+ c(H2A)=0.1mol∙L-1 |
| D.N点pH=4.2时,c(A2-)=c(HA-),溶液中不存在H2A分子 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


