解答题-工业流程题 较难0.4 引用3 组卷278
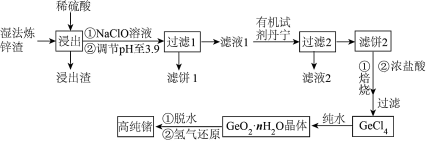
锗是一种重要的半导体材料,其有机化合物在治疗癌症方面有着独特的功效。如图为工业上利用湿法炼锌渣(主要含有 、
、 、
、 、
、 、
、 )制备高纯锗的工艺流程:
)制备高纯锗的工艺流程: 为两性化合物。②
为两性化合物。② 易水解,在浓盐酸中溶解度低。
易水解,在浓盐酸中溶解度低。
③常温下,部分金属阳离子转化为氢氧化物沉淀的pH见表。
④有机试剂丹宁沉淀金属离子的沉淀率见表。
(1)“浸出”时加热的目的是_______ ,该过程发生的主要反应为_______ ;浸出渣的主要成分是_______ (填化学式)。
(2)浸出后加入 溶液的作用是
溶液的作用是_______ (用离子方程式表示)。滤饼1中主要成分为一种,常温下调节溶液的pH范围为_______ 。如果不加 溶液,pH就需要调节到更大的数值,这样会造成
溶液,pH就需要调节到更大的数值,这样会造成_______ 的不良后果。
(3)“滤液2”中主要含有的金属阳离子是_______ (填离子符号)。
(4) 与纯水反应的化学方程式为
与纯水反应的化学方程式为_______ 。
(5)若含锗3.65%的湿法炼锌渣的质量为 ,氢气还原过程中参与反应的氢气体积为89.6L(标准状况下),则锗的回收率为
,氢气还原过程中参与反应的氢气体积为89.6L(标准状况下),则锗的回收率为_______ 。
③常温下,部分金属阳离子转化为氢氧化物沉淀的pH见表。
| 离子 | ||||
| 开始沉淀pH | 7.5 | 2.2 | 6.2 | 8.2 |
| 完全沉淀pH | 9.0 | 3.2 | 8.2 | 11.2 |
| 离子 | ||||
| 沉淀率(%) | 0 | 99 | 0 | 97~98.5 |
(2)浸出后加入
(3)“滤液2”中主要含有的金属阳离子是
(4)
(5)若含锗3.65%的湿法炼锌渣的质量为
2024·四川绵阳·三模
类题推荐
锗是一种重要的半导体材料,其有机化合物在治疗癌症方面有着独特的功效。下图为工业上利用湿法炼锌渣(主要含有GeO2、ZnO、FeO、Fe2O3、SiO2)制备高纯锗的工艺流程:
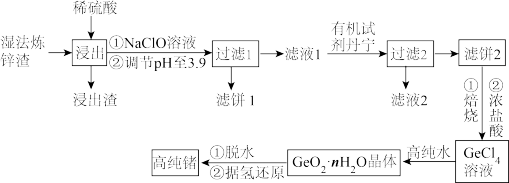
已知:①GeO2为两性化合物。
②常温下,部分金属阳离子转化为氢氧化物沉淀的pH见下表。
③有机试剂丹宁沉淀金属离子的沉淀率见下表。
(1)“浸出”时加热的目的是___________ ;浸出渣的主要成分是___________ (填化学式)。
(2)浸出后加入NaClO溶液的作用是___________ 。
(3)“滤液2”中主要含有的金属阳离子是___________ (填离子符号)。
(4)GeCl4与高纯水反应的化学方程式为___________ 。
(5)I2的一种制备方法如下图所示:
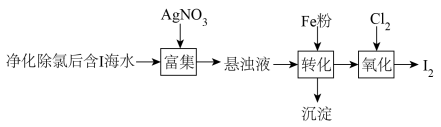
加入Fe粉进行转化反应的离子方程式为___________ ,生成的沉淀与硝酸反应,生成___________ 后可循环使用。

已知:①GeO2为两性化合物。
②常温下,部分金属阳离子转化为氢氧化物沉淀的pH见下表。
| 离子 | Fe2+ | Fe3+ | Zn2+ | Ge4+ |
| 开始沉淀pH | 7.5 | 2.2 | 6.2 | 8.2 |
| 完全沉淀pH | 9.0 | 3.2 | 8.2 | 11.2 |
| 离子 | Fe2+ | Fe3+ | Zn2+ | Ge4+ |
| 沉淀率(%) | 0 | 99 | 0 | 97~98.5 |
(2)浸出后加入NaClO溶液的作用是
(3)“滤液2”中主要含有的金属阳离子是
(4)GeCl4与高纯水反应的化学方程式为
(5)I2的一种制备方法如下图所示:

加入Fe粉进行转化反应的离子方程式为
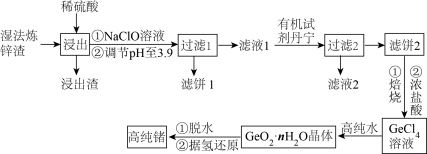
锗是一种重要的半导体材料。图为工业上利用湿法炼锌渣(主要含有GeO2、ZnO、FeO、Fe2O3、SiO2)制备高纯锗的工艺流程:
①GeO2为两性化合物。
②常温下,部分金属阳离子转化为氢氧化物沉淀的pH见下表。
③有机试剂丹宁沉淀金属阳离子的沉淀率见下表。
(1)为了提高锗元素浸出率,“浸出”时可采取的措施___________________ (任写2种)。
(2)浸出后加入NaClO溶液的作用是________________ (用离子方程式表示)。
(3)常温下调节溶液的pH至3.9时,
______  。
。
(4)“滤液2”中主要含有的金属阳离子是_________ (填离子符号)。
(5) GeCl4与高纯水反应的化学方程式为_____________________ 。
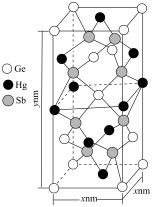
(6)锗(Ge)可与汞(Hg)和锑(Sb)可形成一种绝缘材料,晶胞结构如下图所示。____________ ,该晶胞中与Hg距离最近的Sb的数目为_________ 。
①GeO2为两性化合物。
②常温下,部分金属阳离子转化为氢氧化物沉淀的pH见下表。
离子 | ||||
开始沉淀时pH | 7.5 | 2.2 | 6.2 | 8.2 |
完全沉淀时pH[ | 9.0 | 3.2 | 8.2 | 11.2 |
离子 | ||||
沉淀率(%) | 0 | 99 | 0 | 97~98.5 |
(1)为了提高锗元素浸出率,“浸出”时可采取的措施
(2)浸出后加入NaClO溶液的作用是
(3)常温下调节溶液的pH至3.9时,
(4)“滤液2”中主要含有的金属阳离子是
(5) GeCl4与高纯水反应的化学方程式为
(6)锗(Ge)可与汞(Hg)和锑(Sb)可形成一种绝缘材料,晶胞结构如下图所示。
氧化铋( )俗称铋黄,广泛应用于医药合成、能源材料等领域。以铋精矿(主要成分
)俗称铋黄,广泛应用于医药合成、能源材料等领域。以铋精矿(主要成分 ,还含有
,还含有 、
、 、
、 、
、 等杂质)为原料制备
等杂质)为原料制备 的一种工艺流程如图所示:
的一种工艺流程如图所示:

已知:① 不溶于稀盐酸,酸浸后溶液中金属阳离子主要有
不溶于稀盐酸,酸浸后溶液中金属阳离子主要有 、
、 、
、 、
、 等;②
等;② 在
在 时开始水解,
时开始水解, 时
时 几乎完全水解为白色的BiOCl沉淀;
几乎完全水解为白色的BiOCl沉淀;
③常温下部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
请根据以上信息,回答下列问题:
(1)“酸浸”步骤浸出渣的主要成分除S外还有___________ ,该步骤中发生的最主要的氧化还原反应的离子方程为___________ 。
(2)“转化”步骤中加入盐酸羟胺( )的目的是
)的目的是___________ 。
(3)“调pH”步骤中加入 调节溶液的pH,其合理范围为
调节溶液的pH,其合理范围为___________ ;滤液1中主要的金属阳离子有___________ (填离子符号)。
(4)流程中生成 的化学方程式为
的化学方程式为___________ 。
(5)铋精矿中铋含量为79.42%,取铋精矿10kg,铋元素在整个流程中损失率为5%,经过上述流程可制得氧化铋的质量为___________ g(保留到小数点后一位)。

已知:①
③常温下部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 金属离子 | |||
| 开始沉淀 | 2.7 | 7.6 | 4.7 |
| 完全沉淀 | 3.7 | 9.6 | 6.7 |
(1)“酸浸”步骤浸出渣的主要成分除S外还有
(2)“转化”步骤中加入盐酸羟胺(
(3)“调pH”步骤中加入
(4)流程中生成
(5)铋精矿中铋含量为79.42%,取铋精矿10kg,铋元素在整个流程中损失率为5%,经过上述流程可制得氧化铋的质量为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


