解答题-工业流程题 适中0.65 引用1 组卷438
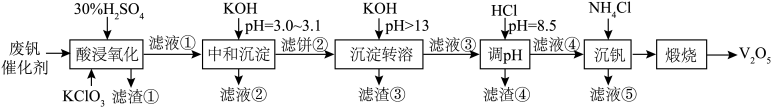
为回收利用废钒催化剂(含有V2O5、VOSO4、SiO2、Fe3O4以及钾和铝的硅酸盐),科研人员研制了一种回收V2O5的新工艺,主要流程如下图。
ii.VOSO4可溶、(VO2)2SO4易溶、V2O5和NH4VO3难溶; +2OH-=
+2OH-= +H2O
+H2O
(1)“酸浸氧化”时,VO2+转化成 反应的离子方程式为
反应的离子方程式为______ ,同时V2O5转化为 。滤渣①主要成分是
。滤渣①主要成分是______ 。
(2)“中和沉淀”中,钒水解并沉淀为V2O5·2H2O,随滤液②可除去金属离子K+以及部分的金属离子有______ 。
(3)“沉淀转溶”中,V2O5·2H2O转化为KVO3溶解,写出V2O5·2H2O与KOH反应的化学方程式______ 。
(4)“调pH”中滤渣④的主要成分是______ 。
(5)全钒液流储能电池可实现化学能和电能的相互转化,其原理如图所示。______ 。
②放电过程中,右槽溶液颜色变化的情况是______ 。
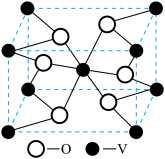
(6)钒的某种氧化物的立方晶胞结构如图所示,钒原子的配位数为______ 。若该晶胞的密度为ρg/cm3,且用NA表示阿伏加德罗常数,则该晶胞的边长为______ nm。
| 金属离子 | Fe3+ | Fe2+ | Al3+ |
| 开始沉淀pH | 1.9 | 7.0 | 3.0 |
| 完全沉淀pH | 3.2 | 9.0 | 4.7 |
(1)“酸浸氧化”时,VO2+转化成
(2)“中和沉淀”中,钒水解并沉淀为V2O5·2H2O,随滤液②可除去金属离子K+以及部分的金属离子有
(3)“沉淀转溶”中,V2O5·2H2O转化为KVO3溶解,写出V2O5·2H2O与KOH反应的化学方程式
(4)“调pH”中滤渣④的主要成分是
(5)全钒液流储能电池可实现化学能和电能的相互转化,其原理如图所示。
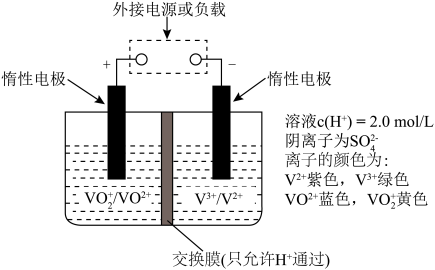
②放电过程中,右槽溶液颜色变化的情况是
(6)钒的某种氧化物的立方晶胞结构如图所示,钒原子的配位数为
2024·广东惠州·三模
类题推荐
钒具有广泛用途。黏土钒矿中,钒以+3、+4、+5价的化合物存在,还包括钾、镁的铝硅酸盐,以及SiO2、Fe3O4。采用以下工艺流程可由黏土钒矿制备NH4VO3。

该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)“酸浸氧化”需要加热,其原因是_____ 。
(2)“酸浸氧化”中,VO+和VO2+被氧化成 ,同时还有
,同时还有____ 离子被氧化。写出VO+转化为 反应的离子方程式
反应的离子方程式_____ 。
(3)“中和沉淀”中,钒水解并沉淀为V2O5·xH2O,随滤液②可除去金属离子K+、Mg2+、Na+、____ ,以及部分的_____ 。
(4)“沉淀转溶”中,V2O5·xH2O转化为钒酸盐溶解。滤渣③的主要成分是______ 。
(5)“调pH”中有沉淀生产,生成沉淀反应的化学方程式是____ 。

该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 | Fe3+ | Fe2+ | Al3+ | Mn2+ |
开始沉淀pH | 1.9 | 7.0 | 3.0 | 8.1 |
完全沉淀pH | 3.2 | 9.0 | 4.7 | 10.1 |
(1)“酸浸氧化”需要加热,其原因是
(2)“酸浸氧化”中,VO+和VO2+被氧化成
(3)“中和沉淀”中,钒水解并沉淀为V2O5·xH2O,随滤液②可除去金属离子K+、Mg2+、Na+、
(4)“沉淀转溶”中,V2O5·xH2O转化为钒酸盐溶解。滤渣③的主要成分是
(5)“调pH”中有沉淀生产,生成沉淀反应的化学方程式是
钒具有广泛用途。黏土钒矿中,钒以+3、+4、+5价的化合物存在,还包括钾、镁的铝硅酸盐,以及SiO2、Fe3O4。采用以下工艺流程可由黏土钒矿制备NH4VO3。
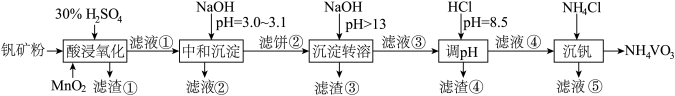
该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)“酸浸氧化”需要加热,其原因是___________ 。
(2)“酸浸氧化”中,VO+和VO2+被氧化成 ,同时还有
,同时还有___________ 离子被氧化。写出VO+转化为 反应的离子方程式
反应的离子方程式___________ 。
(3)“中和沉淀”中,钒水解并沉淀为 ,随滤液②可除去金属离子K+、Mg2+、Na+、
,随滤液②可除去金属离子K+、Mg2+、Na+、___________ ,以及部分的___________ 。
(4)“沉淀转溶”中, 转化为钒酸盐溶解。滤渣③的主要成分是
转化为钒酸盐溶解。滤渣③的主要成分是___________ 。
(5)“调pH”中有沉淀生产,生成沉淀反应的化学方程式是___________ 。
(6)“沉钒”中析出NH4VO3晶体时,需要加入过量NH4Cl,其原因是___________ 。

该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 | Fe3+ | Fe2+ | Al3+ | Mn2+ |
| 开始沉淀pH | 1.9 | 7.0 | 3.0 | 8.1 |
| 完全沉淀pH | 3.2 | 9.0 | 4.7 | 10.1 |
(1)“酸浸氧化”需要加热,其原因是
(2)“酸浸氧化”中,VO+和VO2+被氧化成
(3)“中和沉淀”中,钒水解并沉淀为
(4)“沉淀转溶”中,
(5)“调pH”中有沉淀生产,生成沉淀反应的化学方程式是
(6)“沉钒”中析出NH4VO3晶体时,需要加入过量NH4Cl,其原因是
黏土钒矿中,钒以+3、+4、+5的化合物存在,还包括钾、镁的铝硅酸盐,以及 。黏土钒矿采用以下工艺流程可制备偏钒酸铵。
。黏土钒矿采用以下工艺流程可制备偏钒酸铵。
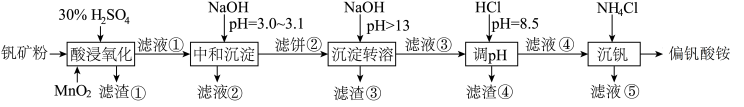
该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的 如下表所示:
如下表所示:
回答下列问题:
(1)钒在周期表中的位置为___________ 。
(2)写出“酸浸氧化”中 转化为
转化为 的离子方程式
的离子方程式___________ 。
(3)“中和沉淀”中,钒水解并沉淀为 ,滤液②中金属阳离子有
,滤液②中金属阳离子有 、
、
___________ 。
(4)“沉淀转溶”中, 溶解为
溶解为 或
或 ,滤渣③的主要成分是
,滤渣③的主要成分是___________ 。
(5)“调 ”中有沉淀产生,生成沉淀反应的化学方程式是
”中有沉淀产生,生成沉淀反应的化学方程式是___________ 。
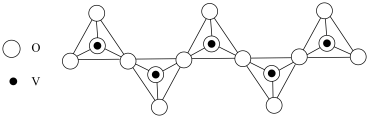
(6)偏钒酸铵,其阴离子呈如图所示的无限链状结构,则偏钒酸铵的化学式为___________ 。
(7)全钒液流储能电池是利用不同价态离子对的氧化还原反应来实现化学能和电能相互转化的装置,其原理如图所示。

①左槽溶液逐渐由黄变蓝,其电极反应式为___________ 。
②充电时若转移的电子数为 个,左槽溶液中
个,左槽溶液中 物质的量的变化量为
物质的量的变化量为___________ 。

该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的
| 金属离子 | ||||
| 开始沉淀 | 1.9 | 7.0 | 3.0 | 8.1 |
| 完全沉淀 | 3.2 | 9.0 | 4.7 | 10.1 |
(1)钒在周期表中的位置为
(2)写出“酸浸氧化”中
(3)“中和沉淀”中,钒水解并沉淀为
(4)“沉淀转溶”中,
(5)“调
(6)偏钒酸铵,其阴离子呈如图所示的无限链状结构,则偏钒酸铵的化学式为

(7)全钒液流储能电池是利用不同价态离子对的氧化还原反应来实现化学能和电能相互转化的装置,其原理如图所示。

①左槽溶液逐渐由黄变蓝,其电极反应式为
②充电时若转移的电子数为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


