解答题-实验探究题 适中0.65 引用1 组卷43
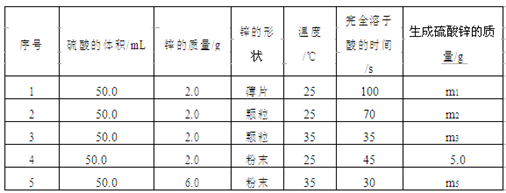
Ⅰ.控制变量法是化学实验的一种常用方法。下表是某学习小组研究等物质的量浓度的稀硫酸和锌反应的实验数据,分析以下数据,回答下列问题:
(1)化学反应速率本质上是由反应物本身的性质决定的,但外界条件也会影响反应速率的大小。本实验中实验2和实验3表明______ 对反应速率有影响。
(2)我们最好选取实验______ (填3个实验序号)研究锌的形状对反应速率的影响。我们发现在其它条件相同时,反应物间的______ 反应速率越快。
(3)若采用与实验1完全相同的条件,但向反应容器中滴加少量硫酸铜溶液,发现反应速率明显加快。原因是______ 。
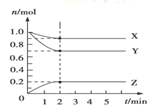
Ⅱ.某温度时,在5L的容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。请通过计算回答下列问题:______ 。
(5)分析有关数据,写出X、Y、Z的反应方程式______ 。
序号 | 硫酸的体积/mL | 锌的质量/g | 锌的形状 | 温度/℃ | 完全溶于酸的时间/s | 生成硫酸锌的质量/g |
1 | 50.0 | 2.0 | 薄片 | 25 | 100 | |
2 | 50.0 | 2.0 | 颗粒 | 25 | 70 | |
3 | 50.0 | 2.0 | 颗粒 | 35 | 35 | |
4 | 50.0 | 2.0 | 粉末 | 25 | 45 | 5.0 |
5 | 50.0 | 6.0 | 粉末 | 35 | 30 | |
6 | 50.0 | 8.0 | 粉末 | 25 | 16.1 | |
7 | 50.0 | 10.0 | 粉末 | 25 | 16.1 |
(1)化学反应速率本质上是由反应物本身的性质决定的,但外界条件也会影响反应速率的大小。本实验中实验2和实验3表明
(2)我们最好选取实验
(3)若采用与实验1完全相同的条件,但向反应容器中滴加少量硫酸铜溶液,发现反应速率明显加快。原因是
Ⅱ.某温度时,在5L的容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。请通过计算回答下列问题:
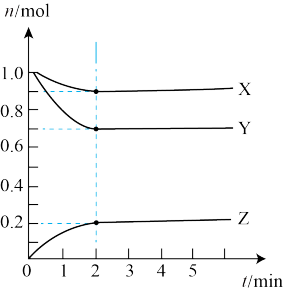
(5)分析有关数据,写出X、Y、Z的反应方程式
23-24高一下·广东韶关·阶段练习
类题推荐
控制变量法是化学实验的一种常用方法。
Ⅰ.下表是某学习小组研究等物质的量浓度的稀硫酸和锌反应的实验数据,分析以下数据,回答下列问题:
(1)判断锌和稀硫酸反应速率大小,最简单的方法可通过测定_______ 进行判断,在此5组实验中,其速率最快的是_______ (填实验序号)。
(2)实验1和2表明_______ 对反应速率有影响,实验1和3对比发现实验3反应速率明显较快,主要原因是_______ 。
(3)进行实验2时,小组同学根据实验过程绘制的氢气体积(标准状况下)与时间的关系如图所示。在OA、AB、BC三段中反应速率最快的是AB段,其原因是_______ 。_______ 。
(5)b点对应的反应速率
_______  。
。
(6)通过以上分析可知选择加入下列哪些试剂可以与加入硫酸铜有相似的效果_______
Ⅰ.下表是某学习小组研究等物质的量浓度的稀硫酸和锌反应的实验数据,分析以下数据,回答下列问题:
| 序号 | 锌的 质量/g | 锌的 形式 | mL | 反应前溶液 的温度/℃ | 其他试剂 | |
| 1 | 0.65 | 粒状 | 0.5 | 50 | 20 | 无 |
| 2 | 0.65 | 粉末 | 0.5 | 50 | 20 | 无 |
| 3 | 0.65 | 粒状 | 0.5 | 50 | 20 | 2滴CuSO4溶液 |
| 4 | 0.65 | 粉末 | 0.8 | 50 | 20 | 无 |
| 5 | 0.65 | 粉末 | 0.8 | 50 | 35 | 2滴CuSO4溶液 |
(2)实验1和2表明
(3)进行实验2时,小组同学根据实验过程绘制的氢气体积(标准状况下)与时间的关系如图所示。在OA、AB、BC三段中反应速率最快的是AB段,其原因是
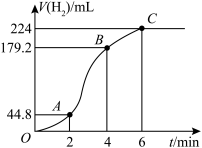
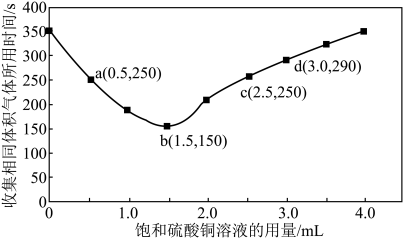
(5)b点对应的反应速率
(6)通过以上分析可知选择加入下列哪些试剂可以与加入硫酸铜有相似的效果_______
| A. | B. | C.稀 | D. |
I.控制变量法是化学实验中的—种常用方法,如表是某课外兴趣小组研究等物质的量浓度的稀硫酸和锌反应的实验数据(计算结果精确到小数点—位),分析以下数据,回答下列问题:
(1)实验①和实验②表明_____ 对反应速率有影响;研究锌的形状对反应速率的影响时,最好选取实验_______ (填3个实验序号)。
(2)下列数据推断正确的是______________________ 。
A. t1<70 B.t1>t4C.m12D.m6=19.3
(3)若采用与实验①完全相同的条件,但向反应窗口中滴加少量硫酸铜溶液,发现反应速率明显加快,原因是___________________________________ 。
(4)根据表中数据计算:硫酸的物质的量浓度是_________________ mol/L。
II.已知在 25℃、l0l kPa 下,2NO(g)+2CO(g) N2(g)+2CO2(g),现将 2molNO、2.4molCO通入恒容密闭容器中,反应过程中部分物质的浓度变化如图所示。
N2(g)+2CO2(g),现将 2molNO、2.4molCO通入恒容密闭容器中,反应过程中部分物质的浓度变化如图所示。
(1) 0〜15min 内,v(CO2) =__________________ 。
(2)该反应的速率时间图象如下图中左图所示。若其他条件不变,仅在反应前加入合适的催化剂,其速率时间图象如下图中右图所示。以下说法正确的是______ (填对应字母)。
A.a1>a2B.b12C.t1>t2
(3) 一定条件下,已知反应NO2(g)+SO2(g) NO(g)+SO3(g),将NO2与SO2以体积比1 :2置于2L密闭容器中发生上述反应,下列能说明该反应达到平衡状态的是
NO(g)+SO3(g),将NO2与SO2以体积比1 :2置于2L密闭容器中发生上述反应,下列能说明该反应达到平衡状态的是_____
a.体系压强保持不变 b.混合气体颜色保持不变
c.NO2与SO2的体积比保持不变 d.每消耗lmol SO2的同时生成lmol NO
序号 | 硫酸的体积 /mL | 锌的质量/g | 锌的形状 | 温度/℃ | 完全溶于酸的 时间/s | 生成硫酸锌的质量/g |
| ① | 50.0 | 2.0 | 薄片 | 15 | 200 | m1 |
| ② | 50.0 | 2.0 | 薄片 | 25 | 100 | m2 |
| ③ | 50.0 | 2.0 | 颗粒 | 25 | 70 | m3 |
| ④ | 50.0 | 2.0 | 颗粒 | 35 | 35 | m4 |
| ⑤ | 50.0 | 2.0 | 粉末 | 25 | t1 | 5.0 |
| ⑥ | 50.0 | 4.0 | 粉末 | 25 | t2 | m5 |
| ⑦ | 50.0 | 6.0 | 粉末 | 25 | t3 | 14.9 |
| ⑧ | 50.0 | 8.0 | 粉末 | 25 | t4 | 19.3 |
| ⑨ | 50.0 | 10.0 | 粉末 | 25 | t5 | 19.3 |
(1)实验①和实验②表明
(2)下列数据推断正确的是
A. t1<70 B.t1>t4C.m12D.m6=19.3
(3)若采用与实验①完全相同的条件,但向反应窗口中滴加少量硫酸铜溶液,发现反应速率明显加快,原因是
(4)根据表中数据计算:硫酸的物质的量浓度是
II.已知在 25℃、l0l kPa 下,2NO(g)+2CO(g)
 N2(g)+2CO2(g),现将 2molNO、2.4molCO通入恒容密闭容器中,反应过程中部分物质的浓度变化如图所示。
N2(g)+2CO2(g),现将 2molNO、2.4molCO通入恒容密闭容器中,反应过程中部分物质的浓度变化如图所示。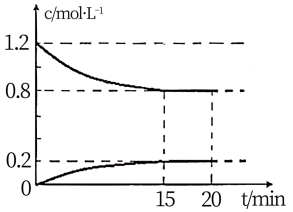
(1) 0〜15min 内,v(CO2) =
(2)该反应的速率时间图象如下图中左图所示。若其他条件不变,仅在反应前加入合适的催化剂,其速率时间图象如下图中右图所示。以下说法正确的是
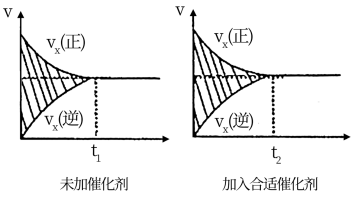
A.a1>a2B.b12C.t1>t2
(3) 一定条件下,已知反应NO2(g)+SO2(g)
 NO(g)+SO3(g),将NO2与SO2以体积比1 :2置于2L密闭容器中发生上述反应,下列能说明该反应达到平衡状态的是
NO(g)+SO3(g),将NO2与SO2以体积比1 :2置于2L密闭容器中发生上述反应,下列能说明该反应达到平衡状态的是a.体系压强保持不变 b.混合气体颜色保持不变
c.NO2与SO2的体积比保持不变 d.每消耗lmol SO2的同时生成lmol NO
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网