填空题 容易0.94 引用1 组卷189
回答下列问题:
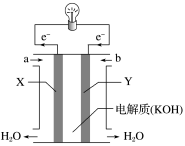
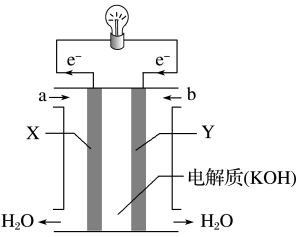
(1)如图为氢氧燃料电池的构造示意图,根据电子运动方向,可知氧气从___________ 口通入(填“a”或“b”),X极为电池的___________ (填“正”或“负”)极,Y极的电极方程式为___________ 。
A极:2H2+2O2--4e-=2H2O
B极:O2+4e-=2O2-
则A极是电池的___________ 极;电子从该极___________ (填“流入”或“流出”)。
(3)微型纽扣电池在现代生活中有广泛应用,有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应为:
Zn+2OH-2e-=ZnO+H2O Ag2O+H2O+2e-=2Ag+2OH-
总反应为Ag2O+Zn=ZnO+2Ag
①Zn是___________ 极,Ag2O发生___________ 反应。
②电子由___________ 极流向___________ 极(填“Zn”或“Ag2O”),当电路通过1 mol电子时,负极消耗物质的质量是___________ g。
③在使用过程中,电解质溶液中KOH的物质的量___________ (填“增大”“减小”或“不变”)。
(1)如图为氢氧燃料电池的构造示意图,根据电子运动方向,可知氧气从
A极:2H2+2O2--4e-=2H2O
B极:O2+4e-=2O2-
则A极是电池的
(3)微型纽扣电池在现代生活中有广泛应用,有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应为:
Zn+2OH-2e-=ZnO+H2O Ag2O+H2O+2e-=2Ag+2OH-
总反应为Ag2O+Zn=ZnO+2Ag
①Zn是
②电子由
③在使用过程中,电解质溶液中KOH的物质的量
22-23高二上·江西南昌·期末
类题推荐
I.在高温、高压、催化剂作用下,1mol石墨转化为金刚石,吸收1.9kJ的热量。
(1)该反应的△H_____ 0(填“大于”或“小于”)。
(2)对于石墨和金刚石,______ 更稳定。
(3)已知几种化学键的键能如表所示:
则反应Cl2(g)+3F2(g) 2ClF3(g)的△H=
2ClF3(g)的△H=____ kJ·mol-1。
II.根据化学能转化电能的相关知识,回答下列问题:
(4)理论上讲,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Cu+2Ag+=2Ag+Cu2+”设计一个化学电池(正极材料用碳棒),回答下列问题:该电池的负极材料是____ ,发生____ (填“氧化”或“还原”)反应。
(5)某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,两极上发生的电极反应分别为A极:2H2+2O2--4e-=2H2O、B极:O2+4e-=2O2-,则A极是电池的____ 极;电子从该极_____ (填“流入”或“流出”)。
(6)微型纽扣电池在现代生活中有广泛应用,有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应为:Zn+2OH--2e-=ZnO+H2O,Ag2O+H2O+2e-=2Ag+2OH-,总反应为Ag2O+Zn=ZnO+2Ag。
①电子由____ 极流向____ 极(填“Zn”或“Ag2O”),当电路通过1mol电子时,负极消耗物质的质量是_____ g。
②在使用过程中,电解质溶液中KOH的物质的量____ (填“增大”“减小”或“不变”)。
(1)该反应的△H
(2)对于石墨和金刚石,
(3)已知几种化学键的键能如表所示:
| 化学键 | Cl-Cl | F-F | Cl-F |
| 键能/kJ·mol-1 | 242 | 159 | 172 |
则反应Cl2(g)+3F2(g)
II.根据化学能转化电能的相关知识,回答下列问题:
(4)理论上讲,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Cu+2Ag+=2Ag+Cu2+”设计一个化学电池(正极材料用碳棒),回答下列问题:该电池的负极材料是
(5)某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,两极上发生的电极反应分别为A极:2H2+2O2--4e-=2H2O、B极:O2+4e-=2O2-,则A极是电池的
(6)微型纽扣电池在现代生活中有广泛应用,有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应为:Zn+2OH--2e-=ZnO+H2O,Ag2O+H2O+2e-=2Ag+2OH-,总反应为Ag2O+Zn=ZnO+2Ag。
①电子由
②在使用过程中,电解质溶液中KOH的物质的量
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网