解答题-实验探究题 适中0.65 引用1 组卷67
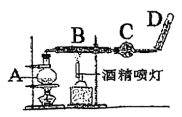
铁是生活中常见的金属,完成"Fe与水蒸气的高温反应实验”。_____ 。
(2)反应的方程式为_____ 。
(3)分析得出B中是铁的氧化物与铁单质,为探究B中反应产物的氧含量,选取5g固体放入硬质试管中,通入足量CO,高温下充分反应,将生成的气体全部通入足量的澄清石灰水中,生成白色沉淀6g。则产物中氧的质量分数为_____ 。
(2)反应的方程式为
(3)分析得出B中是铁的氧化物与铁单质,为探究B中反应产物的氧含量,选取5g固体放入硬质试管中,通入足量CO,高温下充分反应,将生成的气体全部通入足量的澄清石灰水中,生成白色沉淀6g。则产物中氧的质量分数为
23-24高一下·上海奉贤·阶段练习
类题推荐
现有部分短周期元素的性质或原子结构如下表:
(1)四种元素原子半径由大到小的顺序是(写元素符号)_________________________ 。
(2)元素Y与氢元素形成的一种离子YH4+,写出该微粒的电子式________ (用元素符号表示)。
(3)T元素的简单阴离子的结构示意图是______________________ ,
(4)证明该粒子的还原性比Z-强的离子方程式是____________________ .
(5)元素Z的单质与氢氧化钠溶液反应的化学方程式为_______________________ 。
(6)将9g单质X在足量氧气中燃烧,所得气体通入1L 1mol·L-1NaOH溶液中,完全吸收后,将溶液在减压低温条件下蒸干,得到不含结晶水的固体质量为____________ g。
| 元素编号 | 元素性质或原子结构 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| T | 最外层电子数是电子层数的2倍 |
| Z | 元素最高正价是+7价 |
(1)四种元素原子半径由大到小的顺序是(写元素符号)
(2)元素Y与氢元素形成的一种离子YH4+,写出该微粒的电子式
(3)T元素的简单阴离子的结构示意图是
(4)证明该粒子的还原性比Z-强的离子方程式是
(5)元素Z的单质与氢氧化钠溶液反应的化学方程式为
(6)将9g单质X在足量氧气中燃烧,所得气体通入1L 1mol·L-1NaOH溶液中,完全吸收后,将溶液在减压低温条件下蒸干,得到不含结晶水的固体质量为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网