填空题 较易0.85 引用1 组卷56
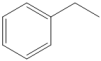 (g)
(g)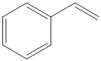 (g)+H2(g)
(g)+H2(g)已知键能数据如图表格:
| 化学键 | ||||
| 键能/ | 412 | 348 | 612 | 436 |
(2)根据上述焓变的计算结果,结合该反应的熵变,以下判断正确的是_____。
| A.高温时反应可以自发进行 |
| B.低温时反应可以自发进行 |
| C.任何温度下反应都可以自发进行 |
| D.任何温度下反应都不可以自发进行 |
23-24高二下·上海·阶段练习
类题推荐
有A、B、C、D四个反应,其焓变和熵变如下表所示
(1)在任何温度都能自发进行的反应是________ ;任何温度下都不能自发进行的反应是________ 。
(2)高温才可以自发进行的反应是________ ;低温有利于自发进行的反应是________ 。
| 反应 | A | B | C | D |
| ΔH/kJ·mol-1 | 10.5 | 1.80 | -126 | -11.7 |
| ΔS/J·mol-l·K-1 | 30.0 | -113.0 | 84.0 | -105.0 |
(2)高温才可以自发进行的反应是
研究表明,在等温、等压及除了体积功以外不做其他功的条件下,化学反应的方向可以用反应的焓变和熵变来综合判断,判据为ΔH-TΔS。任何温度下都能正向自发进行的一项是
| A.CH4(g) = C(s) +2H2(g) ΔH=+74.8 kJ·mol-1 ΔS=+80.7 J·mol-1·K-1 |
| B.C2H2(g)+3H2(g)= 2CH4(g) ΔH=-376.4 kJ·mol-1 ΔS=-220.2J·mol-1·K-1 |
| C.2CO(g)=2C(s,石墨)+O2(g) ΔH=+221.0 kJ·mol-1 ΔS=-178.8J·mol-1·K-1 |
| D.2KClO3(s)=2KCl(s)+3O2(g) ΔH=-78.0 kJ·mol-1 ΔS=+494.4J·mol-1·K-1 |
放热反应可认为是化学反应(体系)将释放的能量传递给了周围的环境,导致环境的熵增加,增加的熵与焓变之间存在关系:△S环境=- 。当△S体系+△S环境>0时,反应能自发进行。已知反应:A(g)+B(g)=C(s) △H=-176kJ·mol-1,△S=-284J·mol-1·K-1,下列说法正确的是
。当△S体系+△S环境>0时,反应能自发进行。已知反应:A(g)+B(g)=C(s) △H=-176kJ·mol-1,△S=-284J·mol-1·K-1,下列说法正确的是
| A.该反应在任意温度下都能自发进行 |
| B.该反应在任意温度下都不能自发进行 |
| C.T=298K时该反应能自发进行 |
| D.T=298K时该反应不能自发进行 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


