解答题-工业流程题 较难0.4 引用1 组卷235
锰在汽车电池、高端装备制造、新材料等领域有广泛应用。利用软锰矿(主要成分为 ,含
,含 等杂质)和黄铁矿(主要成分为
等杂质)和黄铁矿(主要成分为 )联合制备绿矾和高纯
)联合制备绿矾和高纯 ,并用所得
,并用所得 制备
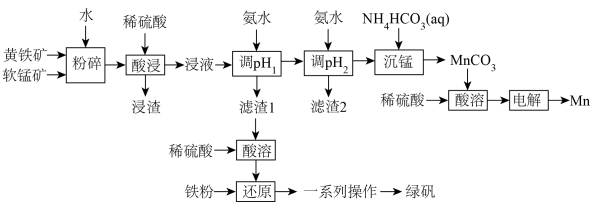
制备 的工艺流程如下:
的工艺流程如下: 如下:
如下:
回答下列问题:
(1)将软锰矿和黄铁矿“粉碎”,并用水调至糊状的目的是______ 。“浸渣”中除了含有不溶于酸的杂质外,还含有生成的单质 ,则“酸浸”时发生的主要反应的离子方程式为
,则“酸浸”时发生的主要反应的离子方程式为______ 。
(2)常温下, 的溶度积
的溶度积
______ 。“调 ”的范围为
”的范围为______ 。
(3)“沉锰”时,溶液的 、反应时间与
、反应时间与 的产率的关系如图1所示。“沉锰”时,应调节溶液的
的产率的关系如图1所示。“沉锰”时,应调节溶液的 为
为______ 。“沉锰”反应的离子方程式为______ 。______ 。
(5)“电解”制取金属锰的化学方程式为______ 。
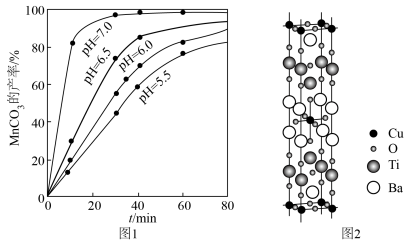
(6)铜、钛和锰、铁都是第四周期的过渡元素。一种含 四元铜氧化物超导体晶体的晶胞结构如图2所示(晶胞参数为
四元铜氧化物超导体晶体的晶胞结构如图2所示(晶胞参数为 ),该晶体的密度为
),该晶体的密度为______  (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
| 金属离子 | ||||
| 开始沉淀的 | 8.1 | 6.3 | 1.5 | 3.4 |
| 沉淀完全 | 10.1 | 8.3 | 2.8 | 4.7 |
(1)将软锰矿和黄铁矿“粉碎”,并用水调至糊状的目的是
(2)常温下,
(3)“沉锰”时,溶液的
(5)“电解”制取金属锰的化学方程式为
(6)铜、钛和锰、铁都是第四周期的过渡元素。一种含
23-24高三下·河南·阶段练习
类题推荐
四氧化三锰( )是一种可用于生产锂离子电池正极材料的原料。以天然二氧化锰粉与硫化锰矿(还含
)是一种可用于生产锂离子电池正极材料的原料。以天然二氧化锰粉与硫化锰矿(还含 等元素)为原料制备高纯
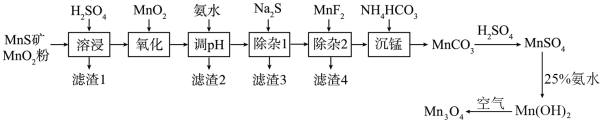
等元素)为原料制备高纯 的工艺流程如下图所示。
的工艺流程如下图所示。 形成氢氧化物沉淀的
形成氢氧化物沉淀的 范围如下表:
范围如下表:
回答下列问题:
(1)“氧化”中添加适量的 的作用是
的作用是___________ 。(用离子方程式表示)
(2)“滤渣2”中主要有___________ ,“调 ”时溶液的
”时溶液的 范围应调节为
范围应调节为___________ ~6.2之间。
(3)“除杂2”的目的是生成 ,沉淀除去
,沉淀除去 。若溶液酸度过高,会导致
。若溶液酸度过高,会导致___________ 。
(4)常温下,利用表格中的数据,计算
___________ 。(已知 )
)
(5) 和氨水混合在
和氨水混合在 下得到的
下得到的 的产率最高。若继续升高温度,会导致产率降低,原因可能是
的产率最高。若继续升高温度,会导致产率降低,原因可能是___________ 。
(6)在“沉锰”时,可用尿素 代替
代替 ,同时控制温度在
,同时控制温度在 ,写出尿素“沉锰”反应的离子方程式:
,写出尿素“沉锰”反应的离子方程式:___________ 。
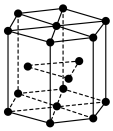
(7)金属 晶体中的原子堆积方式如图所示,六棱柱底边边长为
晶体中的原子堆积方式如图所示,六棱柱底边边长为 ,高为
,高为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,
, 的相对原子质量为M,则
的相对原子质量为M,则 晶体的密度为
晶体的密度为___________  (已知
(已知 ,列出计算式即可)。
,列出计算式即可)。
| 金属离子 | |||||||
| 开始沉淀的 | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 | 6.9 |
| 沉淀完全的 | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.2 | 8.9 |
(1)“氧化”中添加适量的
(2)“滤渣2”中主要有
(3)“除杂2”的目的是生成
(4)常温下,利用表格中的数据,计算
(5)
(6)在“沉锰”时,可用尿素
(7)金属
高品质 可用于生产锂离子电池正极材料锰酸锂。以软锰矿与黄铁矿为主要原料采用“两矿一步浸出法”制备高品质
可用于生产锂离子电池正极材料锰酸锂。以软锰矿与黄铁矿为主要原料采用“两矿一步浸出法”制备高品质 的某工艺流程如图所示:
的某工艺流程如图所示:
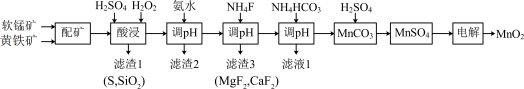
已知:软锰矿与黄铁矿的主要成分为 、
、 ,还含少量
,还含少量 等杂质:
等杂质:
②该工艺条件下,相关金属离子完全形成氢氧化物沉淀的 如下:
如下:
回答下列问题:
(1)“配矿”过程中,将软锰矿与黄铁矿粉碎混匀的目的是___________ 。
(2)“酸浸”操作中需先后分批加入 、
、 。加入
。加入 后发生酸浸过程的主要反应离子方程式为
后发生酸浸过程的主要反应离子方程式为 ,
, 。
。
①已知滤渣1的主要成分为S、 等,其附着在矿粉颗粒表面使上述反应受阻,此时加入
等,其附着在矿粉颗粒表面使上述反应受阻,此时加入 ,利用其迅速分解产生的大量气泡可破除该不利影响,分析导致
,利用其迅速分解产生的大量气泡可破除该不利影响,分析导致 迅速分解的因素是
迅速分解的因素是___________ 。
②矿粉颗粒表面附着物被破除后, 可继续与
可继续与 在酸性条件下反应,产生更多
在酸性条件下反应,产生更多 ,并伴有气体生成,该反应的离子方程式是
,并伴有气体生成,该反应的离子方程式是___________ 。
③ 除上述作用外,还可以将溶液中未与
除上述作用外,还可以将溶液中未与 反应的
反应的 转化为
转化为 ,其目的是:
,其目的是:___________ 。
(3)“调p”时调节溶液 范围为4.7-6.0,此时“滤渣2”的主要成分为
范围为4.7-6.0,此时“滤渣2”的主要成分为___________ (填化学式)。
(4)“沉锰”步骤发生主要反应的离子方程式为___________ 。
(5)“用 除杂”时,溶液体系中的
除杂”时,溶液体系中的 和
和 形成氟化物沉淀。若沉淀后上层清液中
形成氟化物沉淀。若沉淀后上层清液中 ,则
,则
___________ 。( 、
、 )
)

已知:软锰矿与黄铁矿的主要成分为
②该工艺条件下,相关金属离子完全形成氢氧化物沉淀的
| 金属离子 | |||||
| 开始沉淀 | 6.9 | 1.9 | 6.6 | 9.1 | 3.4 |
| 沉淀完全( | 8.3 | 3.2 | 10.1 | 10.9 | 4.7 |
(1)“配矿”过程中,将软锰矿与黄铁矿粉碎混匀的目的是
(2)“酸浸”操作中需先后分批加入
①已知滤渣1的主要成分为S、
②矿粉颗粒表面附着物被破除后,
③
(3)“调p”时调节溶液
(4)“沉锰”步骤发生主要反应的离子方程式为
(5)“用
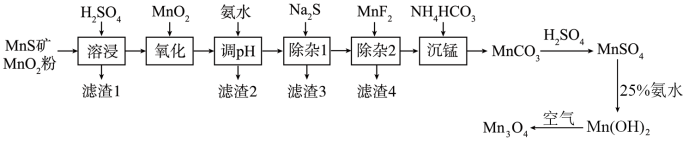
四氧化三锰( )是一种可用于生产锂离子电池正极材料的原料。以天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)为原料制备高纯
)是一种可用于生产锂离子电池正极材料的原料。以天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)为原料制备高纯 的工艺流程如下图所示。
的工艺流程如下图所示。 ]形成氢氧化物沉淀的pH范围如下表:
]形成氢氧化物沉淀的pH范围如下表:
回答下列问题:
(1)“氧化”中添加适量的 的作用是
的作用是___________ (用离子方程式表示)。
(2)“除杂1”的目的是除去 、
、 等杂质离子,则“滤渣3”中主要有
等杂质离子,则“滤渣3”中主要有___________ ,“调pH”时溶液的pH范围应调节为___________ 之间。
(3)“除杂2”的目的是生成 沉淀除去
沉淀除去 ,若溶液酸度过高,会导致
,若溶液酸度过高,会导致___________ 。
(4))常温下,利用表格中的数据,计算
___________ (已知 )。
)。
(5)在“沉锰”时,可用尿素[ ]代替
]代替 ,同时控制温度在115~120℃,写出尿素“沉锰”反应的离子方程式
,同时控制温度在115~120℃,写出尿素“沉锰”反应的离子方程式___________ 。
(6) 和氨水混合在80℃下得到的
和氨水混合在80℃下得到的 的产率最高,若继续升高温度,会导致产率降低,原因可能是
的产率最高,若继续升高温度,会导致产率降低,原因可能是___________ 。
| 金属离子 | |||||||
| 开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 | 6.9 |
| 沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.2 | 8.9 |
(1)“氧化”中添加适量的
(2)“除杂1”的目的是除去
(3)“除杂2”的目的是生成
(4))常温下,利用表格中的数据,计算
(5)在“沉锰”时,可用尿素[
(6)
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


