解答题-原理综合题 适中0.65 引用1 组卷147
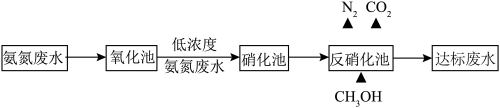
工业废水中的氨氨(以NH3、 形式存在),可通过微生物法或氧化法处理,使水中氨氮达到国家规定的排放标准。
形式存在),可通过微生物法或氧化法处理,使水中氨氮达到国家规定的排放标准。
(1)微生物法:(酸性废水中的部分 在硝化细菌的作用下被氧气氧化为
在硝化细菌的作用下被氧气氧化为 ,
, 作用生成N2。
作用生成N2。
① 转化为
转化为 的离子方程式为
的离子方程式为___________ 。
② 与
与 在转化为N2的反应中消耗
在转化为N2的反应中消耗 与
与 的物质的量之比为
的物质的量之比为___________ 。
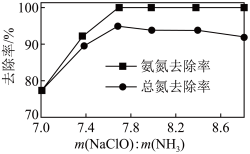
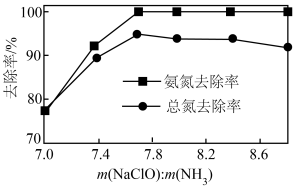
(2)次氯酸钠氧化法:向氨氮废水中加入NaClO,氨氮转化为N2而除去。NaClO氧化NH3的离子方程式为___________ 。
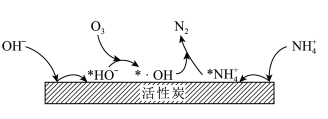
(3)活性炭-臭氧氧化法:活性炭-臭氧氧化氨氮的机理如图所示。*表示吸附在活性炭表面的物种,·OH为羟基自由基,其氧化性比O3更强。

活性炭奥氧氧化氨氮的机理可描述为___________ 。
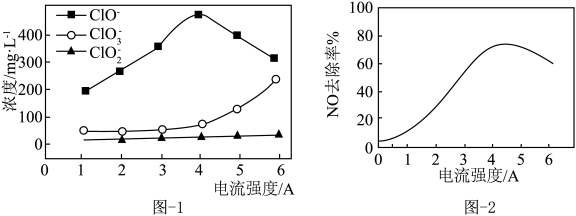
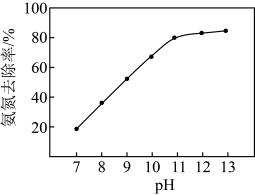
②其它条件不变调节废水的pH,废水中氨氮去除率随pH的变化如题17图-3所示。随pH增大氨氮去除率先明显增大,后变化较小,可能的原因是___________ 。
(1)微生物法:(酸性废水中的部分
①
②
(2)次氯酸钠氧化法:向氨氮废水中加入NaClO,氨氮转化为N2而除去。NaClO氧化NH3的离子方程式为
(3)活性炭-臭氧氧化法:活性炭-臭氧氧化氨氮的机理如图所示。*表示吸附在活性炭表面的物种,·OH为羟基自由基,其氧化性比O3更强。

活性炭奥氧氧化氨氮的机理可描述为
②其它条件不变调节废水的pH,废水中氨氮去除率随pH的变化如题17图-3所示。随pH增大氨氮去除率先明显增大,后变化较小,可能的原因是

23-24高一下·江苏苏州·阶段练习
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网