解答题-结构与性质 较易0.85 引用2 组卷72
明代科学家宋应星在《天工开物》中写道:“凡玉入中国,贵者尽出于田葱岭”。和田玉的主要化学成分是含水的钙镁硅酸盐。回答下列问题:
(1)元素镁能形成很多简单微粒,下面是镁原子形成的微粒的电子排布式,其中再电离出一个电子所需能量最大的是______ (填标号),当从C状态变到B状态,形成的是______ 光谱(选填“发射”或“吸收”)。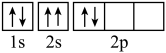 ,该电子排布图违背了
,该电子排布图违背了______ 。
(3)元素钙、镁和氯三种元素形成的最高价氧化物的水化物中,碱性最强的是______ (填化学式,下同),酸性最强的是______ 。
(4) 中中心原子Si的杂化类型是
中中心原子Si的杂化类型是______ ,离子空间结构为______ 。
(5)在 中不存在的化学键类型有
中不存在的化学键类型有______ 。
A.非极性共价键 B.极性共价键 C. 键 D.
键 D. 键
键
碳酸( )的酸性比硅酸(
)的酸性比硅酸( )
)______ (填“强”或“弱”),用离子方程式证明______ 。
(6)羧基( )能电离出
)能电离出 ,使溶液呈现酸性,已知
,使溶液呈现酸性,已知 的酸性小于
的酸性小于 ,则推电子能力较强的是
,则推电子能力较强的是______ (填“ ”或“
”或“ ”)
”)
(1)元素镁能形成很多简单微粒,下面是镁原子形成的微粒的电子排布式,其中再电离出一个电子所需能量最大的是
A. 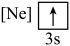 B.
B.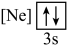 C.
C. 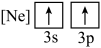 D.
D.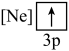
 ,该电子排布图违背了
,该电子排布图违背了(3)元素钙、镁和氯三种元素形成的最高价氧化物的水化物中,碱性最强的是
(4)
(5)在
A.非极性共价键 B.极性共价键 C.
碳酸(
(6)羧基(
23-24高二下·河北张家口·阶段练习
类题推荐
回答下列问题:
(1)Cd与Zn同族且相邻,写出基态Cd原子的价层电子排布式:___________ 。
(2)原子中运动的电子有两种相反的自旋状态,一种自旋状态用 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态Si原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态Si原子,其价电子自旋磁量子数的代数和为___________ 。
(3)O和S处于同一主族,第一电离能较大的是___________ 。 和
和 分子中的键角较大的是
分子中的键角较大的是___________ ,键长较短的是___________ 。单质硫与热的 浓溶液反应的产物之一为
浓溶液反应的产物之一为 ,
, 的空间构型为
的空间构型为___________ 。
(4)已知多个相邻且平行的p轨道重叠则形成大 键,分子中的大
键,分子中的大 键可用符号
键可用符号 表示,其中
表示,其中 代表参与形成大
代表参与形成大 键的原子数,
键的原子数, 代表参与形成大
代表参与形成大 键的电子数(如苯分子的大
键的电子数(如苯分子的大 键可表示为
键可表示为 )。吡咯(
)。吡咯(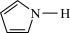 )中所有原子共平面。则吡咯分子中的大
)中所有原子共平面。则吡咯分子中的大 键应表示为
键应表示为___________ 。吡咯分子中N原子的杂化类型为___________ ,1mol吡咯分子中含有___________  键,
键, 噻吩的沸点为84℃,吡咯(
噻吩的沸点为84℃,吡咯(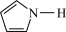 )的沸点在129-131℃之间,吡洛沸点较高,其原因是
)的沸点在129-131℃之间,吡洛沸点较高,其原因是___________ 。
(5)键的极性对物质的化学性质有重要影响。已知一些常见电子基团的吸电子效应的强度: ,则下列物质酸性由强到弱的顺序是___________(填序号)。
,则下列物质酸性由强到弱的顺序是___________(填序号)。
(6) 是离子晶体,其形成过程中的能量变化如图(a)所示。
是离子晶体,其形成过程中的能量变化如图(a)所示。
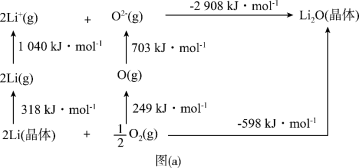
可知,Li原子的第一电离能为_______  ,
, 键键能为
键键能为_______  。
。
(1)Cd与Zn同族且相邻,写出基态Cd原子的价层电子排布式:
(2)原子中运动的电子有两种相反的自旋状态,一种自旋状态用
(3)O和S处于同一主族,第一电离能较大的是
(4)已知多个相邻且平行的p轨道重叠则形成大
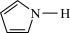 )中所有原子共平面。则吡咯分子中的大
)中所有原子共平面。则吡咯分子中的大 噻吩的沸点为84℃,吡咯(
噻吩的沸点为84℃,吡咯(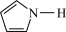 )的沸点在129-131℃之间,吡洛沸点较高,其原因是
)的沸点在129-131℃之间,吡洛沸点较高,其原因是(5)键的极性对物质的化学性质有重要影响。已知一些常见电子基团的吸电子效应的强度:
| A. | B. |
| C. | D. |

可知,Li原子的第一电离能为
A、B、C、D、E、F六种元素的原子序数依次增大,其中A、B、C、D、E为短周期元素,F为第四周期的过渡元素,六种元素的元素性质或原子结构特征如下表:
请回答下列问题:
(1)元素A的核外电子排布式为___________ ;元素F的价层电子的轨道表示式为___________ 。
(2)B的简单气态氢化物的中心原子杂化轨道类型为___________ 。
(3)A、B、C三种元素的电负性由大到小的顺序为___________ (用元素符号回答)。
(4)D的基态原子核外电子的空间运动状态有___________ 种。
(5)下列为E原子核形成的四种微粒,电子排布式分别为:① 、②
、② 、③
、③ 、④
、④ ,电离最外层一个电子所需能量最大的是
,电离最外层一个电子所需能量最大的是___________ (填标号);当E从②状态变到③状态,形成的是___________ 光谱(选填“发射”或“吸收”)。
| 元素 | 元素性质或原子结构特征 |
| A | 原子s轨道电子数是p轨道电子数的2倍 |
| B | 原子p轨道都有电子,且自旋方向相同 |
| C | 原子的价层电子排布是 |
| D | 原子中只有两种形状的电子云,其最外层只有1个电子 |
| E | s轨道与p轨道电子数相同 |
| F | 最外层只有1个电子,次外层内的所有轨道的电子均成对 |
(1)元素A的核外电子排布式为
(2)B的简单气态氢化物的中心原子杂化轨道类型为
(3)A、B、C三种元素的电负性由大到小的顺序为
(4)D的基态原子核外电子的空间运动状态有
(5)下列为E原子核形成的四种微粒,电子排布式分别为:①
Ⅰ.单选题
(1) 溶液中通入适量
溶液中通入适量 ,反应的离子方程式为
,反应的离子方程式为 。下列各离子的电子排布式正确的是
。下列各离子的电子排布式正确的是
(2)下列各组比较中,正确的是
(3)已知 的结构为
的结构为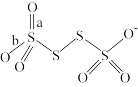 ,下列叙述不正确的是
,下列叙述不正确的是
Ⅱ.非选择题
结构决定性质,研究元素及物质的结构和性质是化学工作者永恒的课题。
(4) 原子核外共有
原子核外共有___________ 种运动状态不同的电子,其基态原子的电子排布式为___________ ,最高能层电子的电子云轮廓形状为___________ 。
(5)我国科学家屠呦呦以研究“青蒿素”获诺贝尔奖。青蒿素的结构简式如图所示,其组成元素的电负性由大到小的顺序为___________ 。
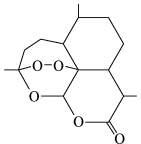
(6)已知,可用异氰酸苯酯与 氯
氯 氨基吡啶反应生成氯吡苯脲:
氨基吡啶反应生成氯吡苯脲:
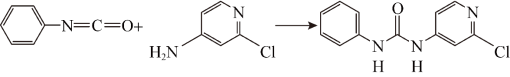
反应过程中,每生成 氯吡苯脲,断裂
氯吡苯脲,断裂___________  键,断裂
键,断裂___________  键。
键。
(7)计算: 的中心原子上的孤电子对数分别是
的中心原子上的孤电子对数分别是___________ 、___________ 。
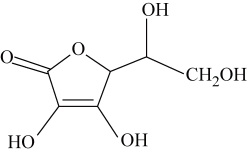
(8)抗坏血酸的分子结构如图所示,分子中碳原子的轨道杂化类型为___________ ;推测抗坏血酸在水中的溶解性:___________ (填“难溶”或“易溶”)于水;坏血酸分子___________ (填“是”或“不是”)手性分子。
(1)
| A. | B. |
| C. | D. |
| A.分子的极性: |
| B. |
| C.钠元素的第一、第二电离能分别小于镁元素的第一、第二电离能 |
| D.在 |
 ,下列叙述不正确的是
,下列叙述不正确的是| A. |
| B. |
| C. |
D.沸点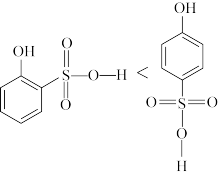 |
Ⅱ.非选择题
结构决定性质,研究元素及物质的结构和性质是化学工作者永恒的课题。
(4)
(5)我国科学家屠呦呦以研究“青蒿素”获诺贝尔奖。青蒿素的结构简式如图所示,其组成元素的电负性由大到小的顺序为
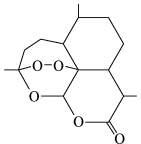
(6)已知,可用异氰酸苯酯与

反应过程中,每生成
(7)计算:
(8)抗坏血酸的分子结构如图所示,分子中碳原子的轨道杂化类型为

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


