解答题-原理综合题 适中0.65 引用1 组卷39
合成气(CO+H2)在煤化工和天然气化工中有着十分重要的地位,由合成气可合成多种有机基础原料和产品。
(1)煤化工中生产合成气的反应为:C(s)+H2O(g) CO(g)+H2(g) ΔH=+131.5kJ·mol-1
CO(g)+H2(g) ΔH=+131.5kJ·mol-1
①判断该反应的自发性条件___________ ;
②在恒温恒容下,同时放入C(s)、H2O(g)、CO(g)、H2(g)四种物质,下列事实能够说明反应C(s)+H2O(g) CO(g)+H2(g)已达到平衡的是
CO(g)+H2(g)已达到平衡的是___________ 。
A.反应体系中,混合气体的密度不再改变
B.反应体系中,各组分的物质的量相等
C.反应体系中,当有2molH—O键断裂的同时有1molH—H键断裂
D.混合气体的平均相对分子质量保持不变
(2)天然气化工中生产合成气的主要反应为:2CH4(g)+O2(g) 2CO(g)+4H2(g) ΔH=akJ·mol-1,在恒容容器中按物质的量之比1︰2加入一定量的CH4和O2,在压强为1.01×105Pa、不同温度下测得CH4的平衡转化率如图所示:
2CO(g)+4H2(g) ΔH=akJ·mol-1,在恒容容器中按物质的量之比1︰2加入一定量的CH4和O2,在压强为1.01×105Pa、不同温度下测得CH4的平衡转化率如图所示:
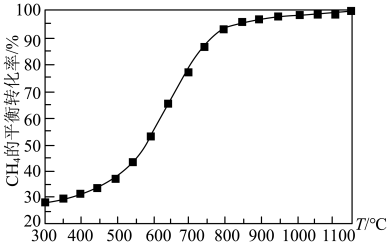
①请在图中画出压强为5.05×105Pa时CH4的平衡转化率随温度的变化曲线________ 。
②现有实验测得反应2CH4(g)+O2(g) 2CO(g)+4H2(g)在750℃下,以不同碳氧比[n(CH4)/n(O2)]投料时反应达平衡后CH4的转化率及H2、CO的选择性,所测数据如表所示。(已知:选择性=目标产物的产率/反应原料的转化率)
2CO(g)+4H2(g)在750℃下,以不同碳氧比[n(CH4)/n(O2)]投料时反应达平衡后CH4的转化率及H2、CO的选择性,所测数据如表所示。(已知:选择性=目标产物的产率/反应原料的转化率)
最佳碳氧比[n(CH4)/n(O2)]为___________ 。
(1)煤化工中生产合成气的反应为:C(s)+H2O(g)
①判断该反应的自发性条件
②在恒温恒容下,同时放入C(s)、H2O(g)、CO(g)、H2(g)四种物质,下列事实能够说明反应C(s)+H2O(g)
A.反应体系中,混合气体的密度不再改变
B.反应体系中,各组分的物质的量相等
C.反应体系中,当有2molH—O键断裂的同时有1molH—H键断裂
D.混合气体的平均相对分子质量保持不变
(2)天然气化工中生产合成气的主要反应为:2CH4(g)+O2(g)

①请在图中画出压强为5.05×105Pa时CH4的平衡转化率随温度的变化曲线
②现有实验测得反应2CH4(g)+O2(g)
| 碳氧比[n(CH4)/n(O2)] | 1︰0.25 | 1︰0.5 | 1︰1 | 1︰1.25 |
| CH4转化率 | 0.40 | 0.88 | 0.98 | 0.99 |
| H2选择性 | 0.98 | 0.93 | 0.67 | 0.40 |
| CO选择性 | 0.99 | 0.94 | 0.65 | 0.32 |
23-24高二上·浙江杭州·阶段练习
类题推荐
合成气 在煤化工和天然气化工中有着十分重要的地位,由合成气可合成多种有机基础原料和产品。
在煤化工和天然气化工中有着十分重要的地位,由合成气可合成多种有机基础原料和产品。
(1)煤化工中生产合成气的反应为:
①该反应的平衡常数表达式为_______ ,该反应在_______ (填高温或低温)自发进行。
②在恒温恒容下,同时放入 四种物质,下列事实能够说明反应
四种物质,下列事实能够说明反应 已达到平衡的是
已达到平衡的是_______ 。
A.反应体系中,混合气体的密度不再改变
B.反应体系中, 和
和 的体积分数相等
的体积分数相等
C.反应体系中,当有 键断裂的同时有
键断裂的同时有 键形成
键形成
D.混合气体的平均相对分子质量保持不变
(2)天然气化工中生产合成气的主要反应为: ,在恒容容器中按物质的量之比
,在恒容容器中按物质的量之比 加入一定量的
加入一定量的 和
和 ,在压强为
,在压强为 、不同温度下测得
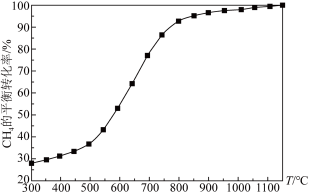
、不同温度下测得 的平衡转化率如下图所示:
的平衡转化率如下图所示: 时
时 的平衡转化率随温度的变化曲线
的平衡转化率随温度的变化曲线______ 。
②现有实验测得反应: 在
在 下,以不同碳氧比
下,以不同碳氧比 投料时反应,达平衡后
投料时反应,达平衡后 的转化率及
的转化率及 的选择性,所测数据如表所示。(已知:选择性=
的选择性,所测数据如表所示。(已知:选择性= )
)
最佳碳氧比 为
为_______ 。假设按碳氧比 =1∶1投料,反应容器的体积为
=1∶1投料,反应容器的体积为 ,通入
,通入 和
和 各
各 ,请列式表示平衡时容器内
,请列式表示平衡时容器内 的浓度
的浓度______ (用a、V的代数式表示)
(3)煤化工可以制取甲醇,甲醇-空气燃料电池,以 溶液为电解质溶液,(电极材料为惰性电极),当
溶液为电解质溶液,(电极材料为惰性电极),当 全部转化为
全部转化为 ,停止放电,写出负极的电极反应式
,停止放电,写出负极的电极反应式_______
(1)煤化工中生产合成气的反应为:
①该反应的平衡常数表达式为
②在恒温恒容下,同时放入
A.反应体系中,混合气体的密度不再改变
B.反应体系中,
C.反应体系中,当有
D.混合气体的平均相对分子质量保持不变
(2)天然气化工中生产合成气的主要反应为:
②现有实验测得反应:
| 碳氧比 | ||||
| 0.40 | 0.88 | 0.98 | 0.99 | |
| 0.98 | 0.93 | 0.67 | 0.40 | |
| 0.99 | 0.94 | 0.65 | 0.32 |
(3)煤化工可以制取甲醇,甲醇-空气燃料电池,以
完成下列问题。
(1)煤化工可以制取甲醇,甲醇﹣空气燃料电池,以KOH溶液为电解质溶液(电极材料为惰性电极),当KOH全部转化为KHCO3,停止放电,写出负极的电极反应式__________ 。
(2)煤化工中生产合成气的反应为:
 。
。
①该反应在_______ (填高温或低温)自发进行。
②在恒温恒容下,同时放入 四种物质,下列事实能够说明反应
四种物质,下列事实能够说明反应
 已达到平衡的是
已达到平衡的是____ 。
A.反应体系中,混合气体的密度不再改变
B.反应体系中,CO和H2的体积分数相等
C.反应体系中,当有2mol H−O键断裂的同时有1mol H−H键形成
D.混合气体的平均相对分子质量保持不变
(3)下列事实可以证明尿酸 是弱电解质的是___________(填字母)。
是弱电解质的是___________(填字母)。
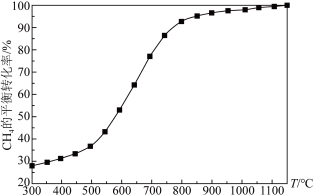
(4)天然气化工中生产合成气的主要反应为:2CH4(g)+O2(g)⇌2CO(g)+4H2(g)ΔH=akJ•mol-1。在恒容容器中按物质的量之比1:2加入一定量的CH4和O2,在压强为1.01×105Pa、不同温度下测得CH4的平衡转化率如图所示,请在图中画出压强为5.05×105Pa时CH4的平衡转化率随温度的变化曲线___________ 。
(1)煤化工可以制取甲醇,甲醇﹣空气燃料电池,以KOH溶液为电解质溶液(电极材料为惰性电极),当KOH全部转化为KHCO3,停止放电,写出负极的电极反应式
(2)煤化工中生产合成气的反应为:
①该反应在
②在恒温恒容下,同时放入
A.反应体系中,混合气体的密度不再改变
B.反应体系中,CO和H2的体积分数相等
C.反应体系中,当有2mol H−O键断裂的同时有1mol H−H键形成
D.混合气体的平均相对分子质量保持不变
(3)下列事实可以证明尿酸
| A. |
| B. |
| C. |
| D. |
(4)天然气化工中生产合成气的主要反应为:2CH4(g)+O2(g)⇌2CO(g)+4H2(g)ΔH=akJ•mol-1。在恒容容器中按物质的量之比1:2加入一定量的CH4和O2,在压强为1.01×105Pa、不同温度下测得CH4的平衡转化率如图所示,请在图中画出压强为5.05×105Pa时CH4的平衡转化率随温度的变化曲线

合成气(CO+H2)是制备合成油和烯烃等众多化工产品的枢纽原料,而催化甲烷部分氧化是生产合成气的主要工艺之一,涉及的反应为:
①2CH4(g)+O2(g) 2CO(g)+4H2(g) △H
2CO(g)+4H2(g) △H
已知如下反应:
②CH4(g)+2O2(g) CO2(g)+2H2O(g) △H1=-810kJ/mol
CO2(g)+2H2O(g) △H1=-810kJ/mol
③CH4(g)+H2O(g) CO(g)+3H2(g) △H2=+225kJ/mol
CO(g)+3H2(g) △H2=+225kJ/mol
④CO(g)+H2O(g) CO2(g)+H2(g) △H3=-35kJ/mol
CO2(g)+H2(g) △H3=-35kJ/mol
请回答下列问题:
(1)试计算反应①的△H=___ 。
(2)在某体积固定的绝热密闭容器中发生反应④,下列事实能证明反应已达平衡的是___ 。
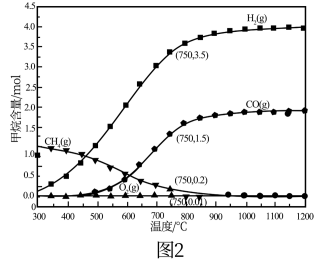
(3)在某恒容密闭容器中加入一定量的甲烷和氧气发生反应③,使其充分反应,测得不同温度和压强下甲烷的转化率如图1所示,由该图可得出的结论是___ 。

(4)现将2molCH4和1molO2加入某体积可变的密闭容器中,发生反应①。控制压强为1atm,测得不同温度下反应体系中各组分平衡含量如图2所示。实际生产中控制的温度为750℃,则此温度下CO的产率为___ ,若平衡时容器的体积为VL,则该反应的平衡常数K=___ 。(用含V代数式表示,不必化简)。
①2CH4(g)+O2(g)
已知如下反应:
②CH4(g)+2O2(g)
③CH4(g)+H2O(g)
④CO(g)+H2O(g)
请回答下列问题:
(1)试计算反应①的△H=
(2)在某体积固定的绝热密闭容器中发生反应④,下列事实能证明反应已达平衡的是
| A.容器内温度不再变化 | B.混合气体的平均分子量不再变化 |
| C.各组分的物质的量相等 | D.1molH—O键断裂同时有1molH—H键断裂 |

(4)现将2molCH4和1molO2加入某体积可变的密闭容器中,发生反应①。控制压强为1atm,测得不同温度下反应体系中各组分平衡含量如图2所示。实际生产中控制的温度为750℃,则此温度下CO的产率为

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


