解答题-工业流程题 适中0.65 引用1 组卷130
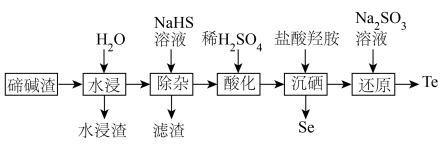
硒、碲广泛应用于传感、光学器件、红外探测等领域。以下是利用碲碱渣(主要含Na2TeO3、Na2SeO3,还有微量的Cu2+、Pb2+及部分不溶性杂质)为原料分离硒、回收碲的流程图:
已知:① 时溶度积常数:
时溶度积常数:
②当c(Mn+)≤1.0×10-5mol/L时认为 离子已经沉淀完全
离子已经沉淀完全
③盐酸羟胺(NH2OH·HCl)是一种还原剂,其氧化产物是
回答下列问题:
(1)基态硒原子的价电子排布式为___________ , 的中心原子的孤电子对数为
的中心原子的孤电子对数为___________ 。
(2)当 完全沉淀时,
完全沉淀时, 的浓度≤
的浓度≤___________ mol/L。
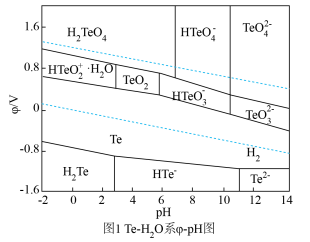
(3)下图是Te—H2O系电位( )—pH图,“酸化”步骤中,当pH为5时,在体系中Te(Ⅳ)主要以
)—pH图,“酸化”步骤中,当pH为5时,在体系中Te(Ⅳ)主要以___________ 形式存在,Te(Ⅳ)可被氧化形成相应的高价Te(Ⅵ)离子,氧化电位随pH值的变化规律为___________ 。
(4)“沉硒”步骤中加入盐酸羟胺,反应的化学方程式为___________ 。
(5)工业上可用电解法制备高纯碲,同时回收工业造纸废液中的NaOH,工作原理如图所示,装置中采用___________ 离子交换膜(填“阳”或“阴”),写出B电极的电极反应式___________ ,若电解8小时,获得1.28吨高纯碲,则电流强度I=___________ C·h-1(已知:一个电子的电荷量e=1.6×10-19C,用含NA的式子表示)。


已知:①
②当c(Mn+)≤1.0×10-5mol/L时认为
③盐酸羟胺(NH2OH·HCl)是一种还原剂,其氧化产物是
回答下列问题:
(1)基态硒原子的价电子排布式为
(2)当
(3)下图是Te—H2O系电位(

(4)“沉硒”步骤中加入盐酸羟胺,反应的化学方程式为
(5)工业上可用电解法制备高纯碲,同时回收工业造纸废液中的NaOH,工作原理如图所示,装置中采用

2024·云南·二模
类题推荐
钪(Sc)是一种稀有金属。从铝土矿生产 的副产品“赤泥”(主要成分为
的副产品“赤泥”(主要成分为 、
、 、
、 、
、 )中回收钪、同时生产聚合硫酸铁铝具有极其重要的工业价值,一种生产工艺流程如图所示:
)中回收钪、同时生产聚合硫酸铁铝具有极其重要的工业价值,一种生产工艺流程如图所示:

已知:①钪离子可以在不同pH下生成
②该工艺条件下,溶液中相关离子开始沉淀和完全沉淀的pH值如下表所示:
回答下列问题:
(1)写出基态Sc原子的核外电子排布式:_______ 。
(2)流程中经处理后可循环利用的物质是_______ (填“物质A”或“物质B”);物质C最好选用_______ (填“NaOH溶液”或“氨水”)。
(3)Sc、Ti、Fe、Al的萃取率与浸出液的酸度关系如图所示,应选择的合适的 浓度为
浓度为_______ mol/L。

(4)“反萃取”时若加入过量的NaOH溶液, 沉淀会溶解。写出
沉淀会溶解。写出 与过量NaOH溶液反应生成
与过量NaOH溶液反应生成 含钪产物的化学方程式:
含钪产物的化学方程式:_______ 。
(5)该工艺流程中引入“还原”与“氧化”这两个步骤的原因是_______ 。
(6)“聚合”生成聚合硫酸铁铝 时,同时产生气体和沉淀,该步骤的离子方程式为
时,同时产生气体和沉淀,该步骤的离子方程式为_______ 。

已知:①钪离子可以在不同pH下生成
②该工艺条件下,溶液中相关离子开始沉淀和完全沉淀的pH值如下表所示:
| 离子 | ||||
| 开始沉淀的pH | 7.0 | 1.9 | 3.0 | 0.3 |
| 完全沉淀的pH | 9.0 | 3.2 | 4.7 | 2.0 |
回答下列问题:
(1)写出基态Sc原子的核外电子排布式:
(2)流程中经处理后可循环利用的物质是
(3)Sc、Ti、Fe、Al的萃取率与浸出液的酸度关系如图所示,应选择的合适的

(4)“反萃取”时若加入过量的NaOH溶液,
(5)该工艺流程中引入“还原”与“氧化”这两个步骤的原因是
(6)“聚合”生成聚合硫酸铁铝
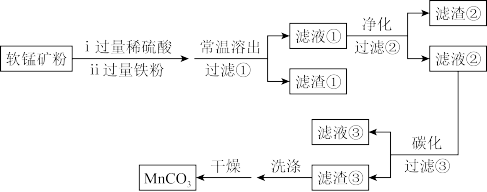
现代工业生产中,MnCO3的用途广泛,是制造电信器材软磁铁氧体、合成MnO2和制造其他锰盐的原料,还可用作脱硫的催化剂,瓷釉、涂料、清漆的颜料等。一种用软锰矿(主要成分为MnO2,主要杂质为Al2O3和SiO2)为原料制备高纯MnCO3的工艺流程如下:
已知:①常温下,MnO2与稀硫酸不反应;
②常温下,相关物质的Ksp数据如下表:
回答下列问题:
(1)将软锰矿预先粉碎的目的是___________ 。
(2)常温溶出时,Fe的氧化过程及得到Mn2+的主要途径如图所示:
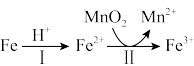
该过程中,步骤II发生反应的离子方程式为___________ 。 滤渣①的成分为___________ (用化学式表示)。
(3)净化过程中,先加H2O2, 再加入氨水调节滤液的pH值。加入H2O2的目的是___________ ,调节滤液pH值的理论最小值为___________ (已知:常温下,当溶液中某离子浓度c≤1.0 ×10-5 mol·L-1时, 可认为该离子沉淀完全)。当净化后所得滤液②的pH值为5时,将含Mn2+的滤液经电解可得MnO2,则生成MnO2的电极反应式为___________ 。
(4)碳化过程中,加入有NH4HCO3和氨水。该步骤的温度不宜过高,其原因是___________ 。
(5)如何证明滤渣③已经洗涤干净___________ 。

已知:①常温下,MnO2与稀硫酸不反应;
②常温下,相关物质的Ksp数据如下表:
| 物质 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Mn(OH)2 |
| Ksp | 1×10-16.3 | 1 ×10-38.6 | 1 ×10-32.3 | 1 ×10-12.7 |
回答下列问题:
(1)将软锰矿预先粉碎的目的是
(2)常温溶出时,Fe的氧化过程及得到Mn2+的主要途径如图所示:
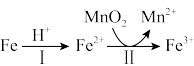
该过程中,步骤II发生反应的离子方程式为
(3)净化过程中,先加H2O2, 再加入氨水调节滤液的pH值。加入H2O2的目的是
(4)碳化过程中,加入有NH4HCO3和氨水。该步骤的温度不宜过高,其原因是
(5)如何证明滤渣③已经洗涤干净
工业上以高硫锰矿与氧化锰矿(还含Si、 Fe、 Al、 Mg、Ni等元素)为原料制备硫酸锰的工艺流程如下图所示:

已知:①部分金属离子形成氢氧化物沉淀时离子的平衡浓度与pH的关系如图所示:

②部分物质的Ksp如下表:
③当溶液中某离子浓度c≤1×10−5mol∙L−1时,可认为该离子沉淀完全。
回答下列问题:
(1)滤渣1的主要成分为S和___________ ,“ 氧化”步骤发生反应的离子方程式为___________ 。
(2)“调 pH” 前检验滤液中是否含Fe2+所用的试剂是___________ , 滤渣2的主要成分为___________ (填化学式)。
(3)已知在“硫化”条件下,溶液中c(S2−)和pH的关系为pH= lgc(S2−)+ 10.5。为使杂质离子沉淀完全,应控制溶液的pH不小于
lgc(S2−)+ 10.5。为使杂质离子沉淀完全,应控制溶液的pH不小于___________ 。
(4)“氟化” 时,若使溶液中的Mg2+和Ca2+沉淀完全,需维持c(F-)不低于___________ mol∙L−1。若溶液酸度过高,Ca2+和 Mg2+沉淀不完全,原因是___________ 。反应MgF2(s)+Ca2+(aq)  CaF2(s)+Mg2+(aq)的平衡常数为
CaF2(s)+Mg2+(aq)的平衡常数为___________ 。
(5)“碳化” 过程中发生反应的离子方程式为___________ 。

已知:①部分金属离子形成氢氧化物沉淀时离子的平衡浓度与pH的关系如图所示:

②部分物质的Ksp如下表:
| 物质 | MnS | FeS | NiS | MgF2 | CaF2 |
| Ksp | 1 ×10−9.6 | 1 ×10−17.2 | 1 ×10−24.0 | 1 ×10−10.2 | 1 ×10−8.2 |
回答下列问题:
(1)滤渣1的主要成分为S和
(2)“调 pH” 前检验滤液中是否含Fe2+所用的试剂是
(3)已知在“硫化”条件下,溶液中c(S2−)和pH的关系为pH=
(4)“氟化” 时,若使溶液中的Mg2+和Ca2+沉淀完全,需维持c(F-)不低于
(5)“碳化” 过程中发生反应的离子方程式为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


