单选题 适中0.65 引用1 组卷40
在V2O5催化下,SO2(g)氧化为SO3(g)的热化学方程式为

 ,研究表明,该反应分两步进行,历程如下:第一步:
,研究表明,该反应分两步进行,历程如下:第一步: (快),第二步:
(快),第二步: (慢)。下列说法错误的是
(慢)。下列说法错误的是
| A.V2O5参与了化学反应 |
| B.总反应中逆反应的活化能比正反应的活化能大 |
| C.第一步的逆反应速率小于第二步的正反应速率 |
| D.提高第二步的反应速率,可提高整个反应的反应速率 |
23-24高三上·河南·阶段练习
类题推荐
已知 ,正反应的活化能为
,正反应的活化能为 ,该反应历程为:
,该反应历程为:
第一步:
 (快反应)
(快反应)
第二步:
 (慢反应)
(慢反应)
下列有关该反应的说法正确的是
第一步:
第二步:
下列有关该反应的说法正确的是
| A.NO比 | B.该化学反应的速率主要由第一步决定 |
| C. | D.该反应的逆反应的活化能大于 |
NO氧化反应: 分两步进行:I.
分两步进行:I.
 ;II.
;II.
 。其反应过程中的能量变化如图所示。
。其反应过程中的能量变化如图所示。
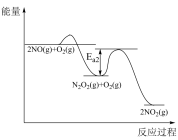
下列说法错误的是

下列说法错误的是
| A.两步反应的 |
| B.决定NO氧化反应速率的是步骤I |
| C.增大压强可以使该反应的速率加快 |
| D.第一步的逆反应活化能比第二步逆反应的活化能小 |
碘蒸气的存在能大幅度提高N2O的分解速率,反应历程为:
第一步I2(g) 2I(g)(快速平衡)
2I(g)(快速平衡)
第二步I(g)+N2O(g)→N2(g)+IO(g)(慢反应)
第三步IO(g)+N2O(g)→N2(g)+O2(g)+I2(g)(快反应)
下列说法错误 的是( )
第一步I2(g)
第二步I(g)+N2O(g)→N2(g)+IO(g)(慢反应)
第三步IO(g)+N2O(g)→N2(g)+O2(g)+I2(g)(快反应)
下列说法
| A.升高温度,第一步向右进行的程度变大 |
| B.第二步的活化能大于第三步的活化能 |
| C.总反应为2N2O |
| D.c[IO(g)]对总反应速率的影响大于c[I(g)] |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


