解答题-原理综合题 适中0.65 引用1 组卷183
现代社会中,人类的一切活动都离不开能量。氢能是一种极具发展潜力的清洁能源。
Ⅰ.已知太阳光分解水制氢气的热化学方程式:
 kJ⋅mol
kJ⋅mol 。
。
(1)反应中主要能量转化形式为____ 能转化为____ 能。
(2)若在反应中使用催化剂,
______ 。(请填写“增大”“减小”或“不变”)
Ⅱ.甲烷、水蒸气催化重整是制备高纯氢的方法之一,反应为: 。一定温度下,向体积为1 L的恒容密闭容器中充入1 mol
。一定温度下,向体积为1 L的恒容密闭容器中充入1 mol  和2 mol
和2 mol ,反应过程中测得
,反应过程中测得 的浓度与反应时间的关系如下表所示:
的浓度与反应时间的关系如下表所示:
(3)101 kPa时,1 mol  气体完全燃烧生成液态水和
气体完全燃烧生成液态水和 气体,放出890.3 kJ的热量,反应的热化学方程式为
气体,放出890.3 kJ的热量,反应的热化学方程式为______ 。
(4)①0~4s时间段内用 表示该反应速率
表示该反应速率
_____ mol⋅L ⋅S
⋅S ,反应到5s时,
,反应到5s时, 的转化率为
的转化率为_____ 。
②下列能判断该反应已经达到化学平衡状态的是_____ 。(填字母)
A. 的浓度不再变化 B.生成1 mol
的浓度不再变化 B.生成1 mol  的同时消耗2 mol
的同时消耗2 mol 
C.容器内气体的密度不再发生变化 D.容器内气体的平均摩尔质量不再发生变化
Ⅰ.已知太阳光分解水制氢气的热化学方程式:
(1)反应中主要能量转化形式为
(2)若在反应中使用催化剂,
Ⅱ.甲烷、水蒸气催化重整是制备高纯氢的方法之一,反应为:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| 0.00 | 0.05 | 0.09 | 0.12 | 0.14 | 0.15 |
(4)①0~4s时间段内用
②下列能判断该反应已经达到化学平衡状态的是
A.
C.容器内气体的密度不再发生变化 D.容器内气体的平均摩尔质量不再发生变化
23-24高一下·河北邯郸·阶段练习
类题推荐
氢能是一种极具发展潜力的清洁能源。
(1)已知1 mol H2完全燃烧生成H2O(g)放出245 kJ能量。该反应的热化学方程式为: △H=
△H=_______ kJ·mol
(2)甲烷、水蒸气催化重整是制备高纯氢的方法之一,反应为: 。一定温度下,向体积为1 L的恒容密闭容器中充入1 mol CH4(g)和2 mol H2O(g),反应过程中测得CO2的浓度与反应时间的关系如下表所示:
。一定温度下,向体积为1 L的恒容密闭容器中充入1 mol CH4(g)和2 mol H2O(g),反应过程中测得CO2的浓度与反应时间的关系如下表所示:
①0〜4s时间段内用H2表示该反应的速率v(H2)=_______ mol·L-1·s-1,反应到5 s时,CH4的转化率为_______ 。
②下列措施可以使该反应速率加快的是_______ 。(填字母)
A.升高温度 B.减小甲烷的浓度 C.使用合适的催化剂
③下列能判断该反应已经达到化学平衡状态的是_______ 。(填字母)
A.CH4的浓度不再变化
B.生成2 mol CO2的同时生成1 mol H2O
C.容器内气体的密度不再发生变化
(3)某氢氧燃料电池已经成功应用在城市公交汽车上,其原理如图所示。工作时的总反应为: ,正极的电极反应式为
,正极的电极反应式为_______ 。
(1)已知1 mol H2完全燃烧生成H2O(g)放出245 kJ能量。该反应的热化学方程式为:
(2)甲烷、水蒸气催化重整是制备高纯氢的方法之一,反应为:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| 0.0 | 5.0 | 9.0 | 12.0 | 14.0 | 15.0 |
②下列措施可以使该反应速率加快的是
A.升高温度 B.减小甲烷的浓度 C.使用合适的催化剂
③下列能判断该反应已经达到化学平衡状态的是
A.CH4的浓度不再变化
B.生成2 mol CO2的同时生成1 mol H2O
C.容器内气体的密度不再发生变化
(3)某氢氧燃料电池已经成功应用在城市公交汽车上,其原理如图所示。工作时的总反应为:
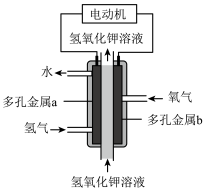
氢能是一种极具发展潜力的清洁能源。
(1)已知 燃烧生成
燃烧生成 放出
放出 能量。该反应的热化学方程式为:
能量。该反应的热化学方程式为:
_______  。
。
(2)甲烷、水蒸气催化重整是制备高纯氢的方法之一,反应为: 。一定温度下,向体积为
。一定温度下,向体积为 的恒容密闭容器中充入
的恒容密闭容器中充入
 和
和 ,反应过程中测得
,反应过程中测得 的浓度与反应时间的关系如下表所示:
的浓度与反应时间的关系如下表所示:
① 时间段内用
时间段内用 表示该反应的速率
表示该反应的速率
_______  ,反应到
,反应到 时,
时, 的转化率为
的转化率为_______ 。
②下列措施可以使该反应速率加快的是_______ 。(填字母)
A.升高温度 B.减小甲烷的浓度 C.使用合适的催化剂
③下列能判断该反应已经达到化学平衡状态的是_______ 。(填字母)
A. 的浓度不再变化
的浓度不再变化
B.生成 的同时生成
的同时生成
C.容器内气体的密度不再发生变化
(3)某氢氧燃料电池已经成功应用在城市公交汽车上,其原理如下图所示。工作时的总反应为: ,负极的电极反应式为
,负极的电极反应式为_______ 。
(1)已知
(2)甲烷、水蒸气催化重整是制备高纯氢的方法之一,反应为:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| 0.0 | 0.05 | 0.09 | 0.12 | 0.14 | 0.15 |
②下列措施可以使该反应速率加快的是
A.升高温度 B.减小甲烷的浓度 C.使用合适的催化剂
③下列能判断该反应已经达到化学平衡状态的是
A.
B.生成
C.容器内气体的密度不再发生变化
(3)某氢氧燃料电池已经成功应用在城市公交汽车上,其原理如下图所示。工作时的总反应为:

2022年北京冬奥会是第一届实现碳中和的冬奥会,氢能作为绿色能源在北京冬奥会中广泛使用,请回答下列问题。
(1)奥运火炬“飞扬”使用氢气作为燃料,氢气不仅是最清洁环保的燃料,而且热值高。已知断裂 相应化学键需要的能量如下:
相应化学键需要的能量如下:
 与
与 反应生成
反应生成
_______ (填吸收或放出)热量_______ kJ。
(2)北京冬奥会大量使用氢燃料电池车,实现了绿色出行。氢燃料电池的工作原理如图所示。
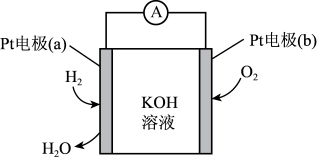
①离子导体中, 向
向 电极
电极_______ (填“a”或“b”)移动。
②写出 电极(a)上的电极反应式
电极(a)上的电极反应式_______ 。
(3)高纯氢的制备是目前的研究热点。甲烷水蒸气催化重整是制高纯氢的方法之一,反应的化学方程式为: 。一定温度下,向体积为2L的恒容密闭容器中充入
。一定温度下,向体积为2L的恒容密闭容器中充入 和
和 ,反应过程中用气体传感器测得不同时间
,反应过程中用气体传感器测得不同时间 的浓度如下表所示:
的浓度如下表所示:
① 时间段内用
时间段内用 表示的该反应的速率
表示的该反应的速率
_______ 。
②为加快反应速率可以采取的措施有_______ (填代号)。
A.使用高效催化剂 B.降低温度
C.保持体积不变充入 D.保持体积不变充入
D.保持体积不变充入
③下列说法能判断该反应已经达到化学平衡状态的是_______ (填代号)。
A.生成 的同时生成
的同时生成
B.混合气体的压强不再发生变化
C. 与
与 的物质的量之比不再发生变化
的物质的量之比不再发生变化
D.混合气体的密度不再发生变化
(1)奥运火炬“飞扬”使用氢气作为燃料,氢气不仅是最清洁环保的燃料,而且热值高。已知断裂
| 化学键 | |||
| 能量 | 436 | 498 | 463 |
(2)北京冬奥会大量使用氢燃料电池车,实现了绿色出行。氢燃料电池的工作原理如图所示。

①离子导体中,
②写出
(3)高纯氢的制备是目前的研究热点。甲烷水蒸气催化重整是制高纯氢的方法之一,反应的化学方程式为:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| 0.0 | 5.0 | 9.0 | 12.0 | 14.0 | 15.0 |
①
②为加快反应速率可以采取的措施有
A.使用高效催化剂 B.降低温度
C.保持体积不变充入
③下列说法能判断该反应已经达到化学平衡状态的是
A.生成
B.混合气体的压强不再发生变化
C.
D.混合气体的密度不再发生变化
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


