解答题-原理综合题 适中0.65 引用1 组卷113
资源利用具有重要意义。
(1)工业上用二氧化碳催化加氢可合成乙醇,其反应原理为
温度 | 400 | 500 |
平衡常数 | 9 | 5.3 |
①通过表格中的数值可以推断:该反应在
②的平衡转化率与氢碳比
及压强随温度变化的关系分别如图
和图
所示。
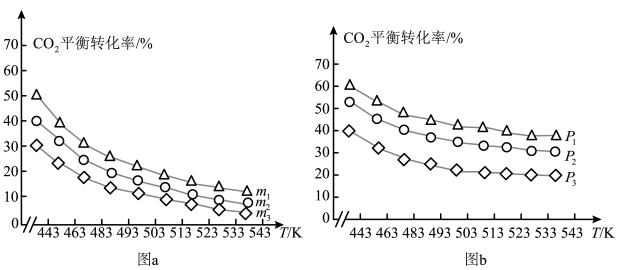
图中氢碳比
从大到小的顺序为
(2)
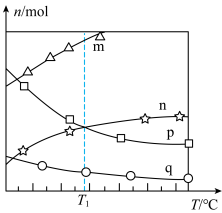
①图中曲线代表乙烯的物质的量随温度的变化关系的是
②℃时,化学平衡常数
的平衡转化率为
(3)
在催化剂作用下,参与反应的机理如图所示
表示乙苯分子中
或
原子的位置; A、B为催化剂的活性位点,其中
位点带部分正电荷,
位点带部分负电荷)。根据元素电负性的变化规律,图中所示的反应机理中步骤I和步骤II可描述为

2024·山西·一模
类题推荐
研究二氧化碳的回收对我国2060年实现碳中和具有现实意义:
(1)已知:①
②
③
写出 与
与 反应生成
反应生成 和
和 的热化学方程式:。
的热化学方程式:。_______ 。
(2)工业上用二氧化碳催化加氢可合成乙醇,其反应原理为:
①通过表格中的数值可以推断:该反应的
_______ 0(填“>”、“<”、或“=”),其正反应在_______ (填“高温”、“低温”或“任何温度”)下能自发进行。
② 的平衡转化率与压强、温度及氢碳比
的平衡转化率与压强、温度及氢碳比 的关系分别如图a和图b所示。
的关系分别如图a和图b所示。
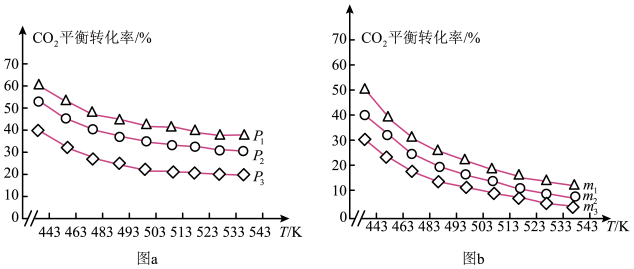
图a中压强从大到小的顺序为_______ ,图b中氢碳比m从大到小的顺序为_______ 。
(3)工业上也可以利用 和
和 合成甲醇:
合成甲醇: 某
某 恒温恒容密闭容器中充入
恒温恒容密闭容器中充入 和
和 发生反应,测得
发生反应,测得 和
和 浓度随时间变化如图所示:
浓度随时间变化如图所示:
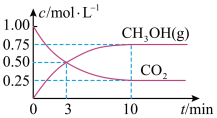
① 内,
内, 的平均反应速率为
的平均反应速率为_______  ,该温度下的平衡常数为
,该温度下的平衡常数为
_______ (单位可忽略)。若达平衡时,保持温度不变,向容器中再充入 和
和 各
各 ,则此时v正
,则此时v正_______ v逆(填“>”、“<”、或“=”)。
②下列说法能说明反应达到化学平衡状态的是_______ 。
A. 的消耗速率与
的消耗速率与 的消耗速率之比为3∶1
的消耗速率之比为3∶1
B.混合气体的密度不变
C.混合气体的平均相对分子质量不变
D. 和
和 的浓度相等时
的浓度相等时
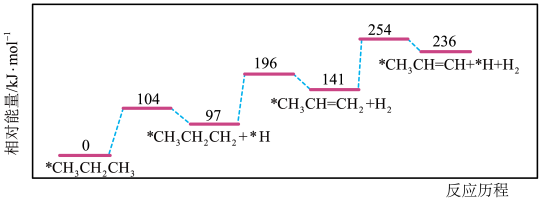
(4)丙烷脱氢是制备丙烯的一种常见方法,下图是某催化剂催化该过程的能量变化,*表示吸附在催化剂表面的物种。下列有关说法正确的是_______。
(1)已知:①
②
③
写出
(2)工业上用二氧化碳催化加氢可合成乙醇,其反应原理为:
| 温度/ | 400 | 500 |
| 平衡常数K | 9 | 5.3 |
①通过表格中的数值可以推断:该反应的
②

图a中压强从大到小的顺序为
(3)工业上也可以利用

①
②下列说法能说明反应达到化学平衡状态的是
A.
B.混合气体的密度不变
C.混合气体的平均相对分子质量不变
D.
(4)丙烷脱氢是制备丙烯的一种常见方法,下图是某催化剂催化该过程的能量变化,*表示吸附在催化剂表面的物种。下列有关说法正确的是_______。

| A. |
| B.在该条件下,所得丙烯中不含其它有机物 |
| C.该过程中发生了碳碳键的断裂与形成 |
| D.相同条件下在该催化剂表面, |
全球大气CO2浓度升高对人类生产生活产生了影响,研究二氧化碳的回收对我国2060年实现碳中和具有现实意义,碳及其化合物的资源化利用成为研究热点。回答下列问题:
(1)已知25℃时,大气中的CO2溶于水存在以下过程:
①CO2(g) CO2(aq)
CO2(aq)
②CO2(aq)+H2O(l) H+(aq)+
H+(aq)+  (aq) K
(aq) K
溶液中CO2的浓度与其在大气中的分压(分压=总压×物质的量分数)成正比,比例系数为ymol•L-1•kPa-1。当大气压强为pkPa,大气中CO2(g)的物质的量分数为x时,溶液中H+的浓度为_____ mol•L-1(忽略 和水的电离)。
和水的电离)。
(2)已知CH4的生成焓(由稳定单质生成该物质)为△H=-71.7kJ•mol-1
反应I:C(s)+H2O(g) CO(g)+H2(g) △H1=+131.3kJ•mol-1 K1
CO(g)+H2(g) △H1=+131.3kJ•mol-1 K1
反应II:C(s)+2H2O(g) CO2(g)+2H2(g) △H2=+90.3kJ•mol-1 K2
CO2(g)+2H2(g) △H2=+90.3kJ•mol-1 K2
反应III:CO(g)+H2O(g) CO2(g)+H2(g) △H3=-41.0kJ•mol-1 K3
CO2(g)+H2(g) △H3=-41.0kJ•mol-1 K3
①写出CO2与H2反应生成CH4和H2O(g)的热化学方程式:_____ 。
②研究表明,反应III的速率方程为v=k[x(CO)x(H2O)- ],x表示相应气体的物质的量分数,Kp为平衡常数(用平衡分压代替平衡浓度计算),k为反应的速率常数。在气体物质的量分数和催化剂一定的情况下,反应速率随温度的变化如图所示,根据速率方程分析T>Tm时,v逐渐下降的原因是
],x表示相应气体的物质的量分数,Kp为平衡常数(用平衡分压代替平衡浓度计算),k为反应的速率常数。在气体物质的量分数和催化剂一定的情况下,反应速率随温度的变化如图所示,根据速率方程分析T>Tm时,v逐渐下降的原因是_____ 。

(3)工业上用二氧化碳催化加氢可合成乙醇,其反应原理为:2CO2(g)+6H2(g) CH3CH2OH(g)+3H2O(g) △H。
CH3CH2OH(g)+3H2O(g) △H。
①通过表格中的数值可以推断:该反应在______ (填“高温”、“低温”或“任何温度”)下能自发进行。
②CO2的平衡转化率与氢碳比m[m= ]及压强、温度的关系分别如图a和图b所示。
]及压强、温度的关系分别如图a和图b所示。

图a中氢碳比m从大到小的顺序为______ 。
图b中压强从大到小的顺序为_____ ,判断依据为______ 。
(1)已知25℃时,大气中的CO2溶于水存在以下过程:
①CO2(g)
②CO2(aq)+H2O(l)
溶液中CO2的浓度与其在大气中的分压(分压=总压×物质的量分数)成正比,比例系数为ymol•L-1•kPa-1。当大气压强为pkPa,大气中CO2(g)的物质的量分数为x时,溶液中H+的浓度为
(2)已知CH4的生成焓(由稳定单质生成该物质)为△H=-71.7kJ•mol-1
反应I:C(s)+H2O(g)
反应II:C(s)+2H2O(g)
反应III:CO(g)+H2O(g)
①写出CO2与H2反应生成CH4和H2O(g)的热化学方程式:
②研究表明,反应III的速率方程为v=k[x(CO)x(H2O)-

(3)工业上用二氧化碳催化加氢可合成乙醇,其反应原理为:2CO2(g)+6H2(g)
| 温度/K | 400 | 500 |
| 平衡常数K | 9 | 5.3 |
②CO2的平衡转化率与氢碳比m[m=

图a中氢碳比m从大到小的顺序为
图b中压强从大到小的顺序为
全球大气  浓度升高对人类生产生活产生了影响,研究二氧化碳的回收对我国2060年实现碳中和具有现实意义,碳及其化合物的资源化利用成为研究热点。回答下列问题:
浓度升高对人类生产生活产生了影响,研究二氧化碳的回收对我国2060年实现碳中和具有现实意义,碳及其化合物的资源化利用成为研究热点。回答下列问题:
(1)工业上用二氧化碳催化加氢可合成乙醇,其反应原理为:
①通过表格中的数值可以推断:该反应在________ (填“高温”、“低温”或“任何温度”)下能自发进行。
② 的平衡转化率与氢碳比
的平衡转化率与氢碳比  及压强、温度的关系分别如图 a和图 b所示。
及压强、温度的关系分别如图 a和图 b所示。

图a中氢碳比 从大到小的顺序为
从大到小的顺序为___________ 。图b中压强从大到小的顺序为___________ 。
(2)反应

反应

反应
①
___________ ,
___________ (用  表示)。
表示)。
②研究表明,反应 Ⅲ的速率方程为 表示反应气体的物质的量分数,
表示反应气体的物质的量分数, 为平衡常数(用平衡分压代替平衡浓度计算),
为平衡常数(用平衡分压代替平衡浓度计算), 为反应的速率常数。当恒压
为反应的速率常数。当恒压 ,只发生反应Ⅲ:COg+H2Og⇌CO2g+H2gΔH3=-akJ⋅mol-1K3且
,只发生反应Ⅲ:COg+H2Og⇌CO2g+H2gΔH3=-akJ⋅mol-1K3且  加料时,平衡转化率为 b,求反应物转化率为
加料时,平衡转化率为 b,求反应物转化率为 时的反应速率
时的反应速率
___________ (用含  的计算式表示,不用化简)。
的计算式表示,不用化简)。
(3)已知 时,大气中的
时,大气中的  溶于水存在以下过程:
溶于水存在以下过程:
①
②
溶液中 的浓度
的浓度  为比例系数,此题可看为常数)。当大气压强为
为比例系数,此题可看为常数)。当大气压强为 ,大气中
,大气中 的物质的量分数为
的物质的量分数为 时,溶液中
时,溶液中 的浓度为
的浓度为_______  (忽略
(忽略 和水的电离)。
和水的电离)。
(1)工业上用二氧化碳催化加氢可合成乙醇,其反应原理为:
| 温度/ | 400 | 500 |
| 平衡常数 | 9 | 5.3 |
②

图a中氢碳比
(2)反应
反应
反应
①
②研究表明,反应 Ⅲ的速率方程为
(3)已知
①
②
溶液中
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


