解答题-实验探究题 较难0.4 引用1 组卷310
氨基甲酸铵 是一种重要的化工原料,可用于药物合成、制备化学肥料、灭火剂或洗涤剂等。某化学兴趣小组用如图所示装置制取氨基甲酸铵:
是一种重要的化工原料,可用于药物合成、制备化学肥料、灭火剂或洗涤剂等。某化学兴趣小组用如图所示装置制取氨基甲酸铵:
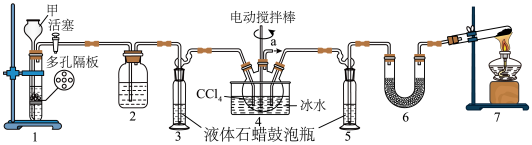
已知:①制取氨基甲酸铵反应为:
 。
。
②氨基甲酸铵溶于水后生成 和
和 。
。
回答下列问题:
(1)仪器甲的名称是___________ ,装置2的作用是除去 中的水蒸气,其盛装的试剂是
中的水蒸气,其盛装的试剂是___________ 。
(2)装置7是实验室制备氨气,其化学方程式为___________ 。
(3)液体石蜡鼓泡瓶的作用是___________ 。
(4)实验制得产品 ,其中可能含有碳酸氢铵杂质(不考虑碳酸氢铵与一水合氨的之间的反应)。设计方案进行成分探究,请填写表中空格。
,其中可能含有碳酸氢铵杂质(不考虑碳酸氢铵与一水合氨的之间的反应)。设计方案进行成分探究,请填写表中空格。
限选试剂:蒸馏水、稀硝酸、 溶液、澄清石灰水、
溶液、澄清石灰水、 溶液、稀盐酸。
溶液、稀盐酸。
通过计算氨基甲酸铵的质量分数是___________ 。(保留小数点后两位)[ 、
、 ]
]
(5)氨基甲酸铵易分解,用如图所示装置测定 时该分解反应的化学平衡常数
时该分解反应的化学平衡常数 ,实验步骤如下:
,实验步骤如下:

(Ⅰ)关闭 ,打开
,打开 和
和 ,开启真空泵抽气至测压仪数值稳定后关闭
,开启真空泵抽气至测压仪数值稳定后关闭 。
。
(Ⅱ)关闭 ,
,___________ ,读取压强数值。
测得 时压强为
时压强为 。
。
①请在空白处完善步骤Ⅱ的实验操作。
②若步骤I中测压仪数值未稳定即关闭 ,
, 测量值
测量值___________ (选填“偏大”、“偏小”或“无影响”)。

已知:①制取氨基甲酸铵反应为:
②氨基甲酸铵溶于水后生成
回答下列问题:
(1)仪器甲的名称是
(2)装置7是实验室制备氨气,其化学方程式为
(3)液体石蜡鼓泡瓶的作用是
(4)实验制得产品
限选试剂:蒸馏水、稀硝酸、
| 实验步骤 | 预期现象和结论 |
| 步骤1:取固体样品于试管中,加入蒸馏水至固体溶解 | 得到无色溶液 |
| 步骤2:向试管中继续加入足量澄清石灰水 | |
| 步骤3:过滤、洗涤、 | 证明样品中有碳酸氢铵 |
(5)氨基甲酸铵易分解,用如图所示装置测定

(Ⅰ)关闭
(Ⅱ)关闭
测得
①请在空白处完善步骤Ⅱ的实验操作。
②若步骤I中测压仪数值未稳定即关闭
2024·广东·一模
类题推荐
氨基甲酸铵(H2NCOONH4)是一种易分解、易水解的白色固体,某研究小组以氢氧化钠固体、浓氨水、干冰等为原料制备氨基甲酸铵的实验装置如图所示,其主要反应的原理为2NH3(g)+CO2(g)⇌NH2COONH4(s) ΔH<0。
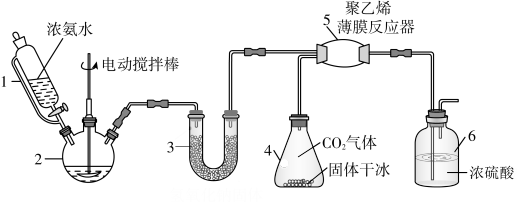
(1)仪器3中盛装的固体是____ ,其作用是________________ 。
(2)仪器6的一个作用是控制原料气按化学计量数充分反应,若反应初期观察到装置内浓硫酸中产生气泡,则应该___ (填“加快”“减慢”或“不改变” )产生氨的速率。
(3)另一种制备氨基甲酸铵的反应装置(液态石蜡和CCl4均充当惰性介质)如图所示。

①液态石蜡鼓泡瓶的作用是________________________ 。
②当CCl4液体中产生较多晶体悬浮物时,立即停止反应,过滤分离得到粗产品,为了将所得粗产品干燥,可采取的方法是___ (填字母)。
A.蒸馏 B.真空微热烘干 C.高压加热烘干
(4)制得的氨基甲酸铵中可能含有碳酸氢铵、碳酸铵中的一种或两种杂质(不考虑氨基甲酸铵与水的反应)。
①设计方案进行成分探究,请填写表中空格。
限选试剂:蒸馏水、稀硝酸、BaCl2溶液、澄清石灰水、AgNO3溶液、稀盐酸。
②根据①的结论,取15.8g氨基甲酸铵样品,用足量氢氧化钡溶液充分处理后,过滤洗涤、干燥,测得沉淀的质量为1.97g。则样品中氨基甲酸铵的质量分数为____ 。

(1)仪器3中盛装的固体是
(2)仪器6的一个作用是控制原料气按化学计量数充分反应,若反应初期观察到装置内浓硫酸中产生气泡,则应该
(3)另一种制备氨基甲酸铵的反应装置(液态石蜡和CCl4均充当惰性介质)如图所示。

①液态石蜡鼓泡瓶的作用是
②当CCl4液体中产生较多晶体悬浮物时,立即停止反应,过滤分离得到粗产品,为了将所得粗产品干燥,可采取的方法是
A.蒸馏 B.真空微热烘干 C.高压加热烘干
(4)制得的氨基甲酸铵中可能含有碳酸氢铵、碳酸铵中的一种或两种杂质(不考虑氨基甲酸铵与水的反应)。
①设计方案进行成分探究,请填写表中空格。
限选试剂:蒸馏水、稀硝酸、BaCl2溶液、澄清石灰水、AgNO3溶液、稀盐酸。
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量固体样品于试管中,加入蒸馏水至固体溶解 | 得到无色溶液 |
| 步骤2:向试管中加入过量的BaCl2溶液,静置 | 若溶液不变浑浊,则证明固体中不含碳酸铵 |
| 步骤3:向试管中继续加入 |
氨基甲酸铵(H2 NCOONH4)是一种易分解、易水解的白色固体。其研究小组以浓氨水、干冰等为原料制备氨基甲酸铵的实验装置如图1所示,其主要反应的原理为2NH3(g)+CO2(g) NH2COONH4(s) △H<0
NH2COONH4(s) △H<0
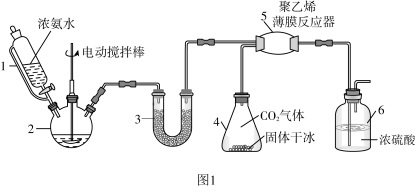

(1)仪器1的名称是___________ 。仪器3中盛装的固体是___________ ,其作用是___________ 。
(2)仪器6的一个作用是控制原料气按反应计量系数充分反应,若反应初期观察到装置内浓硫酸中产生气泡,则应该___________ (填“加快”“减慢”或“不改变”)产生氨气的速率。
(3)另一种制备氨基甲酸铵的反应装置(液体石蜡和CCl4均充当惰性介质)如图2所示。
①液体石蜡鼓泡瓶的作用是______________________ 。
②若无冰水,则氨基甲酸铵易分解生成尿素[CO(NH2)2]请写出氨基甲酸铵受热分解的化学方程式:______________________ 。
③当CCl4液体中产生较多晶体悬浮物时,立即停止反应,过滤分离得到粗产品,为了将所得粗产品干燥,可采取的方法是___________ (填标号)。
A.蒸馏 B.真空微热烘干 C.高压加热烘干
(4)制得的氨基甲酸铵中可能含有碳酸氢铵、碳酸铵中的一种或两种杂质(不考虑氨基甲酸铵与水的反应)。
①设计方案,进行成分探究,请填写表中空格。
限选试剂:蒸馏水、稀硝酸、BaCl2溶液、澄清石灰水、AgNO3溶液、稀盐酸。
②根据①的结论。取15.8g氨基甲酸铵样品,用足量氧氧化钡溶液充分处理后,过滤、洗涤、干燥,测得沉淀质量为1.97g。则样品中氨基甲酸铵的质量分数为___________ 。
 NH2COONH4(s) △H<0
NH2COONH4(s) △H<0

(1)仪器1的名称是
(2)仪器6的一个作用是控制原料气按反应计量系数充分反应,若反应初期观察到装置内浓硫酸中产生气泡,则应该
(3)另一种制备氨基甲酸铵的反应装置(液体石蜡和CCl4均充当惰性介质)如图2所示。
①液体石蜡鼓泡瓶的作用是
②若无冰水,则氨基甲酸铵易分解生成尿素[CO(NH2)2]请写出氨基甲酸铵受热分解的化学方程式:
③当CCl4液体中产生较多晶体悬浮物时,立即停止反应,过滤分离得到粗产品,为了将所得粗产品干燥,可采取的方法是
A.蒸馏 B.真空微热烘干 C.高压加热烘干
(4)制得的氨基甲酸铵中可能含有碳酸氢铵、碳酸铵中的一种或两种杂质(不考虑氨基甲酸铵与水的反应)。
①设计方案,进行成分探究,请填写表中空格。
限选试剂:蒸馏水、稀硝酸、BaCl2溶液、澄清石灰水、AgNO3溶液、稀盐酸。
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量固体样品于试管中,加入蒸馏水至固体溶解 | 得到无色溶液 |
| 步骤2:向试管中加入过量的BaCl2溶液,静置 | 若溶液不变浑浊,则证明固体中不含碳酸铵 |
| 步骤3:向试管中继续加入 |
②根据①的结论。取15.8g氨基甲酸铵样品,用足量氧氧化钡溶液充分处理后,过滤、洗涤、干燥,测得沉淀质量为1.97g。则样品中氨基甲酸铵的质量分数为
氨基甲酸铵是一种重要化工产品,常温时为白色晶体或粉末,易溶于水,难溶于CCl4,59℃时分解为氨及二氧化碳,其制备原理:2NH3(g)+CO2(g) NH2COONH4(s)ΔH=-272kJ·mol−1.某化学兴趣小组利用下图实验装置(部分固定装置已省略)模拟制备NH2COONH4.试回答下列问题:
NH2COONH4(s)ΔH=-272kJ·mol−1.某化学兴趣小组利用下图实验装置(部分固定装置已省略)模拟制备NH2COONH4.试回答下列问题:

(1)仪器组装完毕后,首先应进行的操作是_______ 。仪器b的名称是_______ 。
(2)装置A用于实验室制取NH2COONH4的原料气体之一,该反应的化学方程式为_______ 。
(3)装置F中试剂的名称为_______ 。
(4)为提高原料气的利用率,应控制装置C和E中最佳鼓泡速率比为_______ ,装置D采用冰水浴的原因为_______ 。
(5)生成的氨基甲酸铵悬浮于CCl4中,下列操作可实现产品分离的是_______ 。(填字母)
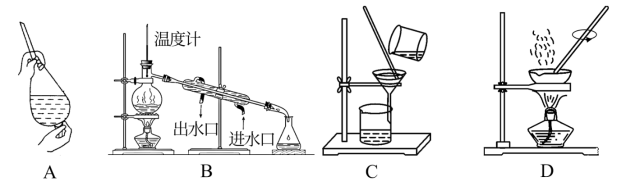
(6)制得的氨基甲酸铵可能含有碳酸氢铵、碳酸铵中的一种或两种杂质。
设计方案,进行成分探究,请填写表中空格。
限选试剂:蒸馏水、稀HNO3、BaCl2溶液、澄清石灰水、AgNO3溶液、稀盐酸。

(1)仪器组装完毕后,首先应进行的操作是
(2)装置A用于实验室制取NH2COONH4的原料气体之一,该反应的化学方程式为
(3)装置F中试剂的名称为
(4)为提高原料气的利用率,应控制装置C和E中最佳鼓泡速率比为
(5)生成的氨基甲酸铵悬浮于CCl4中,下列操作可实现产品分离的是

(6)制得的氨基甲酸铵可能含有碳酸氢铵、碳酸铵中的一种或两种杂质。
设计方案,进行成分探究,请填写表中空格。
限选试剂:蒸馏水、稀HNO3、BaCl2溶液、澄清石灰水、AgNO3溶液、稀盐酸。
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量固体样品于试管中, 加入蒸馏水至固体溶解。 | 得到无色溶液 |
| 步骤2:向试管中加入过量的BaCl2溶液,静置 | 若溶液不变浑浊,证明固体中不含碳酸铵 |
| 步骤3:向试管中继续加入 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


