解答题-无机推断题 适中0.65 引用1 组卷62
现有A、B、C、D、E、F、G、H8种元素,均为前四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
(1) 的电子式为
的电子式为________ 。(A、C为字母代号,请将字母代号用元素符号表示,下同)。
(2)B元素基态原子中能量最高的电子所占据的原子轨道呈________ 形。
(3)E元素基态原子的核外价电子轨道表示式为________ ,该元素的 远远大于
远远大于 ,其原因是
,其原因是________ 。
(4)D、E、F三种元素的简单离子半径由大到小的顺序是________________ 。
(5)G的最高价氧化物对应的水化物与E的氧化物反应的离子方程式________________________ 。
(6)H位于元素周期表中________ 区(按电子排布分区)。
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素是形成化合物种类最多的元素 |
| C元素基态原子的核外p能级电子数比s能级电子数少1 |
| D元素基态原子的核外p轨道中有两个未成对电子 |
| E元素的气态基态原子的第一至第四电离能分别是 |
| F元素的主族序数与周期数的差为4 |
| G元素是前四周期中电负性最小的元素 |
| H元素位于元素周期表中的第8列 |
(2)B元素基态原子中能量最高的电子所占据的原子轨道呈
(3)E元素基态原子的核外价电子轨道表示式为
(4)D、E、F三种元素的简单离子半径由大到小的顺序是
(5)G的最高价氧化物对应的水化物与E的氧化物反应的离子方程式
(6)H位于元素周期表中
23-24高二上·海南海口·阶段练习
类题推荐
(1)元素D在元素周期表中的位置为___________ ;元素 与元素
与元素 所形成的晶体属于
所形成的晶体属于___________ (填分子晶体、共价晶体、金属晶体或离子晶体)
(2)如图中阴影部分所示区域的元素称为___________ 元素,下列元素属于该区域的是___________ 。
(3)G2D2的电子式为___________ 。(D、G为字母代号,请将字母代号用元素符号表示,下同)。
(4)某同学推断E元素基态原子的核外电子轨道表示式如图。该同学所画的电子轨道表示式违背了___________ ,该元素的 远远大于
远远大于 ,其原因是
,其原因是___________ 。
(5)D、E、F三种元素的简单离子半径由大到小的顺序是___________ 。
(6)H位于元素周期表中___________ 区(按电子排布分区),其基态原子的价电子排布为___________ 。与元素 位于同一周期,其原子基态时未成对电子数在同周期中最多的元素是
位于同一周期,其原子基态时未成对电子数在同周期中最多的元素是___________ (填元素符号)。
(7)写出一种由A、B、C、D四种元素组成离子化合物___________ 。
Ⅰ.已知A、B、C、D、E、F、G、H8种短周期元素的原子半径和某些化合价如下表所示:
(1)将D、F两种元素的元素符号填入如图所示元素周期表中的相应位置_______ 。
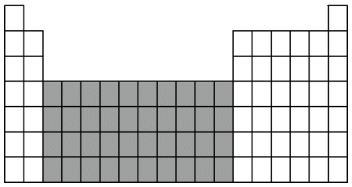
(2)上图中阴影部分所示区域的元素称为_______ 元素,下列元素属于该区域的是_______ 。
A.Ba B.Fe C.Br D.Rb
Ⅱ.现有A、B、C、D、E、F、G、H元素,均为前四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
(3)G2D2的电子式为_______ 。(D、G为字母代号,请将字母代号用元素符号表示,下同)。
(4)某同学推断E元素基态原子的核外电子轨道表示式为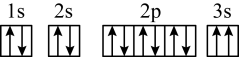 。该同学所画的电子轨道表示式违背了
。该同学所画的电子轨道表示式违背了_______ ,该元素的I3远远大于I2,其原因是_______ 。
(5)D、E、F三种元素的简单离子半径由大到小的顺序是_______ 。
(6)H位于元素周期表中_______ 区(按电子排布分区),其基态原子的价电子排布式为_______ 。与元素H位于同一周期,其原子基态时未成对电子数在同周期中最多的元素是_______ (填元素符号)。
(7)写出一种由A、B、C、D四种元素组成离子化合物_______ 。
(8)GeO2不能形成类似CO2分子中的π键,原因是_______ 。
| 元素 | A | B | C | D | E | F | G | H |
| 化合价 | -2 | +5、-3 | +4、-4 | +6、-2 | +2 | +1 | +7、-1 | +4、-4 |
| 原子半径/nm | 0.073 | 0.075 | 0 077 077 | 0.102 | 0 130 130 | 0.154 | 0 099 099 | 0.111 |

(2)上图中阴影部分所示区域的元素称为
A.Ba B.Fe C.Br D.Rb
Ⅱ.现有A、B、C、D、E、F、G、H元素,均为前四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素是形成化合物种类最多的元素 |
| C元素基态原子的核外p能级电子数比s能级电子数少1 |
| D元素基态原子的核外p轨道中有两个未成对电子 |
| E元素的气态基态原子的第一至第四电离能分别是I1=738kJ/mol,I2=1451kJ/mol,I3=7733kJ/mol,I4=10540kJ/mol |
| F元素的主族序数与周期数的差为4 |
| G元素是前四周期中电负性最小的元素 |
| H元素位于元素周期表中的第8列 |
(4)某同学推断E元素基态原子的核外电子轨道表示式为
 。该同学所画的电子轨道表示式违背了
。该同学所画的电子轨道表示式违背了(5)D、E、F三种元素的简单离子半径由大到小的顺序是
(6)H位于元素周期表中
(7)写出一种由A、B、C、D四种元素组成离子化合物
(8)GeO2不能形成类似CO2分子中的π键,原因是
有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题:
请回答下列问题:
(1)D基态原子中能量最高的电子其原子轨道呈___________ 形。
(2)C基态原子核外电子的运动状态有___________ 种。
(3)G位于元素周期表的位置为:___________ ,位于___________ 区。
(4)写出由A、B、E三种元素形成的离子化合物的电子式___________ 。
(5)检验F元素的方法是___________ 。
(6)同周期,第一电离能位于C、E之间的元素有___________ 种。
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数比s电子数少1个 |
| C元素原子的第一至第四电离能分别是 |
| 原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期序数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |
(1)D基态原子中能量最高的电子其原子轨道呈
(2)C基态原子核外电子的运动状态有
(3)G位于元素周期表的位置为:
(4)写出由A、B、E三种元素形成的离子化合物的电子式
(5)检验F元素的方法是
(6)同周期,第一电离能位于C、E之间的元素有
I.已知A、B、C、D、E、F、G、H8种短周期元素的原子半径和某些化合价如下表所示:
元素 | A | B | C | D | E | F | G | H |
化合价 | -2 | +5、-3 | +4、-4 | +6、-2 | +2 | +1 | +7、-1 | +4、-4 |
原子半径/nm | 0.073 | 0.075 | 0.077 | 0.102 | 0.130 | 0.154 | 0.099 | 0.111 |
(1)元素D在元素周期表中的位置为
(2)如图中阴影部分所示区域的元素称为

A.Ba B.Fe C.Br D.Rb
Ⅱ.现有A、B、C、D、E、F、G、H元素,均为前四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
A | 核外电子数和电子层数相等 |
B | 形成化合物种类最多的元素 |
C | 基态原子的核外p能级电子数比s能级电子数少1 |
D | 基态原子的核外p轨道中有两个未成对电子 |
E | 气态基态原子的第一至第四电离能分别是I1=738kJ/mol,I2=1451kJ/mol,I3=7733kJ/mol,I4=10540kJ/mol |
F | 主族序数与周期数的差为4 |
G | 前四周期中电负性最小的元素 |
H | 位于元素周期表中的第11列 |
(4)某同学推断E元素基态原子的核外电子轨道表示式如图。该同学所画的电子轨道表示式违背了

(5)D、E、F三种元素的简单离子半径由大到小的顺序是
(6)H位于元素周期表中
(7)写出一种由A、B、C、D四种元素组成离子化合物
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


