解答题-结构与性质 适中0.65 引用1 组卷60
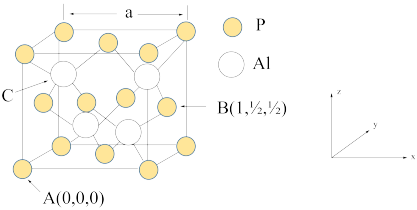
凉山州是矿产资源“聚宝盆”,下辖的会东、金阳、雷波等县磷矿资源丰富,磷化工产业比较发达。请回答下列问题:
(1)基态磷原子的价电子排布图为:___________ ;其基态原子核外有___________ 种不同能量的电子。
(2)含磷药物磷酸氯喹对治疗新冠肺炎有一定效果,其结构如下图。
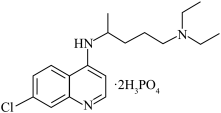
磷酸氯喹中所含第二周期元素第一电离能由大到小的顺序为:___________ ,其中碳原子的轨道杂化类型为:___________ 。
(3)卤化磷通常有三卤化磷和五卤化磷。三卤化磷的熔点见下表,试解释PF3、PCl3、PBr3、PI3熔点逐渐升高的原因是___________ 。
(4)已知PCl5晶体中含有等量的[PCl4]+和[PCl6]-。
①PCl5晶体中的化学键有___________ ,其中[PCl4]+的空间构型为___________ 。
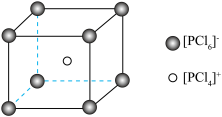
②PCl5晶胞结构如下图,晶胞中含有的P原子的个数为___________ ,已知晶胞边长为apm,阿伏加德罗常数为NA,则该晶体密度为___________ g/cm3(列出计算式即可)。
(1)基态磷原子的价电子排布图为:
(2)含磷药物磷酸氯喹对治疗新冠肺炎有一定效果,其结构如下图。

磷酸氯喹中所含第二周期元素第一电离能由大到小的顺序为:
(3)卤化磷通常有三卤化磷和五卤化磷。三卤化磷的熔点见下表,试解释PF3、PCl3、PBr3、PI3熔点逐渐升高的原因是
| 三卤化磷 | PF3 | PCl3 | PBr3 | PI3 |
| 熔点/℃ | -151.5 | -93.6 | -41.5 | 61.2 |
①PCl5晶体中的化学键有
②PCl5晶胞结构如下图,晶胞中含有的P原子的个数为

2024·四川凉山·一模
类题推荐
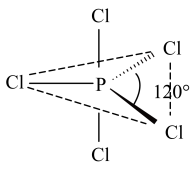
白磷(P4)是磷的单质之一,与卤素单质反应生成卤化磷。卤化磷通常有三卤化磷和五卤化磷(PCl5分子结构如图所示,其中Cl原子有两种不同位置)。回答下列问题:_____ 。P、S、Cl的第一电离能由小到大顺序为_____ 。
(2)PCl5水解产生一种无色油状中间产物POCl3,该分子的空间结构为_____ 。
(3)PCl5中P的轨道杂化类型为_____(填字母标号)。
(4)三卤化磷的熔点见下表,分析变化趋势及原因是_____ 。
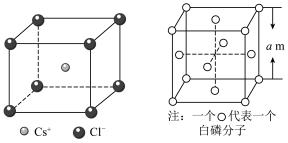
(5)PCl5晶体呈CsCl(晶胞结构如下图)型构造,其中含有等量的 和正四面体形的
和正四面体形的_____ (填化学式),两者之间形成_____ 键。晶胞中含有的P原子的个数为_____ 。 ,则该晶体密度为
,则该晶体密度为_____  (用含NA、a的式子表示)。
(用含NA、a的式子表示)。
(2)PCl5水解产生一种无色油状中间产物POCl3,该分子的空间结构为
(3)PCl5中P的轨道杂化类型为_____(填字母标号)。
| A.sp3 | B.sp3d | C.d2sp3 | D.dsp2 |
| 三卤化磷 | PF3 | PCl3 | PBr3 | PI3 |
| 熔点/℃ | -151.5 | -93.6 | -41.5 | 61.2 |
根据第三周期元素的结构和性质,回答下列问题:
(1)基态氯原子有___ 种能量不同的电子,其价层电子排布式为____ ,未成对电子所处的原子轨道形状是____ 。
(2)磷的氯化物有PCl3和PCl5两种。PCl3中磷原子的杂化类型为_____ ,PCl3的立体构型为_____ ,其中PCl3的熔点____ (填“大于”或“小于”)PCl5。
(3)P、S和Cl三元素的第一电离能大小顺序为____ ,电负性大小顺序为____ 。
(4)氯有多种含氧酸,其电离平衡常数如下:
从结构的角度解释以上含氧酸Ka不同的原因____________ 。
(5)NaCl晶胞如图所示:
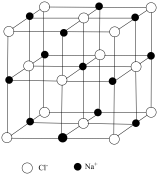
①Na+的配位数为____________ 。
②若氯离子的半径为r nm,阿伏加 德罗常数用NA表示,则晶胞密度的表达式为____ g/cm3(用含r、NA的代数式表示)。
(1)基态氯原子有
(2)磷的氯化物有PCl3和PCl5两种。PCl3中磷原子的杂化类型为
(3)P、S和Cl三元素的第一电离能大小顺序为
(4)氯有多种含氧酸,其电离平衡常数如下:
| 化学式 | HClO4 | HClO3 | HClO2 | HClO |
| Ka | 1×1010 | 1×10 | 1×10-2 | 1×10-8 |
(5)NaCl晶胞如图所示:

①Na+的配位数为
②若氯离子的半径为r nm,阿伏加 德罗常数用NA表示,则晶胞密度的表达式为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网