解答题-工业流程题 较易0.85 引用1 组卷114
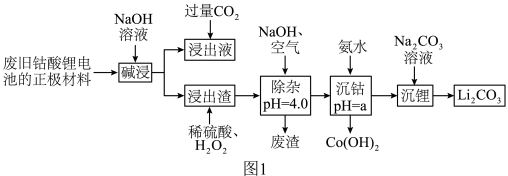
废旧钴酸锂电池的正极材料主要含有难溶于水的LiCoO2及少量Al、Fe、炭黑等,常用如图1所示的一种工艺分离并回收其中的金属钴和锂。
②相关金属离子形成氢氧化物沉淀的pH如下表:
回答下列问题:
(1)LiCoO2中元素Co的化合价为___________ 。
(2)为提高碱浸率,可采取的措施有___________ (答出一条即可)。
(3)碱浸时的离子反应方程式为___________ 。
(4)沉钴的离子方程式为___________ 。
(5)加氨水控制沉钴的pH,当a≥___________ 时,此时溶液中c(Co2+)≤10-5mol⋅L-1,即认为“沉钴”完全。
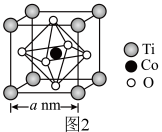
(6)钴的氢氧化物加热至290℃时可以完全脱水,所得产物可用于合成钛酸钴。钛酸钴的晶胞结构如图2所示,则该晶体化学式为___________ 。___________ molAgCl,该配合物中Co3+的配位数为___________ 。
②相关金属离子形成氢氧化物沉淀的pH如下表:
| 金属阳离子 | Al3+ | Fe3+ | Fe2+ |
| 开始沉淀的pH | 4.2 | 2.7 | 7.6 |
| 沉淀完全的pH | 5.2 | 3.7 | 9.6 |
(1)LiCoO2中元素Co的化合价为
(2)为提高碱浸率,可采取的措施有
(3)碱浸时的离子反应方程式为
(4)沉钴的离子方程式为
(5)加氨水控制沉钴的pH,当a≥
(6)钴的氢氧化物加热至290℃时可以完全脱水,所得产物可用于合成钛酸钴。钛酸钴的晶胞结构如图2所示,则该晶体化学式为
23-24高二上·河北秦皇岛·阶段练习
类题推荐
锂被誉为“高能金属”,废旧锂离子电池的正极材料主要含有LiCoO2及少量Al、Fe等,处理该废料的一种工艺流程如图所示:
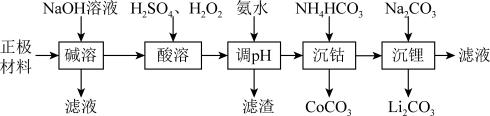
已知:①Ksp(Li2CO3)=1.6×10-3,LiCoO2难溶于水,具有强氧化性;
②相关金属离子形成氢氧化物沉淀的pH值如下表所示:
回答下列问题:
(1)写出“碱溶”时发生主要反应的离子方程式:____________________________________ 。
(2)为提高“酸溶”的浸出速率,可采取的措施有___________________________ (任写一种)。
(3)“酸溶”时,LiCoO2发生的主要反应的离子方程式为_____________________________ ;若用浓盐酸代替H2SO4和H2O2的混合液,缺点是___________________________________ 。
(4)用氨水调节pH的范围为____________ ,若“沉钴”后溶液中c(Li+)=4 mol·L-1,加入等体积的Na2CO3溶液后,沉淀中的Li元素占原Li元素总量的90%,则“沉锂”后溶液中c( )=
)=__________ mol·L-1。
(5)该流程涉及多次过滤,实验室中过滤后洗涤沉淀的操作为________________ 。
(6)写出“沉钴”过程中发生反应的离子方程式:____________________________________ 。

已知:①Ksp(Li2CO3)=1.6×10-3,LiCoO2难溶于水,具有强氧化性;
②相关金属离子形成氢氧化物沉淀的pH值如下表所示:
Al3+ | Fe3+ | Fe2+ | Co2+ | |
开始沉淀的pH | 4.0 | 2.7 | 7.6 | 7.0 |
沉淀完全的pH | 5.2 | 3.7 | 9.6 | 9.0 |
回答下列问题:
(1)写出“碱溶”时发生主要反应的离子方程式:
(2)为提高“酸溶”的浸出速率,可采取的措施有
(3)“酸溶”时,LiCoO2发生的主要反应的离子方程式为
(4)用氨水调节pH的范围为
(5)该流程涉及多次过滤,实验室中过滤后洗涤沉淀的操作为
(6)写出“沉钴”过程中发生反应的离子方程式:
锂被誉为“高能金属”,废旧锂离子电池的正极材料主要含有LiCoO2及少量Al、Fe等,处理该废料的一种工艺流程如图所示:
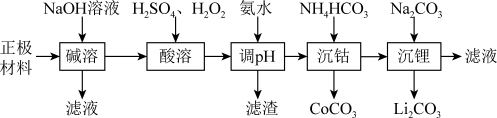
已知:①Ksp(Li2CO3)=1.6×10-3,LiCoO2难溶于水,具有强氧化性;②相关金属离子形成氢氧化物沉淀的pH值如表所示:
回答下列问题:
(1)写出“碱溶”时发生主要反应的离子方程式:______ 。
(2)为提高“酸溶”的浸出速率,可采取的措施有______ (任写一种)。
(3)“酸溶”时,LiCoO2发生的主要反应的离子方程式为______ ;若用浓盐酸代替H2SO4和H2O2的混合液,缺点是______ 。
(4)用氨水调节pH的范围为_____
(5)该流程涉及多次过滤,实验室中过滤后洗涤沉淀的操作为______ 。
(6)写出“沉钴”过程中发生反应的离子方程式:_____ 。

已知:①Ksp(Li2CO3)=1.6×10-3,LiCoO2难溶于水,具有强氧化性;②相关金属离子形成氢氧化物沉淀的pH值如表所示:
| Al3+ | Fe3+ | Fe2+ | Co2+ | |
| 开始沉淀的pH | 4.0 | 2.7 | 7.6 | 7.0 |
| 沉淀完全的pH | 5.2 | 3.7 | 9.6 | 9.0 |
(1)写出“碱溶”时发生主要反应的离子方程式:
(2)为提高“酸溶”的浸出速率,可采取的措施有
(3)“酸溶”时,LiCoO2发生的主要反应的离子方程式为
(4)用氨水调节pH的范围为
(5)该流程涉及多次过滤,实验室中过滤后洗涤沉淀的操作为
(6)写出“沉钴”过程中发生反应的离子方程式:
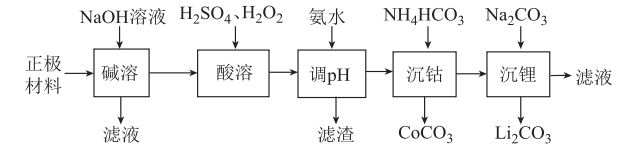
锂被誉为“高能金属”,废旧锂离子电池的正极材料主要含有LiCoO2及少量Al、Fe等,处理该废料的一种工艺流程如图所示:
已知:① ,LiCoO2难溶于水,具有强氧化性(且氧化性强于KMnO4);
,LiCoO2难溶于水,具有强氧化性(且氧化性强于KMnO4);
②相关金属离子形成氢氧化物沉淀的pH值如表所示:
回答下列问题::
(1)写出“碱溶”时发生主要反应的化学方程式:___________ 。
(2)为提高“酸溶”的浸出速率,可采取的措施有___________ (任写一种)。
(3)“酸溶”时,LiCoO2能将H2O2氧化,其离子方程式为___________ ;若用浓盐酸代替H2SO4和H2O2的混合液,缺点是___________ 。
(4)用氨水调节pH的范围为___________ 。
(5)该流程涉及多次过滤,实验室中过滤后洗涤沉淀的操作为___________ 。
(6)写出“沉钴”过程中发生反应的离子方程式:___________ 。

已知:①
②相关金属离子形成氢氧化物沉淀的pH值如表所示:
| 金属离子 | Al3+ | Fe3+ | Fe2+ | Co2+ |
| 开始沉淀的pH | 4.0 | 2.7 | 7.6 | 7.0 |
| 沉淀完全的pH | 5.2 | 3.7 | 9.6 | 9.0 |
回答下列问题::
(1)写出“碱溶”时发生主要反应的化学方程式:
(2)为提高“酸溶”的浸出速率,可采取的措施有
(3)“酸溶”时,LiCoO2能将H2O2氧化,其离子方程式为
(4)用氨水调节pH的范围为
(5)该流程涉及多次过滤,实验室中过滤后洗涤沉淀的操作为
(6)写出“沉钴”过程中发生反应的离子方程式:
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


