解答题-实验探究题 容易0.94 引用1 组卷47
在中国古代,硫酸被炼丹术士称为“绿矾油”。这是因为生产硫酸最古老的方法是以绿矾为原料,在蒸馏釜中煅烧后,釜中逸出刺激性气味的气体,同时有油状液体流出,残留固体呈红棕色。

(1)请写出煅烧绿矾过程中发生反应的化学方程式:
①___________ ;
②___________ 。
(2)化学探究小组的同学用如图所示装置模拟用绿矾制硫酸的实验,并检验生成的硫酸和二氧化硫(加热装置已略去),其中b为干燥的试管。下列关于该反应说法正确的是___________。

(1)请写出煅烧绿矾过程中发生反应的化学方程式:
①
②
(2)化学探究小组的同学用如图所示装置模拟用绿矾制硫酸的实验,并检验生成的硫酸和二氧化硫(加热装置已略去),其中b为干燥的试管。下列关于该反应说法正确的是___________。
| A.若将反应后的气体通入 |
| B.b中产物用紫色石蕊试液即可检验出其中 |
| C.为检验反应的气态生成物是 |
| D.b中所得到的硫酸的质量分数为29.5% |
2024高一·全国·学业考试
类题推荐
生产硫酸最古老的方法是以绿矾为原料,在蒸镏釜中煅烧。反应的化学方程式为


 (已知二氧化硫的沸点为-10℃,三氧化硫的沸点为44.8℃)。用如图所示的装置模拟用绿矾制硫酸的实验,并检验生成的硫酸和二氧化硫,
(已知二氧化硫的沸点为-10℃,三氧化硫的沸点为44.8℃)。用如图所示的装置模拟用绿矾制硫酸的实验,并检验生成的硫酸和二氧化硫, 为干燥的试管,加热装置已略去。下列有关说法正确的是
为干燥的试管,加热装置已略去。下列有关说法正确的是
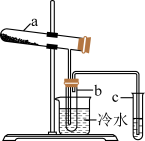

| A.若将反应后的三种气体通入 |
| B. |
| C.为检验反应的另一种生成物,试管 |
| D. |
生产硫酸最古老的方法是以绿矾为原料,在蒸镏釜中煅烧。反应的化学方程式为 (已知二氧化硫的沸点为
(已知二氧化硫的沸点为 ,三氧化硫的沸点为44.8℃)。用如图所示的装置模拟用绿矾制硫酸的实验,并检验生成的硫酸和二氧化硫,b为干燥的试管,加热装置已略去。下列有关说法错误的是
,三氧化硫的沸点为44.8℃)。用如图所示的装置模拟用绿矾制硫酸的实验,并检验生成的硫酸和二氧化硫,b为干燥的试管,加热装置已略去。下列有关说法错误的是
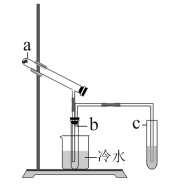

| A.若将反应后的三种气体通入 |
| B.b的作用是使三氧化硫液化,只是发生了物理变化 |
| C.为检验反应的另一种生成物,试管c中应加入的试剂为品红溶液 |
| D.b中所得到的硫酸的质量分数约为29.5% |
绿矾在高温下易分解,用右图装置检验绿矾的分解产物【加热装置已略去】。化学方程式为:2FeSO4·7H2O Fe2O3+SO2↑+SO3↑+14H2O。二氧化硫的沸点为-10℃,三氧化硫的沸点为44.8℃。其中b为干燥的试管。下列有关说法不正确的是
Fe2O3+SO2↑+SO3↑+14H2O。二氧化硫的沸点为-10℃,三氧化硫的沸点为44.8℃。其中b为干燥的试管。下列有关说法不正确的是
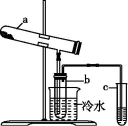
 Fe2O3+SO2↑+SO3↑+14H2O。二氧化硫的沸点为-10℃,三氧化硫的沸点为44.8℃。其中b为干燥的试管。下列有关说法不正确的是
Fe2O3+SO2↑+SO3↑+14H2O。二氧化硫的沸点为-10℃,三氧化硫的沸点为44.8℃。其中b为干燥的试管。下列有关说法不正确的是
| A.SO2是还原产物,Fe2O3是氧化产物 |
| B.b中所得到的硫酸的质量分数理论上为29.5% |
| C.将反应后的气体通入氯化钡溶液中,产生的沉淀为BaSO3、BaSO4 |
| D.将反应后的气体通入硝酸钡溶液中,产生的沉淀为只有BaSO4 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


