填空题 适中0.65 引用1 组卷90
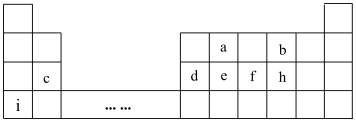
如表所示为元素周期表的前四周期部分,根据图示结合所学知识回答下列问题:
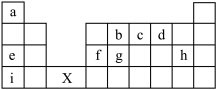
(1)h、i的简单离子半径由大到小的顺序为_______ (填离子符号)。
(2)i、e、f的最高价氧化物对应的水化物的碱性由强到弱的顺序是_______ (填化学式)。
(3)用电子式表示e和h形成离子化合物的过程:________ 。
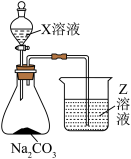
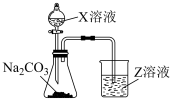
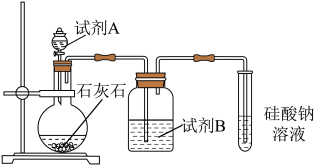
(4)非金属性:b_______ g(填“>”或“<”);以如图装置进行实验比较b、g对应的最高价氧化物对应水化物的酸性,则试剂A为_______ (填试剂名称),试剂B为_______ 。
(5)X处包含_______ 纵列,_______ 个族。
(6)i单质与d的简单氢化物反应的离子方程式为_______ 。

(1)h、i的简单离子半径由大到小的顺序为
(2)i、e、f的最高价氧化物对应的水化物的碱性由强到弱的顺序是
(3)用电子式表示e和h形成离子化合物的过程:
(4)非金属性:b

(5)X处包含
(6)i单质与d的简单氢化物反应的离子方程式为
23-24高一下·江西赣州·阶段练习
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网