解答题-原理综合题 适中0.65 引用1 组卷96
回答下列问题:
(1)工业上常用磷精矿[Ca5(PO4)3F]和硫酸反应制备磷酸。已知25℃,101kPa时:
CaO(s)+H2SO4(l)=CaSO4(s)+H2O(l) ΔH= -271 kJ·mol-1
5CaO(s)+3H3PO4(l)+HF(g)= Ca5(PO4)3F(s)+5H2O(l) ΔH= -937 kJ·mol-1
则Ca5(PO4)3F和硫酸反应生成磷酸的热化学方程式是_______ 。
(2)已知:25℃时, 常温下,将pH和体积均相同的
常温下,将pH和体积均相同的 和
和 溶液分别稀释,溶液pH随加水体积的变化如图:
溶液分别稀释,溶液pH随加水体积的变化如图:
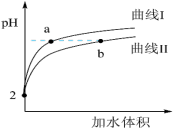
①曲线I代表_______ 溶液(填“ ”或“
”或“ ”)。
”)。
②a、b两点对应的溶液中,水的电离程度a_______ b(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
③向上述 溶液和
溶液和 溶液分别滴加等浓度的
溶液分别滴加等浓度的 溶液,当恰好中和时,消耗
溶液,当恰好中和时,消耗 溶液体积分别为
溶液体积分别为 和
和 ,则
,则
_______  (填“
(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
④酸度( )也可表示溶液的酸碱性,
)也可表示溶液的酸碱性, 。常温下,
。常温下, 的硝酸溶液AG=
的硝酸溶液AG=_______ 。
(3)雪碧是一款柠檬味汽水饮料,其中所含酸性物质包括:碳酸、柠檬酸、苯甲酸。25℃时,上述三种酸的电离常数如表所示:
①三种酸的酸性由强到弱的顺序为_______ (填标号)。
a.苯甲酸 b.碳酸 c.柠檬酸
②欲使水的平衡向右移动,且溶液显碱性,下列符合条件的方法是_______ (填标号)。
A.通入氨气 B.加入Na C.加入苯甲酸钠 固体 D.加热至90℃
固体 D.加热至90℃
(4)亚磷酸H3PO3是一种二元弱酸,可用作还原剂、尼龙增白剂、亚磷酸盐原料、农药中间体以及有机磷水处理药剂的原料。常温下,已知H3PO3溶液中含磷粒子的浓度之和为0.1mol·L-1,溶液中含磷粒子的物质的量分数(δ)与溶液pH的关系如图所示。
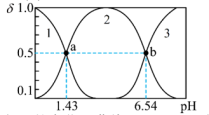
①写出亚磷酸H3PO3的第一步电离方程式_______ 。
② 随溶液pH的变化用曲线
随溶液pH的变化用曲线_______ (填“1”、“2”或“3”)表示。
③反应 的平衡常数K=
的平衡常数K=_______ 。
(1)工业上常用磷精矿[Ca5(PO4)3F]和硫酸反应制备磷酸。已知25℃,101kPa时:
CaO(s)+H2SO4(l)=CaSO4(s)+H2O(l) ΔH= -271 kJ·mol-1
5CaO(s)+3H3PO4(l)+HF(g)= Ca5(PO4)3F(s)+5H2O(l) ΔH= -937 kJ·mol-1
则Ca5(PO4)3F和硫酸反应生成磷酸的热化学方程式是
(2)已知:25℃时,

①曲线I代表
②a、b两点对应的溶液中,水的电离程度a
③向上述
④酸度(
(3)雪碧是一款柠檬味汽水饮料,其中所含酸性物质包括:碳酸、柠檬酸、苯甲酸。25℃时,上述三种酸的电离常数如表所示:
| 化学式 | 苯甲酸 | 碳酸 | 柠檬酸 |
| 电离常数 |
a.苯甲酸 b.碳酸 c.柠檬酸
②欲使水的平衡向右移动,且溶液显碱性,下列符合条件的方法是
A.通入氨气 B.加入Na C.加入苯甲酸钠
(4)亚磷酸H3PO3是一种二元弱酸,可用作还原剂、尼龙增白剂、亚磷酸盐原料、农药中间体以及有机磷水处理药剂的原料。常温下,已知H3PO3溶液中含磷粒子的浓度之和为0.1mol·L-1,溶液中含磷粒子的物质的量分数(δ)与溶液pH的关系如图所示。

①写出亚磷酸H3PO3的第一步电离方程式
②
③反应
23-24高二上·福建泉州·阶段练习
类题推荐
乙酸、碳酸、次氯酸、草酸在生产、生活及医药方面有广泛用途。回答下列问题:
I.已知25℃时,部分物质的电离常数如表所示:
(1)a.CH3COOH、b.H2CO3、c.HClO的酸性由强到弱的顺序为_______ (填编号)。
(2)水存在如下平衡:H2O+H2O⇌H3O++OH-ΔH>0,现欲使平衡向右移动,结果使溶液显碱性,应选择方法_______ 。
A.向水中加入NaHSO4固体 B.向水中加入NaOH固体 C.加热至100℃ D.向水中加入Na
(3)NaClO溶液显碱性的原因(用化学用语表示)_______ 。
(4)向NaClO溶液中通入少量的CO2,反应的离子方程式为_______ 。
(5)pH相同等体积的下列三种物质的溶液:a.HCl,b.H2SO4,c.CH3COOH滴加等浓度的NaOH溶液将它们恰好中和,用去NaOH溶液的体积分别为V1、V2、V3则三者的大小关系_______ 。
A.V3>V2>V1 B.V3=V2=V1 C.V3>V2=V1 D.V1=V2>V3
(6)25℃时,有两种溶液:①0.10mol·L-1CH3COOH溶液,②Na2CO3溶液,下列说法正确的是_______ (填字母)。
A.CH3COOH和Na2CO3都属于强电解质
B.①中:c(CH3COOH)+c(CH3COO-) = 0.10mol·L-1
C.②中:c(Na+)>c(OH-)>c(CO ) > c(HCO
) > c(HCO )>c(H+)
)>c(H+)
II.乙二酸(H2C2O4)俗称草酸,在实验研究和化学工业中应用广泛。
(1)室温下,测得0.1 mol·L-1 H2C2O4溶液的pH =1.3,写出草酸的电离方程式_______ 。
(2)草酸溶液中各粒子的物质的量分数随溶液pH变化关系如图所示:
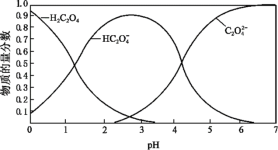
①向草酸溶液中滴加KOH溶液至pH=2.5时发生的主要反应的离子方程式是_______ 。
②0.1 mol·L-1 KHC2O4溶液中,下列粒子浓度关系正确的是_______ (填序号)。
a.c(K+)+c(H+)=c(HC2O )+c(C2O
)+c(C2O )+c(OH-)
)+c(OH-)
b.c(K+)>c(HC2O ) > c(C2O
) > c(C2O ) > c(H2C2O4)
) > c(H2C2O4)
c.c(K+)=c(HC2O ) + c(C2O
) + c(C2O )+c(H2C2O4)
)+c(H2C2O4)
(3)工业上利用硫酸亚铁与草酸反应制备草酸亚铁晶体,其离子方程式为:Fe2++H2C2O4+xH2O FeC2O4·xH2O↓+2H+
FeC2O4·xH2O↓+2H+
①制备时需添加氨水以提高FeC2O4·xH2O的产率,从化学平衡移动原理角度解释原因:_______ 。
②测定草酸亚铁晶体(FeC2O4·xH2O)的x值,实验如下:称取0.5400 g草酸亚铁晶体溶于一定浓度的硫酸中,用KMnO4酸性溶液滴定。到达滴定终点时,消耗0.1000 mol·L-1的KMnO4酸性溶液18.00 mL。已知:滴定过程中铁、碳元素被氧化为Fe3+、CO2,锰元素被还原为Mn2+,则FeC2O4·xH2O中x=_______ (FeC2O4的摩尔质量是144 g·mol-1)。
I.已知25℃时,部分物质的电离常数如表所示:
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离常数 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
(2)水存在如下平衡:H2O+H2O⇌H3O++OH-ΔH>0,现欲使平衡向右移动,结果使溶液显碱性,应选择方法
A.向水中加入NaHSO4固体 B.向水中加入NaOH固体 C.加热至100℃ D.向水中加入Na
(3)NaClO溶液显碱性的原因(用化学用语表示)
(4)向NaClO溶液中通入少量的CO2,反应的离子方程式为
(5)pH相同等体积的下列三种物质的溶液:a.HCl,b.H2SO4,c.CH3COOH滴加等浓度的NaOH溶液将它们恰好中和,用去NaOH溶液的体积分别为V1、V2、V3则三者的大小关系
A.V3>V2>V1 B.V3=V2=V1 C.V3>V2=V1 D.V1=V2>V3
(6)25℃时,有两种溶液:①0.10mol·L-1CH3COOH溶液,②Na2CO3溶液,下列说法正确的是
A.CH3COOH和Na2CO3都属于强电解质
B.①中:c(CH3COOH)+c(CH3COO-) = 0.10mol·L-1
C.②中:c(Na+)>c(OH-)>c(CO
II.乙二酸(H2C2O4)俗称草酸,在实验研究和化学工业中应用广泛。
(1)室温下,测得0.1 mol·L-1 H2C2O4溶液的pH =1.3,写出草酸的电离方程式
(2)草酸溶液中各粒子的物质的量分数随溶液pH变化关系如图所示:

①向草酸溶液中滴加KOH溶液至pH=2.5时发生的主要反应的离子方程式是
②0.1 mol·L-1 KHC2O4溶液中,下列粒子浓度关系正确的是
a.c(K+)+c(H+)=c(HC2O
b.c(K+)>c(HC2O
c.c(K+)=c(HC2O
(3)工业上利用硫酸亚铁与草酸反应制备草酸亚铁晶体,其离子方程式为:Fe2++H2C2O4+xH2O
①制备时需添加氨水以提高FeC2O4·xH2O的产率,从化学平衡移动原理角度解释原因:
②测定草酸亚铁晶体(FeC2O4·xH2O)的x值,实验如下:称取0.5400 g草酸亚铁晶体溶于一定浓度的硫酸中,用KMnO4酸性溶液滴定。到达滴定终点时,消耗0.1000 mol·L-1的KMnO4酸性溶液18.00 mL。已知:滴定过程中铁、碳元素被氧化为Fe3+、CO2,锰元素被还原为Mn2+,则FeC2O4·xH2O中x=
雪碧、可乐是深受人们青睐的碳酸型饮料。
I.雪碧是一款柠檬味汽水饮料,其中所含酸性物质包括碳酸、柠檬酸、苯甲酸。25℃时,上述三种酸的电离常数如表所示:
(1)上述三种酸的酸性由强到弱的顺序为______ (填字母)。
a.苯甲酸 b.碳酸 c.柠檬酸
(2)水中存在平衡:H2O H++OH-,欲使平衡向右移动且溶液显碱性,下列方法可行的是
H++OH-,欲使平衡向右移动且溶液显碱性,下列方法可行的是______ (填字母)。
a.通入氯气 b.加入钠 c.加热至90℃ d.加入Na2CO3固体
II.可乐中的食品添加剂有白砂糖、二氧化碳、焦糖、磷酸、咖啡因等。可乐的辛辣味与磷酸(化学式为H3PO4,沸点高难挥发)有一定关系。
(3)室温下,测得0.1mol/LH3PO4溶液的pH=1.5,原因是______ (用电离方程式表示)。
(4)长期过量饮用可乐会破坏牙釉质,造成龋齿。已知Ca5(PO4)3(OH)(s) 5Ca2+(aq)+3PO
5Ca2+(aq)+3PO (aq)+OH-(aq),结合平衡移动原理解释造成龋齿的原因
(aq)+OH-(aq),结合平衡移动原理解释造成龋齿的原因______ 。
(5)室温下,向磷酸溶液中滴加NaOH溶液,各含磷微粒在溶液中的物质的量分数与pH的关系如图所示。
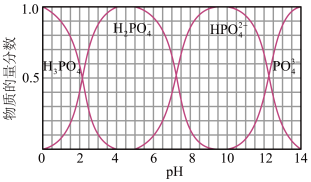
①当溶液pH由11到14时,发生反应的离子方程式为______ 。
②pH=3时,溶液中 =
=______ 。
I.雪碧是一款柠檬味汽水饮料,其中所含酸性物质包括碳酸、柠檬酸、苯甲酸。25℃时,上述三种酸的电离常数如表所示:
| 物质 | 苯甲酸(C6H5COOH) | 碳酸(H2CO3) | 柠檬酸(C6H8O7) |
| 电离常数 | Ka=6.3×10-5 | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka1=7.4×10-4 Ka2=1.7×10-5 Ka3=4.0×10-7 |
(1)上述三种酸的酸性由强到弱的顺序为
a.苯甲酸 b.碳酸 c.柠檬酸
(2)水中存在平衡:H2O
a.通入氯气 b.加入钠 c.加热至90℃ d.加入Na2CO3固体
II.可乐中的食品添加剂有白砂糖、二氧化碳、焦糖、磷酸、咖啡因等。可乐的辛辣味与磷酸(化学式为H3PO4,沸点高难挥发)有一定关系。
(3)室温下,测得0.1mol/LH3PO4溶液的pH=1.5,原因是
(4)长期过量饮用可乐会破坏牙釉质,造成龋齿。已知Ca5(PO4)3(OH)(s)
(5)室温下,向磷酸溶液中滴加NaOH溶液,各含磷微粒在溶液中的物质的量分数与pH的关系如图所示。

①当溶液pH由11到14时,发生反应的离子方程式为
②pH=3时,溶液中
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


