解答题-实验探究题 适中0.65 引用1 组卷124
亚硝酸钠(NaNO2)用途很广泛:可制药,作食品防腐剂、显色剂,作印染工业的媒染剂、漂白剂、缓蚀剂等,某兴趣小组欲制备亚硝酸钠并进行一定的实验探究,查阅资料可知:① ;②
;② ;③
;③ 可被酸性
可被酸性 氧化成
氧化成 ,现用下图所示装置制备
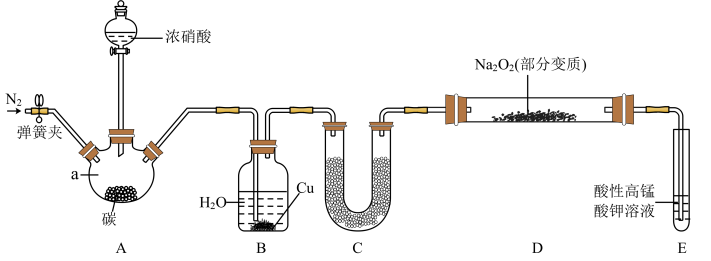
,现用下图所示装置制备 :
:
(1)连接仪器之后,加入药品之前需要进行的操作是_____ ;过氧化钠的电子式是_____ 。
(2)仪器B中Cu的作用是_____ 。(用离子方程式表示)
(3)U形管C中的试剂可以是_____ 。
(4)试管E中反应的离子方程式为_____ 。
(5)以上装置有设计缺陷,会使产品NaNO2中杂质增多,改进方法是_____ 。

(1)连接仪器之后,加入药品之前需要进行的操作是
(2)仪器B中Cu的作用是
(3)U形管C中的试剂可以是
(4)试管E中反应的离子方程式为
(5)以上装置有设计缺陷,会使产品NaNO2中杂质增多,改进方法是
23-24高三上·广东揭阳·阶段练习
类题推荐
亚硝酸钠(NaNO2)用途很广泛:可制药,作食品防腐剂、显色剂,作印染工业的媒染剂、漂白剂、缓蚀剂等。某兴趣小组欲制备亚硝酸钠并进行一定的实验探究,查阅资料可知:① ;②
;② ;③NO可被酸性KMnO4氧化成
;③NO可被酸性KMnO4氧化成 。
。
【制备NaNO2】
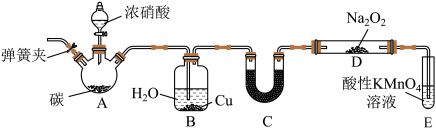
用下图所示装置制备NaNO2:
(1)过氧化钠的电子式是_____ 。
(2)仪器B中Cu的作用是_____ 。
(3)U形管C中的试剂可以是_____ 。
(4)试管E中反应的离子方程式为_____ 。
(5)以上装置有设计缺陷,会使产品NaNO2中杂质增多。改进方法是_____ 。
【测定NaNO2纯度】
(6)①称量0.5000g制得的样品,溶于水配成500mL溶液;
②取25.00mL待测液于锥形瓶中,加入足量KI酸性溶液,滴入2~3滴淀粉溶液;
③取一支_____ (填“酸”或“碱”)式滴定管用蒸馏水洗净后,用0.01mol/LNa2S2O3溶液润洗,装液,排出下端尖嘴内的气泡,调整液面,记下读数:
④进行滴定,记录读数。重复实验后,平均消耗Na2S2O3溶液的体积为20.00mL。(已知: ;
; )
)
(7)下列情况可能会使测得的NaNO2纯度偏低的是_____(填标号)。
(8)样品中NaNO2的质量分数为_____ 。
【制备NaNO2】
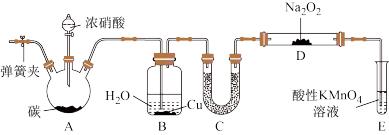
用下图所示装置制备NaNO2:

(1)过氧化钠的电子式是
(2)仪器B中Cu的作用是
(3)U形管C中的试剂可以是
(4)试管E中反应的离子方程式为
(5)以上装置有设计缺陷,会使产品NaNO2中杂质增多。改进方法是
【测定NaNO2纯度】
(6)①称量0.5000g制得的样品,溶于水配成500mL溶液;
②取25.00mL待测液于锥形瓶中,加入足量KI酸性溶液,滴入2~3滴淀粉溶液;
③取一支
④进行滴定,记录读数。重复实验后,平均消耗Na2S2O3溶液的体积为20.00mL。(已知:
(7)下列情况可能会使测得的NaNO2纯度偏低的是_____(填标号)。
| A.操作②中使用的锥形瓶未干燥 |
| B.操作③中未排尽下端尖嘴内的气泡 |
| C.操作④当滴入半滴Na2S2O3溶液,溶液由蓝色变为无色时,立即停止滴定 |
| D.整个滴定操作过慢,用时过长 |
(8)样品中NaNO2的质量分数为
亚硝酸钠(NaNO2)用途很广泛:可制药;作食品防腐剂、显色剂;作印染工业的媒染剂、漂白剂、缓蚀剂等。某兴趣小组欲制备亚硝酸钠并进行实验探究,查阅资料可知:
①Na2O2+2NO=2NaNO2;②Na2O2+2NO2=2NaNO3;③NO可被酸性KMnO4氧化成 。
。
【制备NaNO2】装置如图:
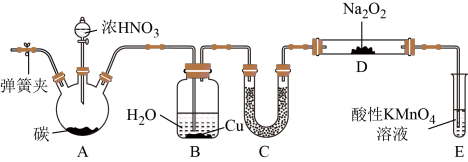
(1)Na2O2是___________ (填“共价化合物”或“离子化合物”)。
(2)U形管C中的试剂可以是___________ 。
(3)试管E中反应的离子方程式为___________ 。
(4)以上装置有设计缺陷,会使产品中杂质增多。改进方法是___________ 。
【测定某NaNO2样品纯度】
(5)①称量0.5000 g某NaNO2样品(假设杂质不反应),溶于水配成500 mL溶液。
②取25.00 mL待测液于锥形瓶中,加入足量KI酸性溶液,滴入2~3滴淀粉溶液。
③取一支______ (填“酸”或“碱”)式滴定管用蒸馏水洗净后,用0.0100 mol/L Na2S2O3溶液润洗,装液,排出下端尖嘴内的气泡,调整液面,记下读数。
④进行滴定,记录读数。重复实验后,平均消耗Na2S2O3溶液的体积为30.00 mL。(已知:2 +2I-+4H+=2NO+I2+2H2O;2Na2S2O3+I2=2NaI+Na2S4O6)。
+2I-+4H+=2NO+I2+2H2O;2Na2S2O3+I2=2NaI+Na2S4O6)。
(6)样品中NaNO2的质量分数为___________ 。
(7)下列情况可能会使测得的NaNO2纯度偏低的是___________(填标号)。
①Na2O2+2NO=2NaNO2;②Na2O2+2NO2=2NaNO3;③NO可被酸性KMnO4氧化成
【制备NaNO2】装置如图:
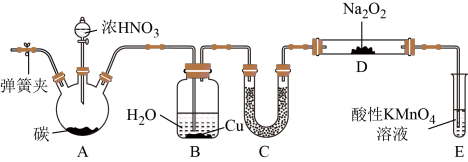
(1)Na2O2是
(2)U形管C中的试剂可以是
(3)试管E中反应的离子方程式为
(4)以上装置有设计缺陷,会使产品中杂质增多。改进方法是
【测定某NaNO2样品纯度】
(5)①称量0.5000 g某NaNO2样品(假设杂质不反应),溶于水配成500 mL溶液。
②取25.00 mL待测液于锥形瓶中,加入足量KI酸性溶液,滴入2~3滴淀粉溶液。
③取一支
④进行滴定,记录读数。重复实验后,平均消耗Na2S2O3溶液的体积为30.00 mL。(已知:2
(6)样品中NaNO2的质量分数为
(7)下列情况可能会使测得的NaNO2纯度偏低的是___________(填标号)。
| A.操作②中使用的锥形瓶未干燥 |
| B.操作③中未排尽下端尖嘴内的气泡 |
| C.操作④当滴入半滴Na2S2O3溶液,溶液由蓝色变为无色时,立即停止滴定 |
| D.整个滴定操作过慢,用时过长 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网