解答题-原理综合题 较难0.4 引用2 组卷477
以 为原料在特定条件下可生产醇类、烷烃、碳酸酯等,实现二氧化碳资源化。科学家通过如下反应合成甲醇:
为原料在特定条件下可生产醇类、烷烃、碳酸酯等,实现二氧化碳资源化。科学家通过如下反应合成甲醇: 。
。
已知:



回答下列问题:
(1)计算上述合成甲醇反应的焓变
______  。
。
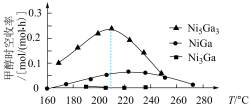
(2)科学研究中常用产物的时空收率(单位物质的量催化剂表面产物分子的平均生成速率)来衡量催化效果.在3 MPa, 时,不同Ni、Ga配比的Ni-Ga/
时,不同Ni、Ga配比的Ni-Ga/ 催化剂下,测定甲醇时空收率随温度的变化曲线如图所示.甲醇时空收率随温度变化先增大后减小的原因是
催化剂下,测定甲醇时空收率随温度的变化曲线如图所示.甲醇时空收率随温度变化先增大后减小的原因是______ 。催化剂的最佳配比和反应温度是______ 。 和
和 充入恒温恒容密闭容器中反应合成甲醇,已知该温度下反应的化学平衡常数
充入恒温恒容密闭容器中反应合成甲醇,已知该温度下反应的化学平衡常数 ,下列事实说明该反应已达平衡的是______。
,下列事实说明该反应已达平衡的是______。
(4)① 合成
合成 存在以下副反应:
存在以下副反应: 。5MPa,200℃时在1 L容器中投入1 mol
。5MPa,200℃时在1 L容器中投入1 mol  和3 mol
和3 mol  ,达成平衡时,二氧化碳转化率为0.5,甲醇选择率为0.8(甲醇选择率=
,达成平衡时,二氧化碳转化率为0.5,甲醇选择率为0.8(甲醇选择率= )。计算合成甲醇反应的化学平衡常数K(写出过程,结果列出计算表达式)
)。计算合成甲醇反应的化学平衡常数K(写出过程,结果列出计算表达式)________________________ 。
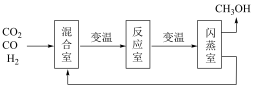
②已知200℃时有60%以上的原料未转化,为了提高转化率,设计如图流程分离甲醇和水,循环利用原料气。已知甲醇的沸点是64.7℃,根据信息判断反应室的温度______ 闪蒸室的温度(选填“<”、“=”或“>”).在原料气中通入CO的目的是________________________ 。
已知:
回答下列问题:
(1)计算上述合成甲醇反应的焓变
(2)科学研究中常用产物的时空收率(单位物质的量催化剂表面产物分子的平均生成速率)来衡量催化效果.在3 MPa,
| A.气体密度保持不变 |
| B. |
| C.某时刻容器中 |
| D.混合气体的平均相对分子质量不变 |
②已知200℃时有60%以上的原料未转化,为了提高转化率,设计如图流程分离甲醇和水,循环利用原料气。已知甲醇的沸点是64.7℃,根据信息判断反应室的温度
2024·广东佛山·一模
类题推荐  不仅是一种温室气体,也是一种来源广泛且廉价易得的碳资源,可通过热化学、电化学等方法再利用。
不仅是一种温室气体,也是一种来源广泛且廉价易得的碳资源,可通过热化学、电化学等方法再利用。
(Ⅰ)科学家通过如下反应利用 合成甲醇:
合成甲醇:
已知:

回答下列问题:
(1)计算上述合成甲醇反应的焓变
___________  。
。
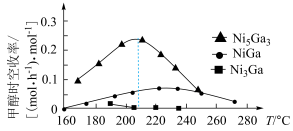
(2)科学研究中常用产物的时空收率(单位物质的量催化剂表面产物分子的平均生成速率)来衡量催化效果,在3MPa, 时,不同Ni、Ga配比的
时,不同Ni、Ga配比的 催化剂下,测定甲醇时空收率随温度的变化曲线如图所示,甲醇时空收率随温度变化先增大后减小的原因是
催化剂下,测定甲醇时空收率随温度的变化曲线如图所示,甲醇时空收率随温度变化先增大后减小的原因是___________ 。催化剂的最佳配比和反应温度是___________ 。 和
和 充入恒温恒容密闭容器中反应合成甲醇,已知该温度下反应的化学平衡常数
充入恒温恒容密闭容器中反应合成甲醇,已知该温度下反应的化学平衡常数 ,下列事实说明该反应已达平衡的是___________。
,下列事实说明该反应已达平衡的是___________。
(Ⅱ)甲烷干重整反应可以将两类重要的温室气体和 进行重整,涉及主要反应如下:
进行重整,涉及主要反应如下:
反应I:
反应Ⅱ:
(4)恒温恒容 密闭容器中,按
密闭容器中,按 投料,初始总压
投料,初始总压 ,达到平衡状态时测得
,达到平衡状态时测得 转化率为
转化率为 ,平衡总压为
,平衡总压为 。计算该温度下反应Ⅰ的浓度平衡常数
。计算该温度下反应Ⅰ的浓度平衡常数
___________  。
。
(5)某研究小组为了评估甲烷干重整反应中不同催化剂的性能差异,在常压、催化剂作用下,按 投料,不同温度下反应相同时间,测得
投料,不同温度下反应相同时间,测得 的转化率(柱形图)和产物
的转化率(柱形图)和产物 (
( )如图所示。请分析产物
)如图所示。请分析产物 随温度变化的原因(不考虑催化剂失活)
随温度变化的原因(不考虑催化剂失活)___________ 。  的资源化利用能有效助力“碳中和”和“碳达峰”,工业上用
的资源化利用能有效助力“碳中和”和“碳达峰”,工业上用 与
与 催化合成甲醇,相关反应如下:
催化合成甲醇,相关反应如下:
请回答下列问题:
(1)
___________ (用含 、
、 的代数式表示)。
的代数式表示)。
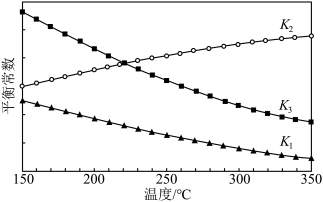
(2)已知平衡常数 、
、 、
、 随温度变化的曲线如图所示:
随温度变化的曲线如图所示:
①
___________ 0(填“>”或“<”),判断依据为___________ 。
②
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(3)一定温度下,向2 L的恒容密闭容器中充入3 mol 和1 mol
和1 mol  ,只发生反应ⅰ和ⅱ,经过10 min后达到平衡状态,测得平衡时气体的压强是开始时的0.7倍,
,只发生反应ⅰ和ⅱ,经过10 min后达到平衡状态,测得平衡时气体的压强是开始时的0.7倍, 的平衡转化率为80%。
的平衡转化率为80%。
①0~10min内用 表示的平均反应速率
表示的平均反应速率
___________  。
。
②平衡时
___________  。该温度下反应ⅱ的化学平衡常数
。该温度下反应ⅱ的化学平衡常数
___________ 。
(4)在催化剂作用下,向某密闭容器中按 投料,发生反应ⅰ、ⅱ和ⅲ,研究发现,在180~250℃温度区域,随温度升高,平衡时混合气体的平均摩尔质量持续减小,在250℃以上区域,平衡时混合气体的平均摩尔质量几乎不变。试分析,250℃以上区域,随温度升高,平衡时混合气体的平均摩尔质量几乎不变的原因可能是
投料,发生反应ⅰ、ⅱ和ⅲ,研究发现,在180~250℃温度区域,随温度升高,平衡时混合气体的平均摩尔质量持续减小,在250℃以上区域,平衡时混合气体的平均摩尔质量几乎不变。试分析,250℃以上区域,随温度升高,平衡时混合气体的平均摩尔质量几乎不变的原因可能是___________ 。
(Ⅰ)科学家通过如下反应利用
已知:
回答下列问题:
(1)计算上述合成甲醇反应的焓变
(2)科学研究中常用产物的时空收率(单位物质的量催化剂表面产物分子的平均生成速率)来衡量催化效果,在3MPa,
| A.气体密度保持不变 |
| B. |
| C.某时刻容器中 |
| D.混合气体的平均相对分子质量不变 |
(Ⅱ)甲烷干重整反应可以将两类重要的温室气体和
反应I:
反应Ⅱ:
(4)恒温恒容
(5)某研究小组为了评估甲烷干重整反应中不同催化剂的性能差异,在常压、催化剂作用下,按
 )如图所示。请分析产物
)如图所示。请分析产物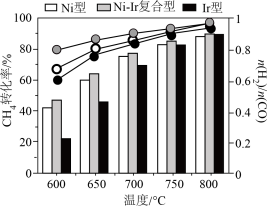
二氧化碳与氢气催化合成甲醇,发生的反应为:CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
(1)已知:
计算上述反应的△H=_________________ kJ.mol-1。
(2)一定条件下,将n(CO2):n(H2)=1:1的混合气充入恒温恒容密闭容器中,下列事实可以说明该反应已达平衡的是______________________ (填选项字母)。
A.容器内气体密度保持不变
B.CO2的体积分数保持不变
C.H2O(g)与CO2(g)的生成速率之比为1∶1
D.该反应的平衡常数保持不变
E.混合气体的平均相对分子质量不变
F.容器中压强保持不变
(3)一定条件下,往2L恒容密闭容器中充入1.2molCO2和3.6molH2,在不同催化剂作用下的反应I、反应II与反应III,相同时间内CO2转化率随温度变化的数据如表所示,据表中数据绘制“图1”:
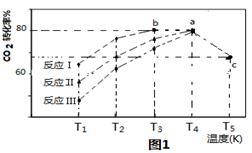
(T5时,图1中C点转化率为66.67%,即转化了2/3)
①催化剂效果最佳的反应是_______________ (填“反应I”,“反应II”,“反应III”)。
②T3的b点v(正)_____________ v(逆)(填 “>”, “<”, “="”" )。
③T4的a点转化率比T5的c点高的原因是________________________ 。
④在温度为T5时,该反应的平衡常数K=__________________________ 。
⑤在温度为T5时,CH3OH的浓度随时间变化的趋势如“图2”所示。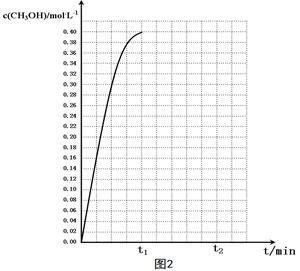
当时间到达t1时,将生成的甲醇和水同时除去,并维持该温度,在 t2时达新平衡。
请在“图2”中画出t1时刻后CH3OH的浓度变化总趋势曲线。
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)(1)已知:
| 化学键 | H-H | C-O | C=O | H-O | C-H |
| 键能/kJ·mol-1 | 436 | 326 | 803 | 464 | 414 |
(2)一定条件下,将n(CO2):n(H2)=1:1的混合气充入恒温恒容密闭容器中,下列事实可以说明该反应已达平衡的是
A.容器内气体密度保持不变
B.CO2的体积分数保持不变
C.H2O(g)与CO2(g)的生成速率之比为1∶1
D.该反应的平衡常数保持不变
E.混合气体的平均相对分子质量不变
F.容器中压强保持不变
(3)一定条件下,往2L恒容密闭容器中充入1.2molCO2和3.6molH2,在不同催化剂作用下的反应I、反应II与反应III,相同时间内CO2转化率随温度变化的数据如表所示,据表中数据绘制“图1”:
| 相同时间内CO2转化率 | T1 | T2 | T3 | T4 | T5 |
| 反应Ⅰ | 65% | 77% | 80% | 80% | 66.67% |
| 反应Ⅱ | 56% | 67% | 76% | 80% | 66.67% |
| 反应Ⅲ | 48% | 62% | 72% | 80% | 66.67% |

(T5时,图1中C点转化率为66.67%,即转化了2/3)
①催化剂效果最佳的反应是
②T3的b点v(正)
③T4的a点转化率比T5的c点高的原因是
④在温度为T5时,该反应的平衡常数K=
⑤在温度为T5时,CH3OH的浓度随时间变化的趋势如“图2”所示。

当时间到达t1时,将生成的甲醇和水同时除去,并维持该温度,在 t2时达新平衡。
请在“图2”中画出t1时刻后CH3OH的浓度变化总趋势曲线。
| 相关反应 | 化学平衡常数(K) | ||
| ⅰ | |||
| ⅱ | |||
| ⅲ |
(1)
(2)已知平衡常数

①
②
(3)一定温度下,向2 L的恒容密闭容器中充入3 mol
①0~10min内用
②平衡时
(4)在催化剂作用下,向某密闭容器中按
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


