解答题-原理综合题 较难0.4 引用2 组卷379
I:
Ⅱ:
Ⅲ:
Ⅳ:
回答下列问题:
(1)已知
(2)将一定体积
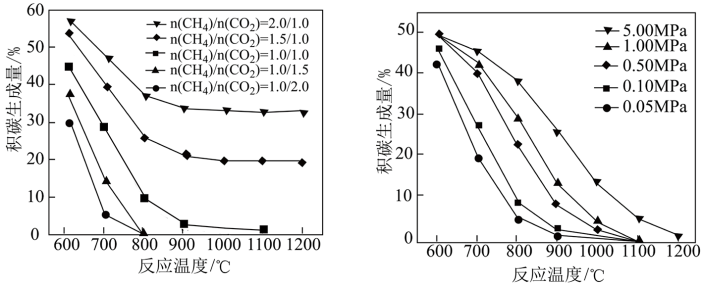
②下列说法正确的是
A.平衡后,移除部分积碳,Ⅲ和Ⅳ均向右移
B.保持其他条件不变,升温积碳量逐渐减小
C.温度一定时,增大投料比
D.温度一定时,增大投料比
2024·山东淄博·一模
类题推荐
我国力争2060年前实现碳中和。CH4与CO2催化重整是实现碳中和的热点研究课题。该催化重整反应体系主要涉及以下反应:
反应I:主反应CH4(g)+CO2(g) 2CO(g)+2H2(g) ΔH1 Kp1
2CO(g)+2H2(g) ΔH1 Kp1
反应II:副反应CO2(g)+H2(g) CO(g)+H2O(g) ΔH2 Kp2
CO(g)+H2O(g) ΔH2 Kp2
反应III:积碳反应2CO(g) CO2(g)+C(s) ΔH3 Kp3
CO2(g)+C(s) ΔH3 Kp3
反应IV:积碳反应CH4(g) C(s)+2H2(g) ΔH4 Kp4
C(s)+2H2(g) ΔH4 Kp4
(1)已知H2(g)、CO(g)的燃烧热ΔH分别为-285.8kJ·mol-1、-283.0lkJ·mol-1,H2O(l)= H2O(g) ΔH5=+44kJ·mol-1,则反应II的ΔH2=____ kJ·mol-1。
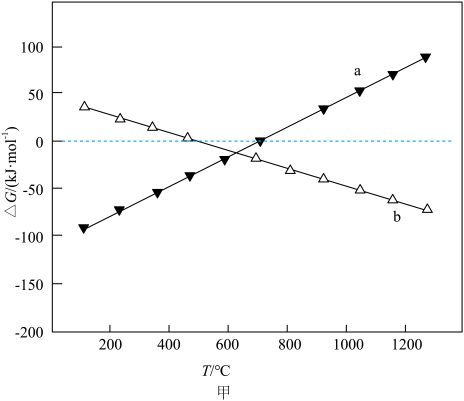
(2)设Kp为分压平衡常数(用分压代替浓度,气体分压=总压×该组分的物质的量分数),反应III、IV的lgKp随 (T表示温度)的变化如图所示。据图判断,反应I的ΔH1
(T表示温度)的变化如图所示。据图判断,反应I的ΔH1_____ 0(选填“大于”、“小于”或“等于”),说明判断的理由____ 。

(3)下列关于该重整反应体系的说法正确的是____ 。
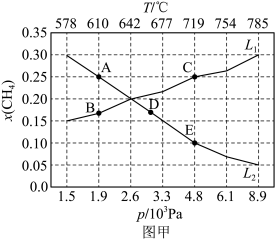
(4)在一定条件下的密闭容器中,按照 =1加入反应物,发生反应I(反应II、III、IV可忽略)。在不同条件下达到平衡,设体系中平衡状态下甲烷的物质的量分数为x(CH4),在T=800℃下的x(CH4)随压强P的变化曲线、在P=100kPa下的x(CH4)随温度T的变化曲线如图所示。
=1加入反应物,发生反应I(反应II、III、IV可忽略)。在不同条件下达到平衡,设体系中平衡状态下甲烷的物质的量分数为x(CH4),在T=800℃下的x(CH4)随压强P的变化曲线、在P=100kPa下的x(CH4)随温度T的变化曲线如图所示。

①图中对应T=800℃下,x(CH4)随压强P的变化曲线是____ ,判断的理由是____ 。
②若x(CH4)=0.1.则CO2的平衡转化率为____ 。
反应I:主反应CH4(g)+CO2(g)
反应II:副反应CO2(g)+H2(g)
反应III:积碳反应2CO(g)
反应IV:积碳反应CH4(g)
(1)已知H2(g)、CO(g)的燃烧热ΔH分别为-285.8kJ·mol-1、-283.0lkJ·mol-1,H2O(l)= H2O(g) ΔH5=+44kJ·mol-1,则反应II的ΔH2=
(2)设Kp为分压平衡常数(用分压代替浓度,气体分压=总压×该组分的物质的量分数),反应III、IV的lgKp随

(3)下列关于该重整反应体系的说法正确的是
| A.在投料时适当增大 |
| B.在一定条件下建立平衡后,移去部分积碳,反应III和反应IV平衡均向右移 |
| C.随着投料比 |
| D.降低反应温度,反应I、II、IV的正反应速率减小,逆反应速率增大;反应III的正反应速率增大,逆反应速率减小 |

①图中对应T=800℃下,x(CH4)随压强P的变化曲线是
②若x(CH4)=0.1.则CO2的平衡转化率为
甲醇是重要的化工基础原料和清洁液体燃料,工业上可利用CO或CO2来生产甲醇。已知制备甲醇的有关化学反应以及在不同温度下的化学平衡常数如表所示:
(1)在恒容密闭容器中发生反应②,达到平衡后升高温度,下列说法正确的是_______ 。
a.平衡正向移动 b.混合气体的平均相对分子质量增大 c.CO2的转化率增大
(2)K1、K2、K3的关系是:K3=_______ 。
(3)500℃时测得反应③在某时刻,H2(g)、CO2(g)、CH3OH(g)、H2O(g)的浓度(mol/L)分别为0.2、0.1、0.01、0.2,则此时v正_______ v逆(填“>”“=”或“<”)。
(4)某温度下在恒容密闭容器中发生反应①,若开始加入2mol/LH2和1mol/LCO,达到平衡时,H2的平衡转化率为80%,则此温度下,该反应的化学平衡常数为_______ 。
(5)相同温度下,在甲、乙两个容积相等的恒容密闭容器中,投入H2和CO2,发生反应②,起始浓度如表所示。其中甲经2min达平衡,平衡时c(H2O)=0.05mol/L,甲中CO2的转化率为_______ ,乙中CO2的转化率_______ (填“大于”、“等于”或“小于”)甲。
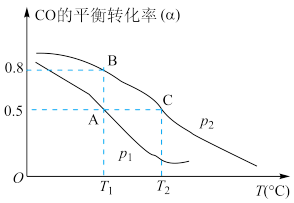
(6)在CO合成甲醇过程中,将10molCO与20molH2充入一容积可变的密闭容器中,在催化剂作用下发生反应生成甲醇。CO的平衡转化率(α)与温度(T)、压强(p)的关系如图所示。下列说法正确的是_______(填字母)。
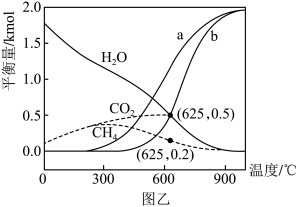
(7)工业上可利用CO或CO2来生产甲醇可能会产生积碳现象。如图表示不同温度条件下,反应Ⅰ: 发生后的汽气比(水蒸气与CO物质的量之比)与CO平衡转化率的变化关系。
发生后的汽气比(水蒸气与CO物质的量之比)与CO平衡转化率的变化关系。
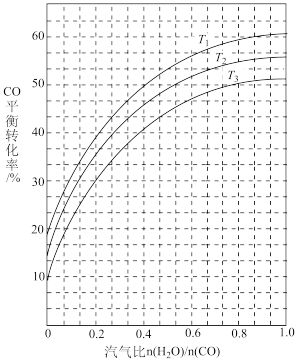
①判断 和
和 由大到小的关系为
由大到小的关系为_______ ;
②若经反应I发生后的汽气比为0.8,所得混合气体经反应II后,得到CO与H2的物质的量之比为 ,则反应II:
,则反应II: 应选择的温度是
应选择的温度是_______ (填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
| 化学反应 | 平衡常数 | 温度/ | |
| 500 | 800 | ||
| ①2H2(g)+CO(g) | K1 | 2.5 | 0.15 |
| ②H2(g)+CO2(g) | K2 | 1.0 | 2.50 |
| ③3H2(g)+CO2(g) | K3 | ||
(1)在恒容密闭容器中发生反应②,达到平衡后升高温度,下列说法正确的是
a.平衡正向移动 b.混合气体的平均相对分子质量增大 c.CO2的转化率增大
(2)K1、K2、K3的关系是:K3=
(3)500℃时测得反应③在某时刻,H2(g)、CO2(g)、CH3OH(g)、H2O(g)的浓度(mol/L)分别为0.2、0.1、0.01、0.2,则此时v正
(4)某温度下在恒容密闭容器中发生反应①,若开始加入2mol/LH2和1mol/LCO,达到平衡时,H2的平衡转化率为80%,则此温度下,该反应的化学平衡常数为
(5)相同温度下,在甲、乙两个容积相等的恒容密闭容器中,投入H2和CO2,发生反应②,起始浓度如表所示。其中甲经2min达平衡,平衡时c(H2O)=0.05mol/L,甲中CO2的转化率为
| 起始浓度 | 甲 | 乙 |
| c(H2)/mol/L | 0.10 | 0.20 |
| c(CO2)/mol/L | 0.10 | 0.20 |
(6)在CO合成甲醇过程中,将10molCO与20molH2充入一容积可变的密闭容器中,在催化剂作用下发生反应生成甲醇。CO的平衡转化率(α)与温度(T)、压强(p)的关系如图所示。下列说法正确的是_______(填字母)。

| A.合成甲醇的反应为吸热反应 |
| B.压强为p1>p2 |
| C.A、B、C三点的平衡常数为KA=KB>KC |
| D.若达平衡状态A时,容器的体积为10L,则在平衡状态B时容器的体积也为10L |

①判断
②若经反应I发生后的汽气比为0.8,所得混合气体经反应II后,得到CO与H2的物质的量之比为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网