填空题 适中0.65 引用1 组卷33
1913年,德国化学家哈伯实现了合成氨的工业化生产,被称作解救世界粮食危机的化学天才,现将1molN2和3molH2投入1L的密闭容器,在一定条件下,利用反应模拟哈伯合成氨的工业化生产:N2(g)+3H2(g) 2NH3(g)
2NH3(g)  H<0. 回答下列问题:
H<0. 回答下列问题:
(1)合成氨反应平衡常数的表达式为_______ 。温度升高,K值_______ (填“增大”“减小”或“不变"):使用催化剂,K值_______ (填“增大“减小”或“不变”)。
(2)反应的 S
S_______ 0(填“>”“<"或“=”)
(3)有利于提高平衡混合物中氨含量的条件有_______ (填序号)。
A.低温 B.高温 C.低压 D.高压 E.催化剂
(4)当反应达到平衡后,向体系中充入N2的,平衡_______ 移动(填“正向”“逆向”或“不”);给体系升温,
_______ (填“增大”“减小”或不变”),
_______ (填“增大”“减小”或“不变”),平衡_______ 移动(填“正向”“逆向”或“不”)。
(1)合成氨反应平衡常数的表达式为
(2)反应的
(3)有利于提高平衡混合物中氨含量的条件有
A.低温 B.高温 C.低压 D.高压 E.催化剂
(4)当反应达到平衡后,向体系中充入N2的,平衡
23-24高二上·广西桂林·期中
类题推荐
1913年,德国化学家哈伯实现了合成氨的工业化生产,被称作解救世界粮食危机的化学天才.现将lmolN2和3molH2投入1L的密闭容器,在一定条件下,利用如下反应模拟哈伯合成氨的工业化生产:N2(g)+3H2(g) 2NH3(g) ∆H<0。当改变某一外界条件(温度或压强)时,NH3的体积分数φ(NH3)变化趋势如图所示。
2NH3(g) ∆H<0。当改变某一外界条件(温度或压强)时,NH3的体积分数φ(NH3)变化趋势如图所示。
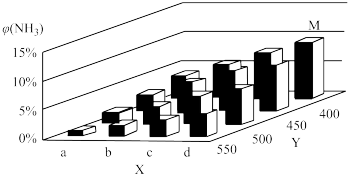
回答下列问题:
(1)已知:①NH3(l)=NH3(g) ∆H1,②N2(g)+3H2(g) 2NH3(l) ∆H2;则反应N2(g)+3H2(g)
2NH3(l) ∆H2;则反应N2(g)+3H2(g) 2NH3(g)的∆H=
2NH3(g)的∆H=____ (用含∆H1、∆H2的代数式表示);
(2)合成氨的平衡常数表达式为____ ,平衡时,M点NH3的体积分数为10%,则N2的转化率为____ (保留两位有效数字)。
(3)X轴上a点的数值比b点____ (填“大”或“小”)。图中,Y轴表示____ (填“温度”或“压强”),判断的理由是____ 。
(4)若将1molN2和3molH2分别投入起始容积为1L的密闭容器中,实验条件和平衡时的相关数据如表所示:
下列判断正确的是____ 。

回答下列问题:
(1)已知:①NH3(l)=NH3(g) ∆H1,②N2(g)+3H2(g)
(2)合成氨的平衡常数表达式为
(3)X轴上a点的数值比b点
(4)若将1molN2和3molH2分别投入起始容积为1L的密闭容器中,实验条件和平衡时的相关数据如表所示:
| 容器编号 | 实验条件 | 平衡时反应中的能量变化 |
| I | 恒温恒容 | 放热Q1kJ |
| II | 恒温恒压 | 放热Q2kJ |
| III | 恒容绝热 | 放热Q3kJ |
| A.放出热量:Ql<Q2<∆Hl | B.N2的转化率:I>III |
| C.平衡常数:II>I | D.达平衡时氨气的体积分数:I>II |
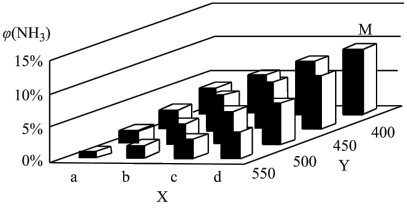
1913年,德国化学家哈伯实现了合成氨的工业化生产,被称作解救世界粮食危机的化学天才。现将lmolN2和3molH2投入1L的密闭容器,在一定条件下,利用如下反应模拟哈伯合成氨的工业化生产: N2(g) +3H2(g)  2NH3(g)△H < 0 当改变某一外界条件(温度或压强)时,NH3的体积分数φ(NH3)变化趋势如下图所示。
2NH3(g)△H < 0 当改变某一外界条件(温度或压强)时,NH3的体积分数φ(NH3)变化趋势如下图所示。
(1)已知:①NH3(l) NH3(g) ΔH1②N2(g)+3H2(g)
NH3(g) ΔH1②N2(g)+3H2(g)  2NH3(l) ΔH2,则反应N2(g)+3H2(g)
2NH3(l) ΔH2,则反应N2(g)+3H2(g)  2NH3(g)的△H=
2NH3(g)的△H=________ (用含△H1、△H2的代数式表示)。
(2)X轴上a点的数值比b点_____ (填“大”或“小”),Y轴表示_______ (填“温度”或“压强”)。
(3)将1mol N2和3mol H2分别投入起始容积为1L的密闭容器中,实验条件相关数据如下表所示:
下列判断正确的是________ 。
A.放出热量:Ql< Q2<|△H| B.N2的转化率:I> III
C.平衡常数:II >I D.达平衡时氨气的体积分数:I>II
(4)平衡时,M点NH3的体积分数为10%。若同温同容下,再充入0.2mol N2,0.6mol H2和1.6molNH 3,重新达平衡时NH3的体积分数________ 10%(填“>”、“<”、“=”或“无法确定”)。
(5)某科研小组探究在其他条件不变的情况下,改变起始物氢气的物质的量对合成NH3反应的影响.实验结果如图所示:(图中T2和T1表示温度,n表示起始时H2的物质的量)
①图象中T2和T1的关系是:T2_____ T1(填“>”、“<”、“=”或“无法确定”)。
②比较在a、b、c三点所处的平衡状态中,反应物N2的转化率最大的是___ (填字母)。
(1)已知:①NH3(l)
(2)X轴上a点的数值比b点
(3)将1mol N2和3mol H2分别投入起始容积为1L的密闭容器中,实验条件相关数据如下表所示:
| 容器编号 | 实验条件 | 平衡时反应中的能量变化 |
| I | 恒温恒容 | 放热Q1kJ |
| II | 恒温恒压 | 放热Q2kJ |
| III | 恒容绝热 | 放热Q3kJ |
A.放出热量:Ql< Q2<|△H| B.N2的转化率:I> III
C.平衡常数:II >I D.达平衡时氨气的体积分数:I>II
(4)平衡时,M点NH3的体积分数为10%。若同温同容下,再充入0.2mol N2,0.6mol H2和1.6molNH 3,重新达平衡时NH3的体积分数
(5)某科研小组探究在其他条件不变的情况下,改变起始物氢气的物质的量对合成NH3反应的影响.实验结果如图所示:(图中T2和T1表示温度,n表示起始时H2的物质的量)
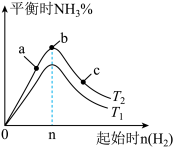
①图象中T2和T1的关系是:T2
②比较在a、b、c三点所处的平衡状态中,反应物N2的转化率最大的是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


