解答题-实验探究题 适中0.65 引用1 组卷25
实验室中经常用酸碱中和滴定的方法测定溶液的浓度。
I.NaOH标准溶液的配制
(1)用托盘天平称取2.0gNaOH固体,加500mL蒸馏水配成溶液,并放置冷却。实验过程中用到的玻璃仪器有量筒、烧杯、___________ 。
(2)现欲测定上述溶液的准确浓度,用准确称取的0.4080g邻苯二甲酸氢钾( ,摩尔质量为
,摩尔质量为 )溶于20mL水所得的溶液与该NaOH溶液反应,测得恰好完全反应时消耗该NaOH溶液的体积为20.20mL。则该溶液中NaOH的物质的量浓度为
)溶于20mL水所得的溶液与该NaOH溶液反应,测得恰好完全反应时消耗该NaOH溶液的体积为20.20mL。则该溶液中NaOH的物质的量浓度为___________  (已知:
(已知: ;计算结果保留4位有效数字,下同)。
;计算结果保留4位有效数字,下同)。
II.若用 的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:
的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:
①用蒸馏水洗涤碱式滴定管,注入 的标准NaOH溶液至“0”刻度线以上;
的标准NaOH溶液至“0”刻度线以上;
②固定好滴定管并使滴定管尖嘴充满液体,调节液面至“0”或“0”刻度线以下,并记下读数;
③量取20.00mL待测液注入洁净的锥形瓶中,并加入2滴甲基橙溶液;
④用标准液滴定至终点,记下滴定管液面读数;
⑤重复以上滴定操作2~3次。
(3)步骤①存在的错误是___________ 。
(4)步骤③中,量取20.00mL待测液应使用___________ (填标号)。
a.酸式滴定管 b.碱式滴定管 c.量筒
(5)步骤④中,判断到达滴定终点的依据是___________ 。
(6)若步骤①中操作正确,以下是实验数据记录表:
从表中可以看出,第1次滴定记录的NaOH溶液体积明显小于后两次的体积,其可能的原因是___________(填标号)。
(7)根据表中记录数据,通过计算可得盐酸浓度为___________  。
。
I.NaOH标准溶液的配制
(1)用托盘天平称取2.0gNaOH固体,加500mL蒸馏水配成溶液,并放置冷却。实验过程中用到的玻璃仪器有量筒、烧杯、
(2)现欲测定上述溶液的准确浓度,用准确称取的0.4080g邻苯二甲酸氢钾(
II.若用
①用蒸馏水洗涤碱式滴定管,注入
②固定好滴定管并使滴定管尖嘴充满液体,调节液面至“0”或“0”刻度线以下,并记下读数;
③量取20.00mL待测液注入洁净的锥形瓶中,并加入2滴甲基橙溶液;
④用标准液滴定至终点,记下滴定管液面读数;
⑤重复以上滴定操作2~3次。
(3)步骤①存在的错误是
(4)步骤③中,量取20.00mL待测液应使用
a.酸式滴定管 b.碱式滴定管 c.量筒
(5)步骤④中,判断到达滴定终点的依据是
(6)若步骤①中操作正确,以下是实验数据记录表:
| 滴定次数 | 盐酸体积/mL | NaOH溶液体积/mL | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.00 | 14.10 |
| 2 | 20.00 | 0.00 | 16.20 |
| 3 | 20.00 | 0.00 | 16.22 |
| A.锥形瓶装液前,留有少量蒸馏水 |
| B.取待测液时,有部分液体洒在锥形瓶外壁上 |
| C.滴定前滴定管尖嘴无气泡,滴定结束后有气泡 |
| D.NaOH标准液保存时间过长,有部分变质 |
23-24高二上·安徽淮北·期中
类题推荐
用0.2000mol/L的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:
①用蒸馏水洗涤碱式滴定管,注入0.2000mol/L的标准NaOH溶液至“0”刻度线以上;
②固定好滴定管并使滴定管尖嘴充满液体;
③调节液面至“0”或“0”刻度线以下,并记下读数;
④量取20.00mL待测液注入洁净的锥形瓶中,并加入2滴甲基橙溶液;
⑤用标准液滴定至终点,记下滴定管液面读数。
⑥重复以上滴定操作2-3次。
请回答
(1)以上步骤有错误的是(填编号)_______
(2)步骤④中,量取20.00mL待测液应使用_______ (填仪器名称)
(3)步骤⑤滴定时眼睛应注视_______ ;判断到达滴定终点的依据是:_______
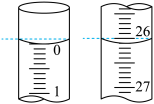
(4)若滴定开始和结束时,碱式滴定管中的液面如图所示:则所用氢氧化钠溶液的体积为_______ mL。
(5)以下是实验数据记录表
从表中可以看出,第1次滴定记录的NaOH溶液体积明显多于后两次的体积,其可能的原因是_______
A.锥形瓶装液前,留有少量蒸馏水
B.滴定结束时,仰视计数
C.滴定前滴定管尖嘴无气泡,滴定结束有气泡
D.锥形瓶用待测液润洗
E.NaOH标准液保存时间过长,有部分变质
(6)根据表中记录数据,通过计算可得,该盐酸浓度为:_______ mol/L
①用蒸馏水洗涤碱式滴定管,注入0.2000mol/L的标准NaOH溶液至“0”刻度线以上;
②固定好滴定管并使滴定管尖嘴充满液体;
③调节液面至“0”或“0”刻度线以下,并记下读数;
④量取20.00mL待测液注入洁净的锥形瓶中,并加入2滴甲基橙溶液;
⑤用标准液滴定至终点,记下滴定管液面读数。
⑥重复以上滴定操作2-3次。
请回答
(1)以上步骤有错误的是(填编号)
(2)步骤④中,量取20.00mL待测液应使用
(3)步骤⑤滴定时眼睛应注视
(4)若滴定开始和结束时,碱式滴定管中的液面如图所示:则所用氢氧化钠溶液的体积为

(5)以下是实验数据记录表
| 滴定次数 | 盐酸体积(mL) | NaOH溶液体积读数(mL) | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.00 | 18.10 |
| 2 | 20.00 | 0.00 | 16.20 |
| 3 | 20.00 | 0.00 | 16.16 |
A.锥形瓶装液前,留有少量蒸馏水
B.滴定结束时,仰视计数
C.滴定前滴定管尖嘴无气泡,滴定结束有气泡
D.锥形瓶用待测液润洗
E.NaOH标准液保存时间过长,有部分变质
(6)根据表中记录数据,通过计算可得,该盐酸浓度为:
用0.2000mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:
①用蒸馏水洗涤碱式滴定管,注入0.2000mol·L-1的标准NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线以下,并记下读数
④量取20.00mL待测液注入洁净的锥形瓶中,并加入2滴甲基橙溶液
⑤用标准液滴定至终点,记下滴定管液面读数
⑥重复以上滴定操作2~3次
请回答下列问题
(1)以上步骤有错误的是___ (填编号)。
(2)步骤④中,量取20.00mL待测液应使用___ (填仪器名称)。
(3)步骤⑤滴定时眼睛应注视___ ;判断到达滴定终点的依据是____ 。
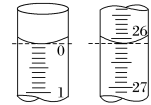
(4)若滴定开始和结束时,碱式滴定管中的液面如图所示,则所用盐酸的体积为____ mL。
(5)以下是实验数据记录表
从表中可以看出,第1次滴定记录的NaOH溶液体积明显多于后两次的体积,其可能的原因是___ 。
A.锥形瓶装液前,留有少量蒸馏水
B.滴定结束时,仰视计数
C.滴定前滴定管尖嘴无气泡,滴定结束有气泡
D.锥形瓶用待测液润洗
E.NaOH标准液保存时间过长,有部分变质
(6)根据表中记录数据,通过计算可得,该盐酸浓度为___ mol·L-1。
(7)请写出该反应的热化学方程式___ 。
①用蒸馏水洗涤碱式滴定管,注入0.2000mol·L-1的标准NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线以下,并记下读数
④量取20.00mL待测液注入洁净的锥形瓶中,并加入2滴甲基橙溶液
⑤用标准液滴定至终点,记下滴定管液面读数
⑥重复以上滴定操作2~3次
请回答下列问题
(1)以上步骤有错误的是
(2)步骤④中,量取20.00mL待测液应使用
(3)步骤⑤滴定时眼睛应注视
(4)若滴定开始和结束时,碱式滴定管中的液面如图所示,则所用盐酸的体积为

(5)以下是实验数据记录表
| 滴定次数 | 盐酸体积(mL) | NaOH溶液体积(mL) | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.00 | 18.10 |
| 2 | 20.00 | 0.00 | 16.20 |
| 3 | 20.00 | 0.00 | 16.16 |
A.锥形瓶装液前,留有少量蒸馏水
B.滴定结束时,仰视计数
C.滴定前滴定管尖嘴无气泡,滴定结束有气泡
D.锥形瓶用待测液润洗
E.NaOH标准液保存时间过长,有部分变质
(6)根据表中记录数据,通过计算可得,该盐酸浓度为
(7)请写出该反应的热化学方程式
用0.2000 mol/L的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:
①用蒸馏水洗涤碱式滴定管,注入0.2000 mol/L的标准NaOH溶液至“0”刻度线以上;②固定好滴定管并使滴定管尖嘴充满液体;③调节液面至“ 0”或“0”刻度线稍下,并记下读数;④量取20.00 mL待测液注入洁净的锥形瓶中,并加入3滴甲基橙溶液;⑤用标准液滴定至终点,记下滴定管液面读数。⑥重复以上滴定操作2-3次。请回答:
(1)以上步骤有错误的是(填编号)____________________
(2)步骤④中,量取20.00 mL待测液应使用_________________ (填仪器名称)
(3)步骤⑤滴定时眼睛应注视______________________________ ;判断到达滴定终点的依据是:______________________________________ 。
(4)以下是实验数据记录表
从表中可以看出,第1次滴定记录的NaOH溶液体积明显多于后两次的体积,其可能的原因是__________
A. 锥形瓶装液前,留有少量蒸馏水 B. 滴定结束时,仰视读数
C.滴定前滴定管尖嘴无气泡,滴定结束有气泡 D.锥形瓶用待测液润洗
E. NaOH标准液保存时间过长,有部分变质
(5)根据表中记录数据,通过计算可得,该盐酸浓度为:____________ mol/L
①用蒸馏水洗涤碱式滴定管,注入0.2000 mol/L的标准NaOH溶液至“0”刻度线以上;②固定好滴定管并使滴定管尖嘴充满液体;③调节液面至“ 0”或“0”刻度线稍下,并记下读数;④量取20.00 mL待测液注入洁净的锥形瓶中,并加入3滴甲基橙溶液;⑤用标准液滴定至终点,记下滴定管液面读数。⑥重复以上滴定操作2-3次。请回答:
(1)以上步骤有错误的是(填编号)
(2)步骤④中,量取20.00 mL待测液应使用
(3)步骤⑤滴定时眼睛应注视
(4)以下是实验数据记录表
| 滴定 次数 | 盐酸体积 (mL) | NaOH溶液体积读数(mL) | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.00 | 18.10 |
| 2 | 20.00 | 0.00 | 16.20 |
| 3 | 20.00 | 0.00 | 16.16 |
从表中可以看出,第1次滴定记录的NaOH溶液体积明显多于后两次的体积,其可能的原因是
A. 锥形瓶装液前,留有少量蒸馏水 B. 滴定结束时,仰视读数
C.滴定前滴定管尖嘴无气泡,滴定结束有气泡 D.锥形瓶用待测液润洗
E. NaOH标准液保存时间过长,有部分变质
(5)根据表中记录数据,通过计算可得,该盐酸浓度为:
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


