解答题-工业流程题 较难0.4 引用1 组卷223
硫酸亚铁晶体( ,摩尔质量为278g/mol)是一种重要的无机化工原料,应用广泛。
,摩尔质量为278g/mol)是一种重要的无机化工原料,应用广泛。
Ⅰ.硫酸亚铁晶体的制备
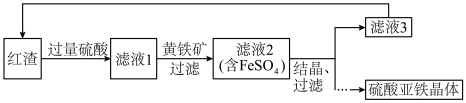
用焙烧铁矿石产生的工业废渣(主要成分为 ,含有少量FeO、
,含有少量FeO、 )为原料生产硫酸亚铁晶体的工艺流程如下。
)为原料生产硫酸亚铁晶体的工艺流程如下。
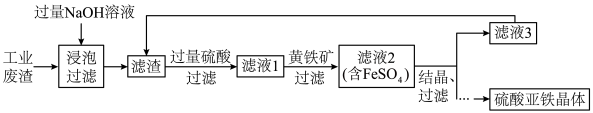
(1)加入过量NaOH溶液进行浸泡时发生反应的离子方程式为________ 。
(2)黄铁矿的主要成分是 ,其作用是
,其作用是________ 。是否可以使用Cu粉替代
________ (填“是”或“否”),解释原因________ 。
(3)为检验加入过量的黄铁矿是否充分起到作用,可以向滤液2中加入的试剂为________ (填化学式),通过________ 现象判断已经充分发挥作用。为灵敏检验滤液2中主要的金属阳离子,选择的试剂为________ (填化学式)。
(4)将滤液3(母液)循环加入滤渣中的目的是________ ,发生反应的离子方程式为________ 。
(5)配制250mL0.2mol/L的 溶液,需称量硫酸亚铁晶体质量为
溶液,需称量硫酸亚铁晶体质量为________ g,下列操作会导致所配溶液浓度偏高的是________ (填字母)。
A.所称取的晶体失去了部分结晶水 B.转移溶液前容量瓶中存在少量蒸馏水
C.定容前未洗涤烧杯和玻璃棒 D.定容时俯视刻度线
(6)产品纯度测定
已知:
取ag硫酸亚铁晶体产品,用稀 和新煮沸过的蒸馏水溶解后,立即滴入
和新煮沸过的蒸馏水溶解后,立即滴入 溶液至恰好完全反应,共消耗
溶液至恰好完全反应,共消耗 溶液bmL。
溶液bmL。 的质量分数是
的质量分数是________ 。
Ⅱ.用制备颜料铵铁蓝
(7) 用稀
用稀 溶解后,加入
溶解后,加入 溶液和
溶液和 溶液,加热,产生白色沉淀
溶液,加热,产生白色沉淀 。酸性条件下再加入
。酸性条件下再加入 溶液,充分反应,得到铵铁蓝。补全离子方程式:
溶液,充分反应,得到铵铁蓝。补全离子方程式:_______
 ________
________ ________+________+________
________+________+________
Ⅰ.硫酸亚铁晶体的制备
用焙烧铁矿石产生的工业废渣(主要成分为

(1)加入过量NaOH溶液进行浸泡时发生反应的离子方程式为
(2)黄铁矿的主要成分是
(3)为检验加入过量的黄铁矿是否充分起到作用,可以向滤液2中加入的试剂为
(4)将滤液3(母液)循环加入滤渣中的目的是
(5)配制250mL0.2mol/L的
A.所称取的晶体失去了部分结晶水 B.转移溶液前容量瓶中存在少量蒸馏水
C.定容前未洗涤烧杯和玻璃棒 D.定容时俯视刻度线
(6)产品纯度测定
已知:
取ag硫酸亚铁晶体产品,用稀
Ⅱ.用制备颜料铵铁蓝
(7)
23-24高一下·黑龙江哈尔滨·开学考试
类题推荐  是一种重要的化工产品。以菱锰矿(主要成分为
是一种重要的化工产品。以菱锰矿(主要成分为 ,还含有
,还含有 、FeO、CoO等)为原料制备
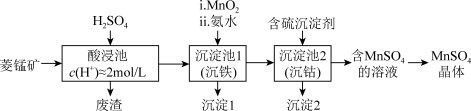
、FeO、CoO等)为原料制备 的工艺流程如图。
的工艺流程如图。

资料:金属离子沉淀的pH
(1)进入酸浸池之前先要对矿石进行粉碎,目的是___________ 。
(2)酸浸后所得溶液的金属阳离子包括 、
、 、
、___________ 。
(3)沉淀池1中,先加 氧化后再加氨水。写出加
氧化后再加氨水。写出加 时发生反应的离子方程式:
时发生反应的离子方程式:___________ 。
(4)沉淀池2中,不能用NaOH代替含硫沉淀剂,原因是___________ 。
(5)如图为 和
和 的溶解度曲线。从“含
的溶解度曲线。从“含 的溶液”中提取“
的溶液”中提取“ 晶体”的操作为蒸发结晶,
晶体”的操作为蒸发结晶,___________ 洗涤,干燥。

(6)受实际条件限制,“酸浸池”所得的废渣中还含有锰元素,其含量测定方法如下。
ⅰ.称取ag废渣,加酸将锰元素全部溶出成 ,过滤,将滤液定容于
,过滤,将滤液定容于 容量瓶中;
容量瓶中;
ⅱ.取 溶液于锥形瓶中,加入少量催化剂和过量
溶液于锥形瓶中,加入少量催化剂和过量 溶液,加热、充分反应后,煮沸溶液使过量的
溶液,加热、充分反应后,煮沸溶液使过量的 分解。
分解。
ⅲ.加入指示剂,用 溶液滴定。滴定至终点时消耗
溶液滴定。滴定至终点时消耗 溶液的体积为
溶液的体积为 ,
, 重新变成
重新变成 .
.
①补全步骤ⅱ中反应的离子方程式:___________ 。

②废渣中锰元素的质量分数为___________ 。  是一种重要的化工产品。以菱锰矿(主要成分为
是一种重要的化工产品。以菱锰矿(主要成分为 ,还含有
,还含有 、FeO、CoO等)为原料制备
、FeO、CoO等)为原料制备 的工艺流程如下图。
的工艺流程如下图。
资料:金属离子沉淀的pH
(1)酸浸后所得溶液的金属阳离子包括 、
、 、
、_______ 。
(2)沉淀池1中,先加 充分反应后再加氨水,写出加
充分反应后再加氨水,写出加 时发生反应的离子方程式:
时发生反应的离子方程式:_______ 。
(3)沉淀池2中,不能用NaOH代替含硫沉淀剂,原因是_______ 。
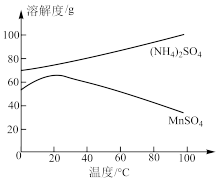
(4)图为 和
和 的溶解度曲线。从“含
的溶解度曲线。从“含 的溶液”中提取“
的溶液”中提取“ 晶体”的操作为
晶体”的操作为_______ 、洗涤、干燥。
(5)受实际条件限制,“酸浸池”所得的废渣中还含有锰元素,其含量测定方法如下。
i.称取a g废渣,加酸将锰元素全部溶出成 ,过滤,将滤液定容于100mL容量瓶中;
,过滤,将滤液定容于100mL容量瓶中;
ii.取25.00 mL溶液于锥形瓶中,加入少量催化剂和过量 溶液,加热、充分反应后,煮沸溶液使过量的
溶液,加热、充分反应后,煮沸溶液使过量的 分解。
分解。
iii.加入指示剂,用b mol/L 溶液滴定,滴定至终点时消耗
溶液滴定,滴定至终点时消耗 溶液的体积为c mL ,
溶液的体积为c mL , 重新变成
重新变成 。
。
①补全步骤ⅱ中反应的离子方程式:_______ 。
 +
+ +_______
+_______
 +_______+_______
+_______+_______
②废渣中锰元素的质量分数为_______ 。

资料:金属离子沉淀的pH
金属离子 | ||||
开始沉淀 | 1.5 | 6.3 | 7.4 | 7.6 |
完全沉淀 | 2.8 | 8.3 | 9.4 | 10.2 |
(2)酸浸后所得溶液的金属阳离子包括
(3)沉淀池1中,先加
(4)沉淀池2中,不能用NaOH代替含硫沉淀剂,原因是
(5)如图为

(6)受实际条件限制,“酸浸池”所得的废渣中还含有锰元素,其含量测定方法如下。
ⅰ.称取ag废渣,加酸将锰元素全部溶出成
ⅱ.取
ⅲ.加入指示剂,用
①补全步骤ⅱ中反应的离子方程式:

②废渣中锰元素的质量分数为

资料:金属离子沉淀的pH
| 金属离子 | Fe3+ | Fe2+ | Co2+ | Mn2+ |
| 开始沉淀 | 1.5 | 6.3 | 7.4 | 7.6 |
| 完全沉淀 | 2.8 | 8.3 | 9.4 | 10.2 |
(2)沉淀池1中,先加
(3)沉淀池2中,不能用NaOH代替含硫沉淀剂,原因是
(4)图为

(5)受实际条件限制,“酸浸池”所得的废渣中还含有锰元素,其含量测定方法如下。
i.称取a g废渣,加酸将锰元素全部溶出成
ii.取25.00 mL溶液于锥形瓶中,加入少量催化剂和过量
iii.加入指示剂,用b mol/L
①补全步骤ⅱ中反应的离子方程式:
②废渣中锰元素的质量分数为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网