解答题-结构与性质 较难0.4 引用1 组卷140
钠、镁、铝、铜及其化合物在生活中具有重要作用。回答下列问题:
(1)基态Cu+的价层轨道表示式为___________ 。
(2)Na、Mg、Al的第一电离能由大到小的顺序为___________ (填元素符号)。
(3)铝离子电池一般采用离子液体作为电解质,某含铝离子液体的结构如图:
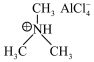
该化合物中阴离子的空间构型为___________ ;传统的有机溶剂大多易挥发,而离子液体相对难挥发,原因是___________ 。
(4)几种氧化物的化学键中离子键成分的百分数和氧化物的熔点如下表:
离子键成分的百分数:MgO高于Al2O3,其原因是___________ ;熔点:MgO高于Na2O,从结构的角度解释其原因是___________ 。
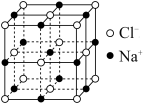
(5)NaCl的晶胞如图所示。NaCl的密度为ρ g/cm3,在NaCl晶体里Na+和Cl-的最短距离为apm,则阿伏加德罗常数的值为___________ (用含a、ρ的表达式表示)。
(1)基态Cu+的价层轨道表示式为
(2)Na、Mg、Al的第一电离能由大到小的顺序为
(3)铝离子电池一般采用离子液体作为电解质,某含铝离子液体的结构如图:

该化合物中阴离子的空间构型为
(4)几种氧化物的化学键中离子键成分的百分数和氧化物的熔点如下表:
| 氧化物 | Na2O | MgO | Al2O3 |
| 离子键的百分数/% | 62 | 50 | 41 |
| 熔点/℃ | 1132 | 2852 | 2054 |
(5)NaCl的晶胞如图所示。NaCl的密度为ρ g/cm3,在NaCl晶体里Na+和Cl-的最短距离为apm,则阿伏加德罗常数的值为

23-24高二下·吉林长春·开学考试
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


 b.
b.