解答题-实验探究题 适中0.65 引用2 组卷554
某学习小组欲探究苯酚的化学性质。
回答下列问题:
Ⅰ.探究苯酚的酸性。
小组分别进行了下列实验:
(1)实验______ (填编号)的对比现象能说明苯酚的酸性较弱。
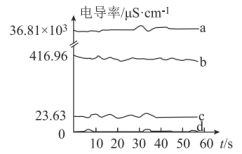
(2)为进一步探究苯酚的酸性,学习小组采用电位滴定法进行测定。分别取20mL浓度均为 的盐酸、醋酸溶液、苯酚溶液、乙醇溶液于四个50mL的烧杯中,用电导率传感器测定其电导率,用数据采集器和计算机进行分析,数据结果如图所示:
的盐酸、醋酸溶液、苯酚溶液、乙醇溶液于四个50mL的烧杯中,用电导率传感器测定其电导率,用数据采集器和计算机进行分析,数据结果如图所示:______ (填图中字母)。
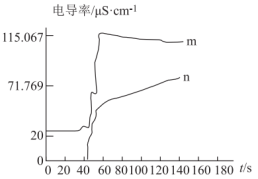
设计实验相关量如表所示,分别向蒸馏水和苯酚溶液中逐滴滴入浓溴水,同时进行磁力搅拌,观察并记录电导率的变化,电导率随时间的变化曲线如图所示:

______ ,
______ 。
(4)苯酚溶液与浓溴水反应的电导率曲线为______ (填图中字母);根据曲线信息推断该反应为______ (填“取代”或“加成”)反应;结合化学反应方程式和必要的文字说明推断理由:____________ 。
(5)实验采用的苯酚溶液为稀溶液,溴水为浓溶液,若两者的浓度关系相反,则产生的后果是____________ 。
(6)写出苯酚在生产生活中的一种用途:____________ 。
回答下列问题:
Ⅰ.探究苯酚的酸性。
小组分别进行了下列实验:
实验编号 | 实验内容 | 实验现象 |
实验1 | 向盛有苯酚溶液的试管中逐滴加入5%NaOH溶液并振荡 | 无明显现象 |
实验2 | 向盛有苯酚浊液的试管中逐滴加入5%NaOH溶液并振荡 | 溶液变澄清 |
实验3 | 向盛有苯酚溶液的试管中加入几滴紫色石蕊溶液 | 无明显现象 |
(2)为进一步探究苯酚的酸性,学习小组采用电位滴定法进行测定。分别取20mL浓度均为
②推测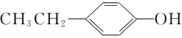 、
、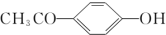 、
、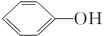 的酸性强弱:
的酸性强弱:
设计实验相关量如表所示,分别向蒸馏水和苯酚溶液中逐滴滴入浓溴水,同时进行磁力搅拌,观察并记录电导率的变化,电导率随时间的变化曲线如图所示:
物质 | 溶液浓度 | 溶液体积 | 加入浓溴水滴数 |
蒸馏水 | 0 | 30 | 10 |
苯酚溶液 | 0.1 |
(4)苯酚溶液与浓溴水反应的电导率曲线为
(5)实验采用的苯酚溶液为稀溶液,溴水为浓溶液,若两者的浓度关系相反,则产生的后果是
(6)写出苯酚在生产生活中的一种用途:
2024·广东·模拟预测
类题推荐
某校化学兴起小组进行了以下两个实验:
实验一:通过以下实验来探究 和
和 两种物质的性质。
两种物质的性质。
(1)观察可知, 和
和 均为
均为___________ 色的固体。
(2)20℃时,称取两种固体各 ,分别放入两个小烧杯中,再各滴加
,分别放入两个小烧杯中,再各滴加 蒸馏水,振荡,发现
蒸馏水,振荡,发现 固体完全溶解,而
固体完全溶解,而 固体有剩余。由此得到结论
固体有剩余。由此得到结论___________ 。
(3)结合以下实验回答问题。
①实验I所得实验数据证明,溶解时吸收热量的物质是___________ 。
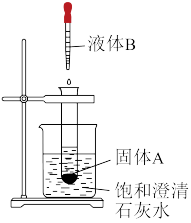
②实验Ⅱ中试管B中的现象为___________ ;通过实验Ⅱ说明 的热稳定性
的热稳定性___________ 于 。(填“强”或“弱”)
。(填“强”或“弱”)
③实验Ⅲ中的现象证明, 与盐酸反应是分步进行的,发生反应的离子方程式为:第一步:
与盐酸反应是分步进行的,发生反应的离子方程式为:第一步: ;第二步:
;第二步:___________ 。
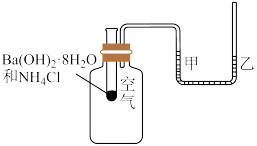
实验二:为研究 的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
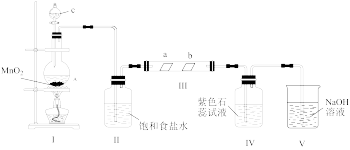
(4)装置I中仪器c的名称是___________ ,写出实验室用二氧化锰和浓盐酸制备氯气的化学方程式___________ 。
(5)装置Ⅱ的作用是___________ 。
(6)若产生 足量,实验过程中装置Ⅳ中的实验现象
足量,实验过程中装置Ⅳ中的实验现象___________ 。
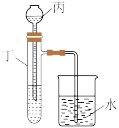
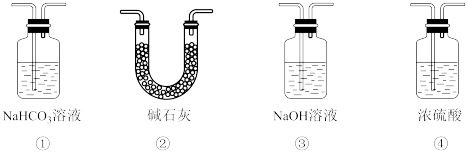
(7)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的___________ 装置(填序号)。
(8)该小组同学向盛有蒸馏水的试管中通入氯气后,再用强光照射氯水,同时使用数据采集器采集数据如下:
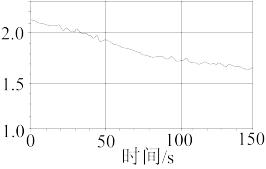
该小组同学采集的数据是___________ (填字母)。
a.水的 b.氯离子的浓度 c.氧气的体积分数
b.氯离子的浓度 c.氧气的体积分数
实验一:通过以下实验来探究
(1)观察可知,
(2)20℃时,称取两种固体各
(3)结合以下实验回答问题。
| 编号 | 实验内容 | 实验数据或者现象 |
| 实验I | 利用传感器探究两种物质分别溶水时的温度变化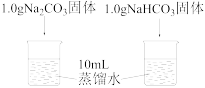 | 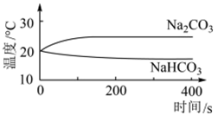 |
| 实验Ⅱ | 探究两种物质的热稳定性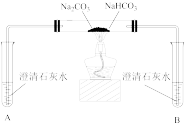 | 一段时间后,A中无明显现象,B中_____ |
| 实验Ⅲ | 探究两种物质分别与盐酸反应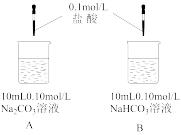 | A中开始无大量气泡,一段时间后产生大量气泡;B中立即产生大量气泡。 |
②实验Ⅱ中试管B中的现象为
③实验Ⅲ中的现象证明,
实验二:为研究

(4)装置I中仪器c的名称是
(5)装置Ⅱ的作用是
(6)若产生
(7)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的

(8)该小组同学向盛有蒸馏水的试管中通入氯气后,再用强光照射氯水,同时使用数据采集器采集数据如下:

该小组同学采集的数据是
a.水的
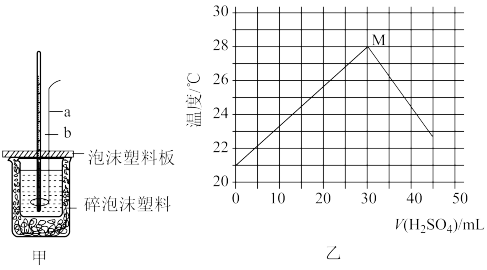
离子反应是中学化学中重要的反应类型。某学习小组为证实Ba(OH)2溶液和H2SO4溶液的反应是离子反应,设计如图1所示实验:
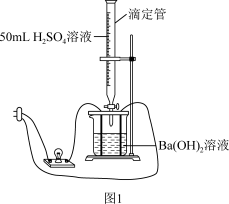
[实验原理]
(1)溶液的导电性由溶液中离子的浓度及离子电荷数决定。观察图1中___________ , 据此判断溶液中自由移动的离子浓度的变化,从而证明该反应是离子反应。
[实验过程与结论]
(2)完成下表空白处
(3)整个过程中混合溶液的导电能力(用电流强度I表示)可近似地用图2中的___________ (填字母)曲线表示。
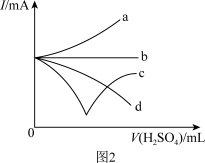
(4)下列三种情况下,与上述实验中离子方程式相同的是___________ (填字母)。
A.向NaHSO4溶液中逐滴加入Ba(OH)2溶液至SO 恰好完全沉淀
恰好完全沉淀
B.向NaHSO4溶液中逐滴加入Ba(OH)2溶液至溶液显中性
C.向NaHSO4溶液中逐滴加入Ba( OH)2溶液至过量
[实验拓展]
已知某无色透明溶液中可能含有下列离子中的若干种:K+、Mg2+、Fe3+、Ba2+、SO 、OH-、CO
、OH-、CO 和Cl-,现取该溶液进行如下实验:
和Cl-,现取该溶液进行如下实验:
I.取少量原溶液,滴入紫色石蕊试液,溶液呈蓝色;
II.取少量原溶液,滴入BaCl2溶液,无明显现象;
III.取少量原溶液,先滴加足量稀硝酸,再加入AgNO3溶液,有白色沉淀产生;
IV.取少量原溶液,滴入少量稀H2SO4有白色沉淀产生。
回答下列问题:
(5)根据上述现象判断,原溶液中肯定存在的离子是___________ ;肯定不存在的离子是___________ 。
(6)写出实验III中发生反应的离子方程式___________ 、___________ 。
(7)若溶液中各离子的浓度相等,则可确定溶液中一定___________ (填“有”或“没有”)某种可能存在的离子。

[实验原理]
(1)溶液的导电性由溶液中离子的浓度及离子电荷数决定。观察图1中
[实验过程与结论]
(2)完成下表空白处
| 实验步骤 | 实验现象 | 实验结论 |
| 连接好装置,向烧杯中加入25 mL 1 mol·L-1的Ba(OH)2溶液和2滴酚酞溶液,逐滴滴加1 mol·L-1的H2SO4溶液直至过量,边滴加边振荡 | Ba(OH)2溶液和H2SO4元溶液的反应是离子反应 |

(4)下列三种情况下,与上述实验中离子方程式相同的是
A.向NaHSO4溶液中逐滴加入Ba(OH)2溶液至SO
B.向NaHSO4溶液中逐滴加入Ba(OH)2溶液至溶液显中性
C.向NaHSO4溶液中逐滴加入Ba( OH)2溶液至过量
[实验拓展]
已知某无色透明溶液中可能含有下列离子中的若干种:K+、Mg2+、Fe3+、Ba2+、SO
I.取少量原溶液,滴入紫色石蕊试液,溶液呈蓝色;
II.取少量原溶液,滴入BaCl2溶液,无明显现象;
III.取少量原溶液,先滴加足量稀硝酸,再加入AgNO3溶液,有白色沉淀产生;
IV.取少量原溶液,滴入少量稀H2SO4有白色沉淀产生。
回答下列问题:
(5)根据上述现象判断,原溶液中肯定存在的离子是
(6)写出实验III中发生反应的离子方程式
(7)若溶液中各离子的浓度相等,则可确定溶液中一定
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网