解答题-实验探究题 较难0.4 引用5 组卷548
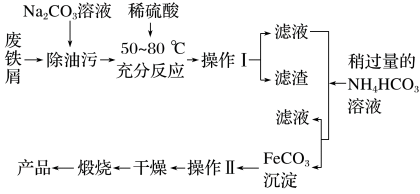
实验室利用含钴废渣[含 、
、 等]制备磁性材料
等]制备磁性材料 。回答下列问题:
。回答下列问题:
I.稀硫酸的配制。
(1)实验室里需要:450mL 溶液,用98%浓硫酸(密度为
溶液,用98%浓硫酸(密度为 )配制该溶液时,所需的浓硫酸的体积为
)配制该溶液时,所需的浓硫酸的体积为_______ (保留1位小数)mL。
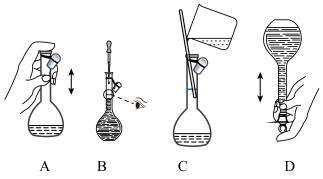
(2)下图关于容量瓶的操作,正确的是_______ 。
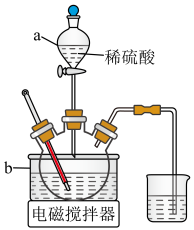
Ⅱ.浸取,将一定量的钴渣粉与 溶液配成悬浊液,加入三颈烧瓶中(装置如图),70℃通过仪器a缓慢滴加稀硫酸,充分反应,过滤。
溶液配成悬浊液,加入三颈烧瓶中(装置如图),70℃通过仪器a缓慢滴加稀硫酸,充分反应,过滤。_______ 作为最佳传热介质。
(5)该过程中, 转化为
转化为 的离子方程式为
的离子方程式为_______ 。
Ⅲ.沉钴。Co(Ⅱ)盐溶液可以形成 、
、 和
和 等多种形式的沉淀。
等多种形式的沉淀。
已知:向0.100mol/L溶液中滴加NaOH溶液调节pH, 时开始出现
时开始出现 沉淀。
沉淀。
(6)向除杂后的 溶液中加入
溶液中加入 溶液或
溶液或 溶液作沉淀剂,可得到
溶液作沉淀剂,可得到 ,不能用同浓度的
,不能用同浓度的 溶液代替
溶液代替 溶液的原因是
溶液的原因是_______ 。
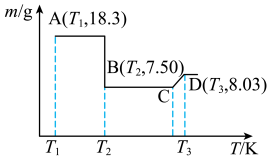
Ⅳ.制备 ,将所得的18.3g草酸钴晶体(
,将所得的18.3g草酸钴晶体( )高温灼烧,其热重分析图如图:
)高温灼烧,其热重分析图如图:_______ ,CD段发生反应的化学方程式为_______ 。
I.稀硫酸的配制。
(1)实验室里需要:450mL
(2)下图关于容量瓶的操作,正确的是
| A.定容时俯视容量瓶刻度线 |
| B.容量瓶未干燥处理 |
| C.定容加水时超过刻度线后,立即吸出多余的水 |
| D.将溶液从烧杯转移到容量瓶中后没有洗涤烧杯 |
Ⅱ.浸取,将一定量的钴渣粉与
(5)该过程中,
Ⅲ.沉钴。Co(Ⅱ)盐溶液可以形成
已知:向0.100mol/L溶液中滴加NaOH溶液调节pH,
(6)向除杂后的
Ⅳ.制备
2024·四川成都·二模
类题推荐
Ⅰ.“84消毒液”有效成分是NaClO。某次实验需要使用900mL0.2mol/L的NaClO溶液,欲用NaClO固体配制该溶液。
(1)计算所需NaClO固体的质量为________ g。
(2)配制溶液时,下图不需要的仪器是________ (写仪器名称)。
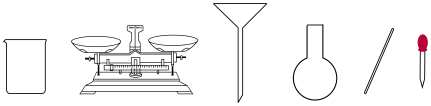
(3)写出配制溶液时的正确操作顺序(用字母表示,每个字母只能用一次)________ 。
A.洗涤 B.称量、溶解 C.转移 D.摇匀 E.定容
(4)配制过程中,下列操作导致溶液浓度偏小的是________(填序号)。
Ⅱ.某班同学通过实验探究 、
、 的性质。回答下列问题:
的性质。回答下列问题:
(5)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol/L的溶液。刻制印刷电路板时用氯化铁溶液作为“腐蚀液”,发生反应的离子方程式是________ 。
(6)甲组同学取 溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明
溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明 可将
可将 氧化。
氧化。 溶液与氯水反应的离子方程式为
溶液与氯水反应的离子方程式为________ 。
(7)乙组同学认为甲组的实验不够严谨,该组同学在 溶液中先加入0.5mL煤油(不溶于水,密度比水小),再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红。煤油的作用是:
溶液中先加入0.5mL煤油(不溶于水,密度比水小),再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红。煤油的作用是:________ 。
(8)向 溶液中滴加NaOH溶液,现象是
溶液中滴加NaOH溶液,现象是________ ;沉淀变色的原因是________ (用化学方程式解释)。
(1)计算所需NaClO固体的质量为
(2)配制溶液时,下图不需要的仪器是

(3)写出配制溶液时的正确操作顺序(用字母表示,每个字母只能用一次)
A.洗涤 B.称量、溶解 C.转移 D.摇匀 E.定容
(4)配制过程中,下列操作导致溶液浓度偏小的是________(填序号)。
| A.加水定容时俯视刻度线 |
| B.容量瓶未干燥处理 |
| C.定容加水时超过刻度线后,立即吸出多余的水 |
| D.溶液从烧杯转移到容量瓶中后没有洗涤烧杯 |
Ⅱ.某班同学通过实验探究
(5)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol/L的溶液。刻制印刷电路板时用氯化铁溶液作为“腐蚀液”,发生反应的离子方程式是
(6)甲组同学取
(7)乙组同学认为甲组的实验不够严谨,该组同学在
(8)向
某工厂以镍废渣(主要成分为Ni含少量Fe、Fe3O4、Al2O3和不溶性杂质等)为原料制备翠矾(NiSO4•7H2O),其生产工艺如图:
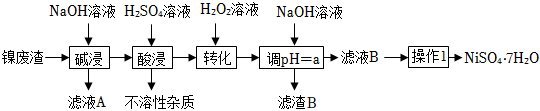
该流程中几种金属离子生成对应氢氧化物沉淀的pH如表:
回答下列问题:
(1)配制NaOH溶液时,下列操作导致溶液浓度偏高的是 ___________。
(2)“滤液A”中主要溶质的化学式为 ___________ 。
(3)“转化”过程中加入H2O2的目的是___________ ,该过程用离子方程式表示为 ___________ ;“转化”过程中温度不宜过高,原因是 ___________ 。
(4)调节pH=a,则a的取值范围是___________ 。证明杂质离子已经被完全除去的实验操作及现象是:取少量滤液B于试管中,___________ 。
(5)“操作1”的具体操作是控制pH、蒸发浓缩、冷却结晶、___________ 、___________ 、干燥。
(6)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH.写出该反应的离子方程式___________ 。

该流程中几种金属离子生成对应氢氧化物沉淀的pH如表:
| 金属离子 | 开始沉淀的pH | 完全沉淀的pH |
| Fe3+ | 2.7 | 3.7 |
| Fe2+ | 7.6 | 9.7 |
| Ni2+ | 7.1 | 9.2 |
(1)配制NaOH溶液时,下列操作导致溶液浓度偏高的是 ___________。
| A.容量瓶用蒸馏水洗净之后未干燥,直接用于溶液的配制 |
| B.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒 |
| C.摇匀后,发现液面低于刻度线,又滴加蒸馏水至与刻度线相切 |
| D.定容时,俯视刻度线 |
(3)“转化”过程中加入H2O2的目的是
(4)调节pH=a,则a的取值范围是
(5)“操作1”的具体操作是控制pH、蒸发浓缩、冷却结晶、
(6)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH.写出该反应的离子方程式
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网