单选题 较难0.4 引用1 组卷55
常温下, 在Na2CO3溶液中发生反应,可能生成
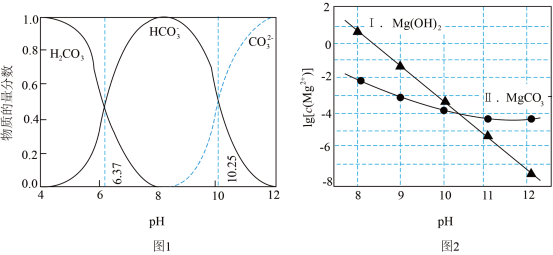
在Na2CO3溶液中发生反应,可能生成 或MgCO3。图1表示Na2CO3溶液中各含碳物种的物质的量分数与溶液pH的关系;图2中曲线Ⅰ的离子浓度关系符合
或MgCO3。图1表示Na2CO3溶液中各含碳物种的物质的量分数与溶液pH的关系;图2中曲线Ⅰ的离子浓度关系符合 ;曲线Ⅱ的离子浓度关系符合
;曲线Ⅱ的离子浓度关系符合 。利用平衡原理分析,下列说法正确的是
。利用平衡原理分析,下列说法正确的是

| A.常温时, |
| B. |
| C.由图2,当pH=11, |
| D.由图1和图2,在pH=8, |
23-24高二下·湖北恩施·开学考试
类题推荐
利用平衡移动原理,分析一定温度下 在不同pH的Na2CO3体系中的可能产物。
在不同pH的Na2CO3体系中的可能产物。
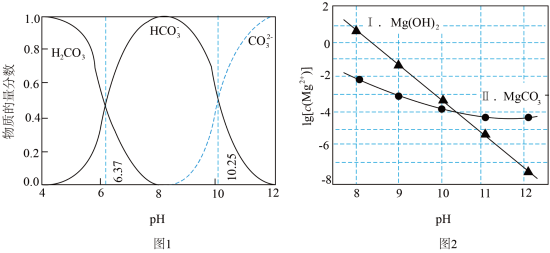
已知:①图1中曲线表示Na2CO3体系中各含碳粒子的物质的量分数与pH的关系。
②图2中曲线I的离子浓度关系符合 ;曲线II的离子浓度关系符合
;曲线II的离子浓度关系符合 。
。 ,不同pH下
,不同pH下 由图1得到。
由图1得到。
下列说法不正确的是
已知:①图1中曲线表示Na2CO3体系中各含碳粒子的物质的量分数与pH的关系。
②图2中曲线I的离子浓度关系符合
下列说法不正确的是
| A.由图1,NaHCO3的水解平衡常数的数量级是 |
| B.由图2,初始状态pH=12、 |
| C.由图2,初始状态pH=9、 |
| D.由图1和图2,初始状态pH=9、 |
碳酸钠溶液显碱性,含 的溶液与碳酸钠溶液反应,产物可能是
的溶液与碳酸钠溶液反应,产物可能是 或
或 。已知:
。已知:
①图1中曲线表示 体系中各含碳粒子的物质的量分数与溶液
体系中各含碳粒子的物质的量分数与溶液 的关系
的关系
②图2中曲线Ⅰ的离子浓度关系符合 ;曲线Ⅱ的离子浓关系符合
;曲线Ⅱ的离子浓关系符合 。注:起始
。注:起始 ,不同
,不同 下
下 由图1得到。下列说法正确的是
由图1得到。下列说法正确的是
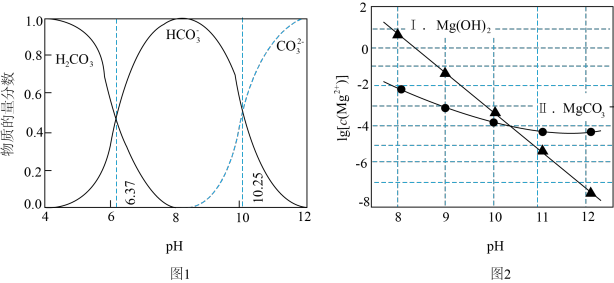
①图1中曲线表示
②图2中曲线Ⅰ的离子浓度关系符合
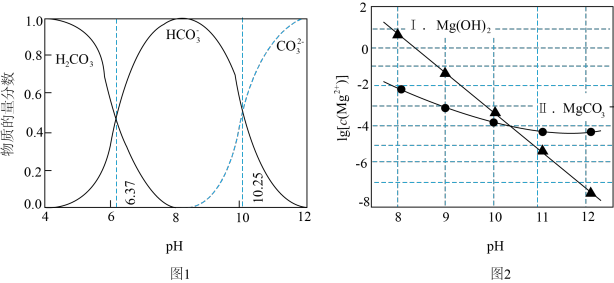
| A.常温下, |
| B.由图2,初始状态 |
| C.由图2,初始状态 |
| D.由图1和图2,初始状态 |
利用平衡移动原理,分析一定温度下 在不同pH的
在不同pH的 体系中的可能产物。
体系中的可能产物。
已知:i.图甲中曲线表示 体系中各含碳粒子的物质的量分数与pH的关系。
体系中各含碳粒子的物质的量分数与pH的关系。
ii.图乙中曲线Ⅰ的离子浓度关系符合 ;曲线Ⅱ的离子浓度关系符合
;曲线Ⅱ的离子浓度关系符合 [注:起始
[注:起始 ,不同pH下
,不同pH下 由图甲得到]。
由图甲得到]。

下列说法不正确的是
已知:i.图甲中曲线表示
ii.图乙中曲线Ⅰ的离子浓度关系符合

下列说法不正确的是
| A.由图甲,pH=10.25, |
| B.由图乙,初始状态pH=11、 |
| C.由图乙,初始状态pH=9、 |
| D.由图甲和图乙,初始状态pH=8、 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


